
科目: 来源: 题型:
【题目】化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素的最外层p轨道上的电子数等于前一电子层电子总数;X原子最外层的p轨道中有一个轨道填充了2个电子。则
(1)X元素基态原子的电子排布式是________,Y原子的价层电子的电子排布图是_________。
(2)YX2的分子构型是____________。
(3)YX2分子中,Y原子的杂化类型是__________,一个YX2分子中含________个π键。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醛分子的结构式如图所示,下列描述正确的是( )
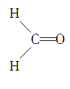
A. 甲醛分子中有4个σ键
B. 甲醛分子中的C原子为sp3杂化
C. 甲醛分子中的O原子为sp杂化
D. 甲醛分子为平面三角形,有一个π键垂直于三角形平面
查看答案和解析>>
科目: 来源: 题型:
【题目】下列推断正确的是( )
A. BF3为三角锥形分子
B. NH的电子式为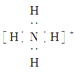 ,离子呈平面正方形结构
,离子呈平面正方形结构
C. CH4分子中的4个C—H键都是氢原子的1s轨道与碳原子的2p轨道形成的s—p σ键
D. CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成C—H σ键
查看答案和解析>>
科目: 来源: 题型:
【题目】下列分子的空间构型可用sp2杂化轨道来解释的是( )
①BF3 ②CH2=CH2 ③![]() ④CH≡CH ⑤NH3 ⑥CH4
④CH≡CH ⑤NH3 ⑥CH4
A. ①②③ B. ①⑤⑥ C. ②③④ D. ③⑤⑥
查看答案和解析>>
科目: 来源: 题型:
【题目】纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。
制备纳米TiO2的方法之一是TiCl4水解生成TiO2xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到粉体TiO2。
用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。
请回答下列问题:
(1)TiCl4水解生成TiO2xH2O的化学方程式为______________________________。
(2)检验TiO2xH2O中Cl-是否被除净的方法是______________________________。
(3)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是__________;使用的仪器除天平、药匙、玻璃棒、烧杯、量筒外,还需要下图中的__________(填字母代号)。
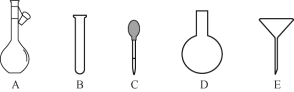
(4)滴定终点的判定现象是________________________________________。
(5)滴定分析时,称取TiO2(摩尔质量为Mg/mol)试样wg,消耗cmol/LNH4Fe(SO4)2 标准溶液VmL,则TiO2质量分数表达式为______________________________。
(6)判断下列操作对TiO2质量分数测定结果的影响(填“偏高”“偏低”或“无影响”)。
①若在配制标准溶液过程中,烧杯中的NH4Fe(SO4)2溶液有少量溅出,使测定结果__________。
②若在滴定终点读取滴定管刻度时,俯视标准液液面,使测定结果__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为測定某工业碱(组成为xNa2CO3·yNaHCO3)中Na2CO3的貭量分數,甲、乙、丙三名同学分別设计并完成了如下实验:
甲同学:准备称取11.40g样品利用图中装置迸行实验,反应后測定装置C中碱石灰増重5.06g。
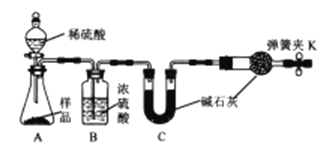
乙同学:准确称取11.40g研细的样品,加热样品至固体完全分解,剩余固体质量为9.54g.
丙同学:准确称取11.40g样品,配成1000mL溶液,量取25.00mL溶液于锥形瓶中,加入指示剂,用0.1500mol/L标准盐酸溶被滴定至终点。完成三次平行实验后,消耗盐酸的体积平均为30.00mL。
(1)如何检查甲同学实验装置的气密性?_______________。
(2)①乙同学需要在______(填仪器名称,下同)将样品研细,在______中加热样品;
②乙同学在实验时需要将固体加热一段时间然后冷却,称量,再加热、冷却、称量,直至最后两次称量的质量差不超过0.10g,其目的是___________ 。
(3)丙同学在实验之前为了确定晶体中是否含有NaHCO3,设计了以下实验方案进行检验。
实验步骤:取少量样品于锥形瓶中加入适量蒸馏水使之溶解,加入几滴酚酞,用0.100mol/L盐酸滴定至溶液由浅红色变无色,记录消耗盐酸的体积为V1;______(填实验操作),记录消耗盐酸的体积为V2,若V2_____V1(填“<、>或=”),说明晶体中含有NaHCO3.
(4)请分析、计算后回答。
①_____同学实验结果错误,其实验失败的原因是___________。
②晶体中Na2CO3的质量分数为____________。(计算结果保留4位有效数字)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 分子式为C9H10O2的同分异构体中,苯环上连有一个甲基的酯类化合物有6种
B. 甲烷性质稳定,不能发生氧化反应
C. 苯和乙烯均能使溴水褪色,但褪色机理不同
D. 有机物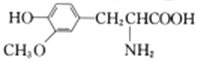 与
与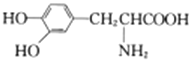 互为同系物
互为同系物
查看答案和解析>>
科目: 来源: 题型:
【题目】新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2 ,电解质为KOH溶液。某研究小组将两个甲烷燃料电池串联后作为电源,进行饱和氯化钠溶液电解实验,如图所示。

回答下列问题:
(1)甲烷燃料电池正极、负极的电极反应分别为________________ 、_______________ ;
(2)闭合K开关后,a、b电极上均有气体产生.其中a电极上得到的是_________(填化学式),电解氯化钠溶液的总反应方程式为___________________;
(3)若每个电池甲烷通入量为1 L(标准状况),且反应完全,则理论上最多能产生的氯气体积为____________L(标准状况);
(4)若饱和氯化钠溶液体积为100mL,电解一段时间后,常温下测得溶液pH为13,若要使溶液恢复到电解前的状态,可向溶液中加(或通)入__________(填写物质的化学式)_________g。
查看答案和解析>>
科目: 来源: 题型:
【题目】湖北随州安陆等地区盛产银杏,银杏叶具有敛肺平喘、活血化淤、止痛的作用,是一种珍贵的中药材。对银杏叶活性成分黄酮类物质的提取常用的技术有溶剂提取法、蒸馏法、升华法、结晶法、超声波提取法等。下列关于分离提纯实验仪器和操作正确的是
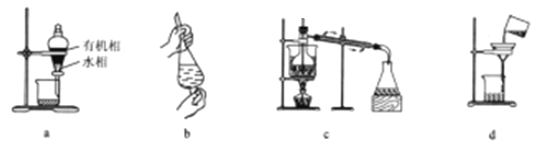
A. 用装置a分液,放出水相后再从分液漏斗下口放出有机相
B. 操作b:银杏油粗产品从银杏叶中分离后,用有机溶剂萃取其中的有效成分,振荡过程中不时地旋开活塞使漏斗内气体放出
C. 用装置c进行蒸馏操作,将有机溶剂分离出去得到银杏叶有效成分黄酮类物质
D. 结晶后利用装置d将晶体与溶剂分离开
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com