
科目: 来源: 题型:
【题目】由于镁合金具有硬度大、密度小、散热性好、抗震性好等优异性能它被用于制笔记本电脑外壳、竞赛自行车车架等。现称取一定质量的镁铝合金样品放入500mL稀硫酸中,固体全部溶解并放出气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如下图所示。

试计算:
(1)合金中Al的质量______。
(2)NaOH溶液的物质的量浓度_____
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科研人员研制出一种室温“可呼吸”Na-CO2电池。放电时该电池“吸入”CO2,充电时“呼出”CO2。吸入CO2时,其工作原理如右图所示。吸收的全部CO2中,有![]() 转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法正确的是( )
转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面。下列说法正确的是( )

A. “吸入”CO2时,钠箔为正极
B. “吸入”CO2时的正极反应:4Na++ 3CO2+ 4e-= 2Na2CO3+ C
C. “呼出”CO2时,Na+向多壁碳纳米管电极移动
D. 标准状况下,每“呼出”22.4 L CO2,转移电子数为0.75 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】CPAE是蜂胶的主要活性成分,其结构简式如图所示。下列说法不正确的是( )

A. CPAE能发生取代反应、加成反应
B. CPAE能使酸性高锰酸钾溶液褪色
C. CPAE可与氢氧化钠溶液发生反应
D. CPAE在酸性条件下水解得到相对分子质量较小的有机物的同分异构体共有9种
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)下列微粒中,只有氧化性的是_____________ (用字母填写,下同),既有氧化性又有还原性的是___________________。
A. Cl2 B. S2— C. H+ D. Na E. FeCl2
(2)在4HCl(浓)+MnO2 ![]() MnCl2+Cl2↑+2H2O反应中
MnCl2+Cl2↑+2H2O反应中
①氧化剂是________,氧化产物是________;
②被氧化与未被氧化的HCl的质量之比为_______,若有7.3gHCl被氧化,转移电子的物质的量为________;。
查看答案和解析>>
科目: 来源: 题型:
【题目】如下图所示操作能实现实验目的的是( )
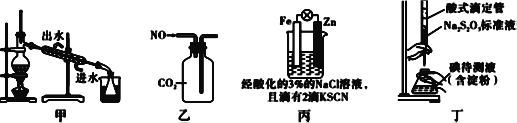
A. 用图甲装置分离碘和四氯化碳,在锥形瓶中收集到碘单质
B. 用图乙装置收集NO气体
C. 用图丙装置验证牺牲阳极的阴极保护法
D. 用图丁装置测定待测液中I2的含量
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是向MgCl2和AlCl3的混合溶液中加入NaOH溶液和盐酸时沉淀的物质的量y mol与加入NaOH溶液和盐酸的体积x mL的关系图,根据图示判断,下列结论中不正确的是

A. N点时溶液中的溶质只有NaCl
B. 原混合溶液中c (MgCl2)∶c (AlCl3)=1∶2
C. c (NaOH)=c (HCl)
D. M点之前加入的是NaOH溶液,M点之后加入的是盐酸
【答案】B
【解析】由图象可知N→M发生Al(OH)3+OH-===AlO2-+2H2O,设氢氧化钠溶液浓度为c,则消耗氢氧化钠0.01cmol,n[Al(OH)3]=n(AlCl3)=0.01cmol;ON消耗氢氧化钠0.05cmol,分别发生MgCl2+2NaOH=Mg(OH)2↓+2NaCl、AlCl3+3NaOH=Al(OH)3↓+3NaCl,可知n(MgCl2)=(0.05cmol-0.01c×3mol)/2=0.01cmol,则c(AlCl3):c(MgCl2)=1:1,M点时溶液成分为NaAlO2,之后继续加入溶液后沉淀质量逐渐增大,此时应加入盐酸,发生反应为:NaAlO2+HCl+H2O= Al(OH)3↓+NaCl,继续加入盐酸沉淀逐渐溶解,生成氯化镁、氯化铝和氯化钠,则消耗的氢氧化钠和HCl的物质的量相等,A.根据分析可知,N点时溶液中的溶质只有NaCl,A正确;B.原混合溶液中c(MgCl2):c(AlCl3)=1:1,B错误;C.由横坐标可知消耗盐酸和氢氧化钠的体积相同,则二者物质的量浓度相同,C正确;D.根据分析可知,M点之前加入的是NaOH溶液,M点之后加入的是盐酸,D正确;答案选B。
【题型】单选题
【结束】
16
【题目】证明某溶液中只含有Fe2+而不含有Fe3+的实验方法是
①先滴加氯水,再滴加KSCN溶液后显红色
②先滴加KSCN溶液,不显红色,再滴加氯水后显红色
③滴加NaOH溶液,先产生白色沉淀,后变灰绿,最后呈红褐色
④只需滴加KSCN溶液
A. ①② B. ②③ C. ③④ D. ①④
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学取海带灰加蒸馏水煮沸2~3 min,冷却,过滤,获得含I-的溶液,并设计以下实验方案,从中提取I2。
![]()
(1)反应1中硫酸的作用是提供酸性环境,则试剂a的作用是__________。
(2)试剂b应选择______(填序号)。
A. CCl4 B. 苯 C. 酒精 D. 醋酸
(3)操作1的名称是_______。实验室里进行操作1需要的玻璃仪器除烧杯外,还需要__________。
(4)反应2为:3I2+6NaOH=5NaI+NaIO3+3H2O,单线桥标出此反应电子转移______。此反应氧化剂是__________,氧化产物是__________。
(5)反应3的离子方程式是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】通常检测SO2含量是否达到排放标准的反应原理是SO2 +H2O2 + BaCl2 ===BaSO4↓+ 2HCl。NA表示阿伏伽德罗常数,下列说法正确的是( )
A. 0.1 mol BaCl2晶体中所含微粒总数为0.1NA
B. 25 ℃时,pH =1的HCl溶液中含有H+的数目为0.1NA
C. 17 g H2O2中含有非极性键数目为0.5NA
D. 生成2.33 g BaSO4沉淀时,转移电子数目为0.01NA
查看答案和解析>>
科目: 来源: 题型:
【题目】化学实验中,如使某步中的有害产物作为另一步的反应物,形成一个循环,就可不再向环境排放该种有害物质。例如:
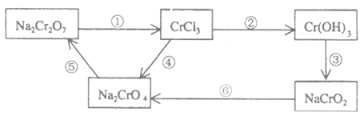
(1)配平并回答问题,用单线桥标出2个反应的电子转移的方向和数目。
反应①为:__Na2Cr2O7+__HCl→__NaCl+__CrCl3+__Cl2↑+____,氧化剂_______,氧化产物__________。
反应⑥为:__ClO3-+__CrO2-+____→__Cl-+__CrO42-+__H2O,还原剂________,还原产物__________。
(2)在上述有编号的步骤中,除了①⑥外,需用氧化剂的步骤是(填编号)______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com