
科目: 来源: 题型:
【题目】常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
C. 第二阶段,Ni(CO)4分解率较低
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目: 来源: 题型:
【题目】三氯化磷(PCl3)是一种重要的有机合成催化剂。实验室常用红磷与干燥的Cl2制取PCl3,装置如图所示。
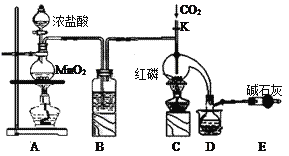
已知: PCl3熔点为-112℃,沸点为75.5℃。易被氧化,遇水易水解。与Cl2反应生成PCl5。
(1)A中反应的化学方程式为__________________。
(2)B中所装试剂名称是___________________,E中碱石灰的作用是___________________。
(3)实验时,检查装置气密性后,向C装置的曲颈甑中加入红磷,打开止水夹K通入干燥的CO2,一段时间后,关闭K,加热曲颈甑至上部有黄色升华物出现时通入氯气,反应立即进行。通干燥CO2的作用是____________________。CO2______(选填“能”或“不能”)用Cl2代替,理由是________________。
(4)D中烧杯中盛装__________,其作用是_______________。
(5)PCl3水解得到亚磷酸(分子式:H3PO3。二元弱酸),写出亚磷酸钠被浓硝酸氧化的离子方程式_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于物质的分类中依次按照强电解质、弱电解质和非电解质排列全部正确的组合是()
A.NaCl HF Cl2B.NaHCO3 NH3·H2O CCl4
C.Ba(OH)2 HCl CuD.AgCl H2SO4 C2H5OH
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中,不正确的是( )
A.光导纤维是以二氧化硅为主要原料制成的
B.二氧化硅溶于水生成硅酸
C.石英、水晶、玛瑙的主要成分都是二氧化硅
D.二氧化硅是一种熔沸点很高、硬度很大的氧化物
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,下列有关溶液的说法正确的是( )
A. pH相等的①NH4Cl、②NH4Al(SO4)2、③NH4HSO4溶液:浓度的大小顺序为①>②>③
B. HA的电离常数Ka =4.93×1010,则等浓度的NaA、HA混合溶液中:c(Na+) >c(HA) >c(A)
C. NaHCO3溶液加水稀释,c(Na+)与c(HCO3)的比值将减小
D. 已知在相同条件下酸性HF >CH3COOH,则物质的量浓度相等的NaF与CH3COOK溶液中:c(Na+) – c(F) >c(K+ ) c(CH3COO)
查看答案和解析>>
科目: 来源: 题型:
【题目】关于下列各装置图的叙述中错误的是( )
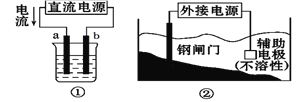
A. 用装置①精炼铜,则a极为粗铜,电解质溶液为CuSO4溶液
B. 装置②中钢闸门应与外接电源的负极相连
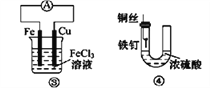
C. 装置③的总反应式是Cu+2Fe3+=Cu2++2Fe2+
D. 装置④中的铁钉几乎没被腐蚀
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组设计如图所示的微型实验装置。实验时,现断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流表指针偏转,下列有关描述正确的是
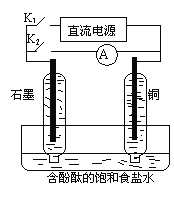
A. 断开K2,闭合K1时,总反应的离子方程式为:2H+ + 2Cl-![]() Cl2↑+H2↑
Cl2↑+H2↑
B. 断开K2,闭合K1时,石墨电极附近溶液变红
C. 断开K1,闭合K2时,铜电极上的电极反应为: Cl2+2e-=2Cl-
D. 断开K1,闭合K2时,石墨电极作正极
查看答案和解析>>
科目: 来源: 题型:
【题目】已知分解1 mol 液态H2O2 ,生成液态H2O和氧气放出热量98kJ,在含少量I-的溶液中,H2O2的分解机理为:
H2O2(l)+ I-(aq) ![]() H2O(l) +IO-(aq) △H1 反应Ⅰ
H2O(l) +IO-(aq) △H1 反应Ⅰ
H2O2(l)+ IO-(aq)![]() H2O(l) +O2(g)+ I-(aq)△H2 反应Ⅱ
H2O(l) +O2(g)+ I-(aq)△H2 反应Ⅱ
下列有关说法错误的是( )
A. 可以用带火星的木条检验H2O2是否开始分解
B. IO-在反应Ⅰ中是氧化产物,在反应Ⅱ中是氧化剂
C. 在H2O2溶液中加入NaIO也能提高H2O2分解速率
D. △H1+△H2 ![]() -98kJ/mol
-98kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂废水中含游离态氯,通过下列实验测定其浓度。
①取水样10.0mL于锥形瓶中,加入10.0mL的KI溶液(足量),发生的反应为:Cl2+2KI=2KC1+I2,滴入指示剂2~3滴。
②取碱式滴定管依次用自来水、蒸馏水洗净后,马上注入0.01mol/LNa2S2O3溶液,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+2Na2S4O6.试回答下列问题:
(1)步骤①加入的指示剂是____________。
(2)判断达到滴定终点的实验现象是____________。
(3)假设未描述的事项都规范合理,则该测定结果将_______(填“偏高”、“偏低”或“无影响”)。
(4)碳酸H2CO3,K1=4.3×10-7,K2=5.6×10-11,草酸H2C2O4,K1=5.9X10-2,K2=6.4×10-5。0.1mol/LNa2CO3溶液的pH____0.1mol/L Na2C2O4溶液的pH。(选填“大于”、“小于”或“等于”)。若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是________。(选填编号)
A. c(H+)>c(HC2O4-)>c(HCO3-)>c(CO32-) B. c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
C. c(H+)>c(HC2O4-)>c(C2O42-)>c(CO32-) D. c(H2CO3)>c(HCO3-)>c(HC2O4-)>c(CO32-)
(5) 已知: ①难溶电解质的溶度积常数: Ksp(CaF2)=1.5×10-10②25℃时,2.0×10-3mol/L氢氟酸水溶液中,调节溶液pH (忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示,请根据以下信息回答下列问题:

①25℃时,HF电离平衡常数的数值Ka≈________。
②4.0×10-3mo1/LHF溶液与4.0×10-4mo1/L CaCl2液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),请通过列式计算说明是否有沉淀产生:_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com