
科目: 来源: 题型:
【题目】下列关于胶体和溶液的说法中,正确的是( )
A.溶液呈电中性,而胶体可以带电荷
B.胶体不均一、不稳定,静置后易产生沉淀;溶液均一、稳定,静置后不产生沉淀
C.某纳米材料微粒直径为30nm,因此该纳米材料属于胶体
D.往Fe(OH)3胶体中逐滴加入稀硫酸会产生先沉淀而后沉淀逐渐溶解
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上可通过煤的液化合成甲醇,主反应为:
CO(g)+2H2(g)![]() CH3OH(l) △H=x。
CH3OH(l) △H=x。
(1)已知常温下CH3OH、H2和CO 的燃烧热分别为726.5 kJ/mol、285.5 kJ/mol、283.0 k J/mol,则x=____;为提高合成甲醇反应的选择性,关键因素是__________________________。
(2)TK下,在容积为1.00 L的某密闭容器中进行上述反应,相关数据如图一。
①该化学反应0~10 min的平均速率v(H2)=_______;M和N点的逆反应速率较大的是_____(填“v逆(M)”、“v逆(N)”或“不能确定”)。
②10 min时容器内CO的体积分数为______。

③对于气相反应,常用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)表示平衡常数(以KP表示),其中,pB=p总×B的体积分数;若在TK 下平衡气体总压强为x atm,则该反应KP=____(计算表达式)。实验测得不同温度下的lnK(化学平衡常数K 的自然对数)如图二,请分析1nK 随T呈现上述变化趋势的原因是________________。
(3)干燥的甲醇可用于制造燃料电池。
①研究人员发现利用NaOH 干燥甲醇时,温度控制不当会有甲酸盐和H2生成,其反应方程式为______________________________;
②某高校提出用CH3OH-O2燃料电池作电源电解处理水泥厂产生的CO2(以熔融碳酸盐为介质),产物为C 和O2。其阳极电极反应式为___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】1 mol过氧化钠与2 mol碳酸氢钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,残留的固体物质是( )
A. Na2CO3 B. Na2O2、Na2CO3
C. NaOH、Na2CO3 D. Na2O2、NaOH、Na2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学反应速率的说法中,正确的是
A. 2mol/L盐酸与锌反应时,加入4mol/L的氯化钠溶液,生成氢气的速率加快
B. 对于可逆反应2CO+2NO![]() N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快
N2+2CO2,使用合适的催化剂,CO的生成速率和消耗速率都加快
C. 工业上合成氨是放热反应,升高温度,正反应速率减慢
D. 在K2SO4和BaCl2两溶液反应时,增大压强,生成沉淀速率加快
查看答案和解析>>
科目: 来源: 题型:
【题目】用一定量的铁与足量的稀硫酸及足量的CuO制单质铜,有人设计了以下两种方案:
①Fe![]() H2
H2![]() Cu ②CuO
Cu ②CuO![]() CuSO4
CuSO4![]() Cu
Cu
若按实验原则进行操作,则两者制得单质铜的量为
A. 一样多 B. ①多 C. ②多 D. 无法判断
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年8月,联合国开发计划署在中国的首个“氢经济示范城市”在江苏如皋落户。用吸附了H2的碳纳米管等材料制作的二次电池的原理如图所示。下列说法正确的是( )
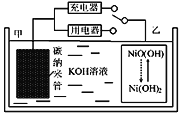
A. 放电时,甲电极反应为:NiO(OH)+H2O+e=Ni(OH)2+OH
B. 放电时,甲电极为正极,OH移向乙电极
C. 电池总反应为H2+2NiO(OH) ![]() 2Ni(OH)2
2Ni(OH)2
D. 充电时,电池的碳电极与直流电源的正极相连
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,CO2(g)+3H2(g)![]() H2O(g)+CH3OH(g) △H=-53.7kJ/mol;向2L 恒容恒温密闭容器中充入1mol CO2和2.8molH2反应,图中过程I、Ⅱ是在两种不同催化剂作用下建立平衡的过程中CO2的转化率[α(CO2)]随时间(t)的变化曲线。下列说法不正确的是
H2O(g)+CH3OH(g) △H=-53.7kJ/mol;向2L 恒容恒温密闭容器中充入1mol CO2和2.8molH2反应,图中过程I、Ⅱ是在两种不同催化剂作用下建立平衡的过程中CO2的转化率[α(CO2)]随时间(t)的变化曲线。下列说法不正确的是
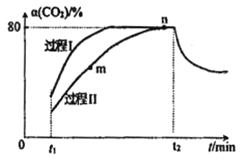
A. m点:v(正)>v(逆)
B. 活化能:过程Ⅱ>过程I
C. n点时该反应的平衡常数K=50
D. 过程I,t2时刻改变的反应条件可能是升高温度
查看答案和解析>>
科目: 来源: 题型:
【题目】高铁酸盐在水溶液中有四种含铁型体,25℃时,它们的物质的量分数随pH的变化如图所示。下列叙述错误的是
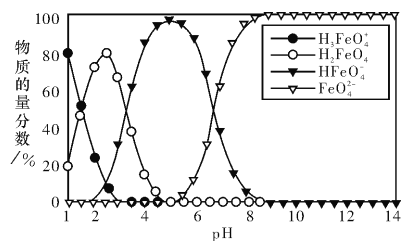
A. 已知H3FeO4+的电离半衡常数分别为:K1=2.5×10-2,K2=4.8×10-4,K3=5.0×10-8,当pII=4吋,溶液中![]()
B. 为获得尽可能纯净的高铁酸盐,应控制pH≥9
C. 向pH=5的高铁酸盐溶液中加入KOH溶液,发生反应的离子方程式为HFeO4ˉ+OHˉ=FeO42-+H2O
D. pH=2时,溶液中主要含铁型体浓度的大小关系为c(H2FeO4)>c(H3FeO4+)> c (HFeO4ˉ)
查看答案和解析>>
科目: 来源: 题型:
【题目】根据要求结合化学用语解释下列问题:
(1)NaHCO3溶液呈碱性的原因:__________________
(2)可用CuO除去CuCl2溶液中的FeCl3溶液的原因:_________________
(3)水垢中含有CaSO4,可先用Na2CO3溶液处理,使之转化为疏松、易溶于酸的CaCO3,而后用酸除去,请分析转化原理:_________________
(4)将密封的NO2气体加热,气体颜色变深的原因:______________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com