(2012?丹东模拟)二甲醚(CH
3OCH
3)被称为21世纪的新型燃料,在未来可能替代汽油、液化气、煤气等并具有优良的环保性能.工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H
2(g)═CH
3OH(g)△H
1=-90.7kJ?mol
-1②2CH
3OH(g)═CH
3OCH
3(g)+H
2O(g)△H
2=-23.5kJ?mol
-1③CO(g)+H
2O(g)═CO
2(g)+H
2(g)△H
3=-41.2kJ?mol
-1(1)若要增大反应①中H
2的转化率,在其它条件不变的情况下可以采取的措施为
B C
B C
.
A.加入某物质作催化剂
B.加入一定量CO
C.反应温度降低
D.增大容器体积
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1mol/L,c(H
2)=2.4mol/L,5min后达到平衡,CO的转化率为50%,则5min内CO的平均反应速率为
0.1mol/(L?min)
0.1mol/(L?min)
;若反应物的起始浓度分别为:c(CO)=4mol/L,c(H
2)=a mol/L;达到平衡后,c(CH
3OH)=2mol/L,a=
5.4
5.4
mol/L.
(3)催化反应室中总反应3CO(g)+3H
2(g)═CH
3OCH
3(g)+CO
2(g)的△H=
-246.1 kJ?mol-1
-246.1 kJ?mol-1
;830℃时反应③的K=1.0,则在催化反应室中反应③的K
>
>
1.0(填“>”、“<”或“=”).
(4)二甲醚的燃烧热为1455kJ?mol
-1,则二甲醚燃烧的热化学方程式为
CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1455 kJ?mol-1
CH3OCH3(g)+3O2(g)=2CO2(g)+3H2O(l)△H=-1455 kJ?mol-1
.
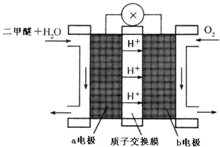
(5)“二甲醚燃料电池”是一种绿色电源,其工作原理如图所示.写出a电极上发生的电极反应式
CH3OCH3+3H2O-12e-=2CO2+12H+
CH3OCH3+3H2O-12e-=2CO2+12H+
.

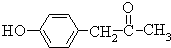 ,X可能发生的反应有
,X可能发生的反应有