
科目: 来源: 题型:
【题目】向1.0 mol·L-1的甲溶液中逐滴加入1.0 mol·L-1的乙溶液至过量,产生氢氧化铝沉淀的质量与加入的乙溶液的体积关系如图所示。
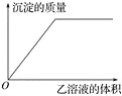
符合图中关系的是下列各组溶液中的( )
A. 甲为氯化铝,乙为氢氧化钠 B. 甲为氢氧化钠,乙为氯化铝
C. 甲为偏铝酸钠,乙为盐酸 D. 甲为氯化铝,乙为氨水
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室里需要纯净的氯化钠晶体,但现在只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
请回答下列问题:
(1)操作①加热的目的是________________,
(2)操作②除用BaCl2溶液外,还可用____________替代。
(3)操作②,判断SO42-已除尽的方法是________________________。
(4)操作③的目的是____________,不先过滤后再加Na2CO3溶液的理由是____________。
(5)操作④的名称是______________,应在________(填仪器名称)中进行。
查看答案和解析>>
科目: 来源: 题型:
【题目】除去下列括号内的杂质,所加试剂和操作均正确的是
选项 | 需除杂的物质 | 试剂 | 操作 |
A | Cl2(HCl) | 饱和食盐水 | 洗气 |
B | NaBr溶液(NaI) | Cl2 | 洗气 |
C | Cl2(H2O) | 碱石灰(CaO和NaOH) | 洗气 |
D | 铁粉(铝粉) | 稀硫酸 | 过滤 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各项括号内为杂质,后面为除杂质操作,其中正确的是( )
A.乙酸乙酯(乙酸),加NaOH溶液、分液
B.福尔马林(乙酸),加Na2CO3溶液、分液
C.溴乙烷(乙醇),加水振荡、分液
D.苯(苯酚),加溴水振荡、过滤
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)0.5 mol Na2CO3中含有___________个Na+。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体,在相同温度和相同压强条件下,体积最大的是____________。
(3)配制90 mL 0.1 mol/L CuSO4溶液,需要胆矾________g。
(4)氧化还原反应3S+6KOH=2K2S+K2SO3+3H2O中,氧化剂与还原剂的物质的量之比为_____________,若反应中消耗了0.6molS,则反应中转移的电子为________mol。
(5)现有下列10种物质:①H2O、②Mg、③CH3COOH、④NaOH、⑤CuSO4·5H2O、⑥碘酒、⑦C2H5OH、⑧盐酸,(将序号填在相应的空格内)其中,属于强电解质的是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:乙二酸晶体熔点101.5℃;乙二酸晶体加热分解的方程式为:H2C2O42H2O![]() 3H2O + CO2↑+ CO↑。现利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。请回答下列问题:
3H2O + CO2↑+ CO↑。现利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。请回答下列问题:

(1)检验装置A气密性的方法是________________________________________________
(2)A装置是否有误_____________(填“是”或“否”),原因为_______________________
(3)按气流方向连接各仪器,用数字表示接口的连接顺序:①→_________________________;
(4)该套装置有明显缺陷,请予以更正________________________________________________
(5)证明CO存在的实验现象是_________________________________________________;
(6)根据题给的数据,假设反应产生的气体全部排出,并与吸收液充分反应(提示:B、C中澄清石灰水均先变浑浊,后又变澄清),最终D中生成了两种物质,则这两种生成物的化学式及对应的物质的量分别是①_______________,②_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】冰晶石(Na3AlF6)微溶于水,工业上用萤石(CaF2含量为96%)、二氧化硅为原料,采用氟硅酸钠法制备冰晶石,其工艺流程如下:
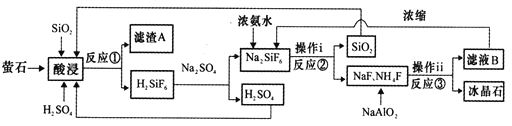
(1)Na3AlF6中氟、铝以共价键结合,写出Na3AlF6中所含阳离子的电子式________________,滤渣A的主要成分是_______________________(填名称)。
(2)为探究适合“酸浸”的条件,取4份相同样品进行实验,所得结果如下表所示:
实验编号 | 萤石品位 | 硫酸的 | 反应温度/℃ | 获得 Na2SiF6的质量 |
(CaF2含量) | 质量分数 | |||
1 | 96% | 25% | 60~70 | 120 |
2 | 96% | 35% | 60~70 | 153 |
3 | 96% | 35% | 80~90 | 100 |
4 | 96% | 40% | 60~70 | 141 |
①实验3比实验2获得Na2SiF6的质量低的原因可能是___________________。
②选择“酸浸”时所采用的最适合条件为____________________________。
(3)写出反应③的离子方程式:______________________________。
(4)“操作ⅰ”不能用硅酸盐质设备进行分离的原因__________________________。
(5)经测定,操作ⅰ所得滤液中所含杂质中K+浓度为0.05mol·L-1,当Na+浓度降为0.01mol·L-1时,若不考虑其它离子影响和溶液体积变化,K+___________(填“是”或“否”)开始沉淀。(已知25℃时,Ksp(Na3AlF6)=4.0×10-10,Ksp(K3AlF6)=6.0·10-8)
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)① ![]() 的名称是(用系统命名法命名)_____________,生成顺式聚合物的结构简式是_______________________。
的名称是(用系统命名法命名)_____________,生成顺式聚合物的结构简式是_______________________。
②聚合物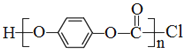 的单体是__________________。
的单体是__________________。
(2)①写出![]() 与足量溴水反应的化学方程式__________。
与足量溴水反应的化学方程式__________。
②写出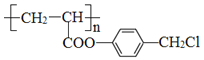 与足量NaOH溶液反应的化学方程式________。
与足量NaOH溶液反应的化学方程式________。
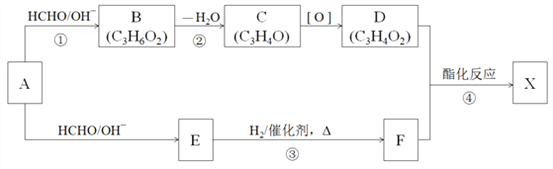
(3)有机物X是重要的工业原料,由A为原料合成X路线如下(部分反应条件略):
已知:a. 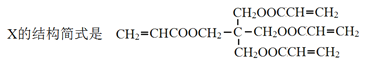
b. ![]()
① B的结构简式是_____________________________。
② A→E的化学方程式是_________________________________________。
③ D和F反应生成X的化学方程式是_____________________________。
(4)写出以甲苯为主要原料合成![]() 的流程(无机试剂、某些有机原料任选)。
的流程(无机试剂、某些有机原料任选)。
已知:a. ![]() ;b. 羧基活化苯环的间位,____________
;b. 羧基活化苯环的间位,____________
查看答案和解析>>
科目: 来源: 题型:
【题目】某无色溶液中滴入酚酞试液显红色,该溶液中可以大量共存的离子组是
A.Mg2+、Al3+、HCO3-、SO32- B.K+、Ca2+、MnO4-、Cl-
C.Ba2+、Na+、AlO2-、NO3- D.NH4+、Fe3+、SO42-、SCN-
查看答案和解析>>
科目: 来源: 题型:
【题目】汽车尾气处理装置中可发生反应:4CO+2NO2 ![]() 4CO2+N2,下列对该反应的说法正确的是
4CO2+N2,下列对该反应的说法正确的是
A. NO2被氧化 B. CO是氧化剂
C. 该条件下,氧化性CO2<NO2 D. 该条件下,还原性CO<N2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com