
科目: 来源: 题型:
【题目】实验室常见的仪器如下图所示,请回答下列问题:
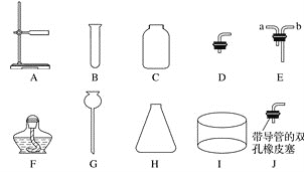
(1)仪器Ⅰ的名称为__________;仪器G的名称为__________。
(2)若将B、D、F组合成气体发生装置,则该制气原理的反应条件一定是__________________。
(3)若将C、G、H、I、J(导管略)组合成一套制取并收集气体的装置,则该装置收集得到的常见气体可能是____________。
(4)若将C、E装置组合用于向上排空气法收集气体,则气体从________(填“a”或“b”)导管口进入。
查看答案和解析>>
科目: 来源: 题型:
【题目】钛由于其稳定的化学性质,良好的耐高温、耐低温、抗强酸、抗强碱以及高强度、低密度,被美誉为“未来钢铁”、“战略金属”。
(1)基态钛原子核外共有_____种运动状态不相同的电子,价电子排布式____________________;与钛同周期的元素中,基态原子的未成对电子数与钛相同的有__种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是___________________。
(3) TiCl4是氧化法制取钛的中间产物。TiCl4分子结构与CCl4相同,在常温下都是液体。TiCl4分子的空间构型是_______________,Ti原子采取____杂化方式;TiCl4稳定性比CCl4差,极易水解,试从结构分析其原因:_______________________________。
(4)钙钛矿材料是一类有着与钛酸钙(CaTiO3)相同晶体结构的材料,这种奇特的晶体结构让它具备了很多独特的理化性质,比如吸光性、电催化性等。CaTiO3晶体结构如图所示。其中,A代表__________(写离子符号),它的配位数是___________。

查看答案和解析>>
科目: 来源: 题型:
【题目】C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1) CO2的重整用CO2和H2为原料可得到CH4燃料。
已知: ①CH4 (g)+CO2(g)=2CO(g)+2H2(g) △H1=+247k/mol
②CH4 (g)+H2O(g)=CO(g)+3H2(g) △H2=+205k/mol
写出CO2重整的热化学方程式:___________________________。
(2)“亚碳酸盐法”吸收烟中的SO2
①将烟气通入1.0mol/L 的Na2SO3溶液,若此过程中溶液体积不变,则溶液的pH不断___(填“减小”“不变”或“增大)。当溶液pH约为6时,吸收SO2的能力显著下降,应更换吸收剂,此时溶液中c(SO32-) =0.2 mol/L,则溶液中c(HSO3-) =_______。
②室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与各组分物质的量分数的变化关系如图:
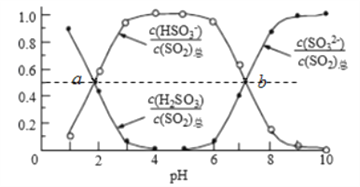
b点时溶液pH=7,则n(NH4+):n(HSO3-)=__________。
(3)催化氧化法去除NO。一定条件下,用NH3消除NO污染,其反应原理; 4NH3+6NO![]() 5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如下图所示:
5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如下图所示:
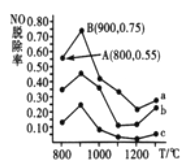
①曲线a中,NO的起始浓度为6×10-4mg·m-3,从A点到B点经过0.8s,该时间段内NO的脱除速率为___________mg·m-3·s-1。
②曲线b对应NH3与NO的物质的量之比是____________________。
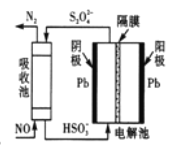
(4)间接电化学法除NO。其原理如图所示:写出阴极的电极反应式(阴极室溶液呈酸性)______。吸收池中除去NO的原理_____________ (用离子方程式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于硅酸盐工业的叙述正确的是
A. 普通玻璃的主要成分可以表示为Na2O·CaO·6SiO2,说明玻璃为纯净物
B. 陶瓷、玻璃、水泥都属于硅酸盐产品
C. 制玻璃、水泥时都用到了石灰石和黏土
D. 制玻璃的过程中发生了反应:Na2CO3+SiO2![]() Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3
Na2SiO3+CO2↑,说明酸性:H2SiO3>H2CO3
查看答案和解析>>
科目: 来源: 题型:
【题目】石墨烯锂硫电池是一种高容量、长循环寿命、低成本及环境友好的新型二次电池,其工作原理如图所示,电池反应为2Li+nS![]() Li2Sn。下列说法错误的是
Li2Sn。下列说法错误的是

A. 放电时,Li+向正极移动
B. 充电时,A电极连接直流电源的正极
C. 充电时,每生成nmolS,外电路中流过2nmol电子
D. 放电时,正极上可发生反应2Li++Li2S4+2e-=2Li2S2
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定质量的锌、铝混合物与足量的稀硫酸反应,生成2.8 L(标况)氢气,原混合物的质量可能是( )
A. 2 g B. 1 g C. 8 g D. 10 g
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用含三价钒(V2O3)为主的某石煤为原料(含有Al2O3、CaO等杂质),钙化法焙烧制备V2O5,其流程如下:
![]()
【资料】:+5价钒在溶液中的主要存在形式与溶液pH的关系:
pH | 4~6 | 6~8 | 8~10 | 10~12 |
主要离子 | VO2+ | VO3 | V2O74 | VO43 |
(1)焙烧:向石煤中加生石灰焙烧,将V2O3转化为Ca(VO3)2的化学方程式是______。
(2)酸浸: ① Ca(VO3)2难溶于水,可溶于盐酸。若焙砂酸浸时溶液的pH=4,Ca(VO3)2溶于盐酸的离子方程式是______。
② 酸度对钒和铝的溶解量的影响如图所示:酸浸时溶液的酸度控制在大约3.2%,根据如图推测,酸浸时不选择更高酸度的原因是______。

(3)转沉:将浸出液中的钒转化为NH4VO3固体,其流程如下:
![]()
① 浸出液中加入石灰乳的作用是______。
② 已知CaCO3的溶解度小于Ca3(VO4)2。向Ca3(VO4)2沉淀中加入(NH4)2CO3溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:______。
③ 向(NH4)3VO4溶液中加入NH4Cl溶液,控制溶液的pH=7.5。当pH>8时,NH4VO3的产量明显降低,原因是______。
(4)测定产品中V2O5的纯度:
称取a g产品,先用硫酸溶解,得到(VO2)2SO4溶液。再加入b1 mL c1 mol·L1 (NH4)2Fe(SO4)2溶液(VO2+ + 2H+ + Fe2+ == VO2+ + Fe3+ + H2O)。最后用c2 mol·L1 KMnO4溶液滴定过量的(NH4)2Fe(SO4)2至终点,消耗KMnO4溶液的体积为b2 mL。已知 MnO4被还原为Mn2+,假设杂质不参与反应。则产品中V2O5的质量分数是______。(V2O5的摩尔质量:182 g·mol1)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:H2(g)+I2(g)![]() 2HI(g)△H=-14.9kJ·mol-1。某温度下,在体积均为2.0L的甲、乙两个恒容密闭容器中充入反应物,其起始物质的量如下表所示。甲中反应达到平衡时,测得c(H2)=0.008mol·L-1。下列判断正确的是( )
2HI(g)△H=-14.9kJ·mol-1。某温度下,在体积均为2.0L的甲、乙两个恒容密闭容器中充入反应物,其起始物质的量如下表所示。甲中反应达到平衡时,测得c(H2)=0.008mol·L-1。下列判断正确的是( )
起始物质的量 | n(H2)/mol | n(I2)/mol | n(HI)/mol |
甲 | 0.02 | 0.02 | 0 |
乙 | 0.04 | 0.04 | 0 |
A. 平衡时,乙中H2的转化率是甲中的2倍
B. 平衡时,甲中混合物的颜色比乙中深
C. 平衡时,甲、乙中热量的变化值相等
D. 该温度下,反应的平衡常数K=0.25
查看答案和解析>>
科目: 来源: 题型:
【题目】在常温下,用0.1000mol/L的盐酸滴定25mL0.100mol/Lna2CO3溶液,所得滴定曲线如下图所示。下列相关微粒浓度间的关系不正确的是

A. a点:c(CO32-)>c(Cl-)>c(HCO3-)
B. b点:c(Na+)+c(H+)= c(Cl-)+ c(HCO3-)+2c(CO32-)+c(OH-)
C. c点:c(OH-)+ c(CO32-)= c(H+)+c(H2CO3)
D. d点:c(Cl-)= c(Na+)
查看答案和解析>>
科目: 来源: 题型:
【题目】我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应H2S+O2=H2O2+S,已知甲池中发生的反应为
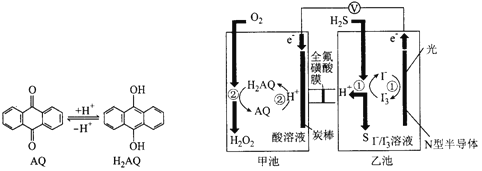
下列说法正确的是( )
A. 该装置中电能转化为光能
B. H+从甲池移向乙池
C. 甲池中碳棒上发生的电极反应为AQ+2H+-2e-=H2AQ
D. 乙池溶液屮发生的反应为H2S+I3-=3I-+S+2H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com