
科目: 来源: 题型:
【题目】有机物X的结构简式如下图所示。下列关于有机物X的说法正确的是

A. X化学式为C8H6O6
B. X可发生加成反应、水解反应和氧化反应
C. X分子中所有的原子一定在同一平面内
D. X能使溴水和KMnO4溶液褪色,原因均与分子中碳碳双键有关
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物I (分子式为C13H18O2)是一种香料,如图是该香料的一种合成路线。
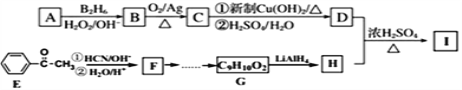
已知:①![]() ;
;![]()
②有机物D的摩尔质量为88 g·mol-1,其核磁共振氢谱有3组峰;有机物H是苯甲醇的同系物,苯环上只有一个侧链。回答下列问题:
(1)用系统命名法命名有机物A___________________;
(2)B的结构简式为_____________________________________;
(3)F→G经历两步反应,反应类型依次为____________,_____________。
(4)C→D第①步反应的化学方程式为_________________________________。
(5)F在一定条件下能形成一种聚酯类化合物,写出该反应的化学方程式___________________________________________________________。
(6)己知有机物甲符合下列条件:①为芳香族化合物;②与H互为同分异构体;③能被催化氧化成醛。符合上述条件的有机物甲有_______种, 写出一种满足苯环上有3个侧链,且核磁共振氢谱有5组峰,峰面积比为6:2:2:1:1的有机物的结构简式_______;
(7)参照上述合成路线以丙酮等为原料合成D (无机试剂任选)______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,向[H+]=1×10-6 mol·L-1的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液中[H+]=1×10-3mol·L-1。下列对该溶液的叙述不正确的是( )
A. 该温度高于25 ℃
B. 所得溶液中,由水电离出来的H+的浓度为1×10-11mol·L-1
C. 加入NaHSO4晶体抑制水的电离
D. 该温度下,此NaHSO4溶液与某pH=11的Ba(OH)2溶液混合后溶液呈中性,则消耗的NaHSO4溶液与Ba(OH)2溶液的体积比为100:1
查看答案和解析>>
科目: 来源: 题型:
【题目】太阳能电池板材料除单晶硅外,还有铜、铟、镓、硒等化学物质。
(1)基态铜原子的电子排布式为_____________;已知高温下CuO![]() Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是___________________________。
Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是___________________________。
(2)硒、硅均能与氢元素形成气态氢化物,则它们形成的最简单的氢化物中,分子构型分别为____________, 若“Si-H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se____Si (填“>”、“<”)。人们把硅与氢元素形成的一类化合物叫硅烷。硅烷的组成、结构与相应的烷烃相似,硅烷的沸点与相对分子质量的关系如图所示,呈现这种变化的原因是_____________________________________________。

(3)与铟、镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤电子对的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3。BF3·NH3中B原子的杂化轨道类型为______, B与N之间形成___________键。
(4)金刚砂(SiC)的硬度为9.5,其晶胞结构如下图所示,则金刚砂晶体类型为_________________,在SiC中,每个C原子周围最近的C原子数目为___个;若晶胞的边长为a pm,则金刚砂的密度为____g/cm3 (用NA表示阿伏伽德罗常数的值)。

查看答案和解析>>
科目: 来源: 题型:
【题目】醋酸溶液中存在电离平衡CH3COOH![]() H++CH3COO-,下列叙述正确的是( )
H++CH3COO-,下列叙述正确的是( )
A. 升高温度,平衡正向移动,醋酸的电离常数Ka值增大
B. 0.10mol/L的CH3COOH溶液中加水稀释,溶液中所有离子的浓度都减小
C. 向溶液中加少量的CH3COONa固体,平衡逆向移动,c(CH3COO-)的浓度减小
D. 25℃时,加入少量浓醋酸,平衡正向移动,醋酸的电离程度增大
查看答案和解析>>
科目: 来源: 题型:
【题目】李克强总理在《2018年国务院政府工作报告》中强调“今年二氧化硫、氮氧化物排放量要下降3%。”因此,研究烟气的脱硝(除NOx)、脱硫(除SO2)技术有着积极的环保意义。
(1)汽车的排气管上安装“催化转化器”,其反应的热化学方程式为:2NO(g)+2CO(g)![]() 2CO2(g)+N2(g) ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min) NO的物质的量随时间变化如图。
2CO2(g)+N2(g) ΔH=-746.50kJ·mol-1。T℃时,将等物质的量的NO和CO充入容积为2L的密闭容器中,若温度和体积不变,反应过程中(0~15min) NO的物质的量随时间变化如图。

①图中a、b分别表示在相同温度下,使用质量相同但表面积不同的催化剂时,达到平衡过程中n (NO)的变化曲线,其中表示催化剂表面积较大的曲线是___________。(填“a”或“b”)
②T℃时,该反应的化学平衡常数K=_______________;平衡时若保持温度不变,再向容器中充入CO、CO2各0.2 mol,则平衡将_________移动。(填“向左”、“向右”或“不”)
③15min时,若改变外界反应条件,导致n (NO)发生图中所示变化,则改变的条件可能是_______________________________________________ (任答一条即可)。
(2)在催化剂作用下,用还原剂[如肼(N2H4)]选择性地与NOx反应生成N2和H2O。
已知200℃时:Ⅰ.3N2H4(g)=N2(g)+4NH3(g) ΔH1=-32.9 kJ·mol-1;
II. N2H4(g)+H2(g) =2NH3(g) ΔH2=-41.8 kJ·mol-1。
①写出肼的电子式:____________________。
②200℃时,肼分解成氮气和氢气的热化学方程式为:_____________________________。
③目前,科学家正在研究一种以乙烯作为还原剂的脱硝原理,其脱硝率与温度、负载率(分子筛中催化剂的质量分数)的关系如下图所示。

为达到最佳脱硝效果,应采取的条件是_________________________________________。
(3)利用电解装置也可进行烟气处理,如图可将雾霾中的NO、SO2分别转化为NH4+和SO42-,阳极的电极反应式为____________________________;物质A是______________ (填化学式)。

查看答案和解析>>
科目: 来源: 题型:
【题目】一种用软锰矿(主要成分MnO2)和黄铁矿(主要成分FeS2) 制取MnSO4·H2O并回收单质硫的工艺流程如下:
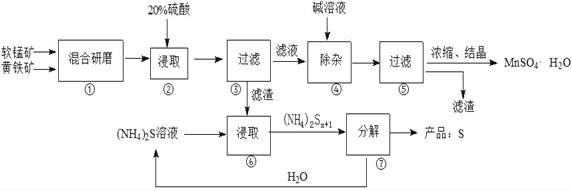
已知:本实验条件下,高锰酸钾溶液与硫酸锰溶液混合产生二氧化锰。
回答下列问题:
(1)步骤①混合研磨成细粉的主要目的是_____________________________________________;步骤②浸取时若生成S、MnSO4及Fe2(SO4)3的化学方程式为_____________________________________。
(2)步骤③所得酸性滤液可能含有Fe2+,为了除去Fe2+可先加入______________________;步骤④需将溶液加热至沸然后在不断搅拌下加入碱调节pH为4~5,再继续煮沸一段时间,“继续煮沸”的目的是_____________________________________。步骤⑤所得滤渣为__________________(填化学式)。
(3)步骤⑦需在90~100℃下进行,该反应的化学方程式为_________________________________。
(4)测定产品MnSO4·H2O的方法之一是:准确称取a g产品于锥形瓶中,加入适量ZnO及H2O煮沸,然后用c mol·L-1KMnO4标准溶液滴定至浅红色且半分钟不褪色,消耗标准溶液VmL,产品中Mn2+的质量分数为w(Mn2+)=________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】恒温恒容, 4A(s)+3B(g)![]() 2C(g)+D(g)经2min,B的浓度减少0.6mol·L-1,下列说法正确的是
2C(g)+D(g)经2min,B的浓度减少0.6mol·L-1,下列说法正确的是
A. 用A表示的反应速率是0.4mol·L-1·min-1
B. 分别用B、C表示反应的速率,其关系是:3υ(B)=2υ(C)
C. 2min末的反应速率υ(B)=0.3mol·L-1·min-1
D. 气体的密度不再变化,则证明反应已经达到平衡状态
查看答案和解析>>
科目: 来源: 题型:
【题目】为测定某地空气中SO2和可吸入颗粒的含量,某同学设计了如下图所示的实验装置:

注:气体流速管是用来测量单位时间内通过气体体积的装置
(1)上述实验测定原理为_________________________________ (用化学方程式表示)。
(2)应用上述装置测定空气中SO2和可吸入颗粒的含量,除需测定气体流速(单位:mL·s-1)外,还需要测定碘溶液蓝色褪去所需的时间和___________________________。
(3)己知:碘单质微溶于水,KI可以增大碘在水中溶解度。为精确配制100 mL 5.0×10-4mol·L-1的碘溶液,先要配制1000 mL 1.0×10-2mol·L-1碘溶液,再取5.00 mL溶液稀释成为5.0×10-4mol·L-1碘溶液。
①第一步:用托盘天平称取___ g 碘单质加入烧杯中,同时加入少量碘化钾固体,加适量水搅拌使之完全溶解。
②第二步:________________,洗涤、定容、摇匀。
③第三步:用第二步所得溶液配制5.0×10-4mol·L-1碘溶液,此步操作中,除烧杯、玻璃棒、胶头滴管外还需要的玻璃仪器有________________________。
(4)空气中SO2含量的测定:
①已知空气中二氧化硫的最大允许排放浓度不得超过0.02mg·L-1,在指定的地点取样,以200mL·s-1气体流速通过气体流速管通入到上图实验装置中,观察记录碘溶液褪色所需时间为500s,则该地空气中的SO2含量是________ mg·L-1,____________(填“符合”、“不符合”)排放标准。
②如果甲同学用该方法测量空气中SO2的含量时,所测得的数值比实际含量低,其原因可能是________________________________(假设溶液配制、称量或量取及各种读数均无错误。写出一种可能原因即可)
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、W、Q 四种元素在元素周期表中的位置如下,下列叙述错误的是
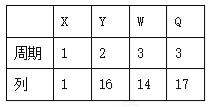
A. Y 的氢化物沸点高于 Q 的氢化物沸点
B. 最高正价与最低负价之和为 0 的元素只有 W
C. 原子半径顺序为:r(W) > r(Q) > r(Y) > r(X)
D. X、Y、Q 三元素形成的分子中,原子最外层电子数之和最大为 32
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com