
科目: 来源: 题型:
【题目】某可充电电池的原理如图所示,已知a、b为惰性电极,溶液呈酸性。充电时右槽溶液颜色由绿色变为紫色。下列叙述正确的是

A. 放电时,H+从左槽迁移进右槽
B. 放电过程中,左槽溶液颜色由黄色变为蓝色
C. 充电时,b极接直流电源正极,a极接直流电源负极
D. 充电过程中,a极的电极反应式为:VO2++2H++e- = VO2++H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】我国化工专家侯德榜的“侯氏制碱法”曾为世界制碱工业做出了突出贡献。他利用NaHCO3、NaCl、NH4C1等物质溶解度的差异,以食盐、氨气、二氧化碳等为原料制得NaHCO3,进而生产出纯碱。以下A、B、 C、 D四个装置可组装成实验室模拟“侯氏制碱法”制取NaHCO3的实验装置。装置中分别盛有以下试剂:B:稀硫酸;C:盐酸、碳酸钙;D:含氨的饱和食盐水、水。

四种盐在不同温度下的溶解度(g/100 g水)表(说明:①>35 ℃ NH4HCO3会有分解)

请回答以下问题:
(1)装置的连接顺序应是__________(填字母)。
(2)A装置中盛放的试剂是__________,其作用是___________________。
(3)在实验过程中,需要控制D温度在30℃~35℃,原因是_________________。
(4)反应结束后,将锥形瓶浸在冷水中,析出NaHCO3晶体。用蒸馏水洗涤NaHCO3晶体的目的是除去____(杂质以化学式表示)。
(5)将锥形瓶中的产物过滤后,所得的母液中含有___________(以化学式表示),加入氯化氢,并进行_________操作,使NaCl溶液循环使用,同时可回收NH4Cl。
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转.

请回答下列问题:
(1)甲池为 (填“原电池”、“电解池”或“电镀池”),A电极的电极反应式为 .
(2)丙池中F电极为 (填“正极”、“负极”、“阴极”或“阳极”),该池的总反应方程式为 .
(3)当乙池中C极质量减轻10.8g时,甲池中B电极理论上消耗O2的体积为 mL(标准状况).
(4)一段时间后,断开电键K,下列物质能使乙池恢复到反应前浓度的是 (填选项字母).
A.Cu
B.CuO
C.Cu(OH)2
D.Cu2(OH)2CO3.
查看答案和解析>>
科目: 来源: 题型:
【题目】对氨基水杨酸钠(PAS-Na)是抑制结核杆茵最有效的药物。某同学设计的合成PAS-Na的两种路线如下:
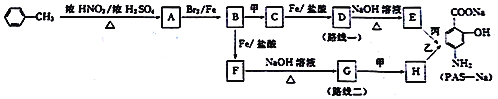
已知以下信息:
①甲、乙、丙为常用的无机试剂;
②![]()
③![]() (苯胺,易被氧化)。
(苯胺,易被氧化)。
回答下列问题:
(1)甲和丙的名称分别是_________________、____________________。
(2)E的结构简式是______________________。
(3)A→B的化学方程式是______________________________________,反应类型是______。
(4)A的同分异构体中氨基(一NH2)与苯环直接相连并且能发生银镜反应的有____种,其中核磁共振氢谱为4组峰且面积之比为2:2:2:1的结构简式为___________。
(5)有同学认为“路线二”不合理,不能制备PAS-Na,你的观点及理由是_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】硫酸铵可用作肥料,也可用于纺织、皮革、医药等方面。某化学兴趣小组对硫酸铵的一些性质进行探究。回答下列问题:
(1)在试管中加入少量硫酸铵样品,加水溶解,滴加NaOH溶液。将湿润的红色石蕊试纸放在试管口,试纸颜色无明显变化。再将试管加热,试纸很快变蓝。由此可知:______________________________________、_________________________________。
(2)从废铁屑中回收铁屑,用碱溶液洗净之后,再用过量硫酸溶解。然后加入稍过量硫酸铵饱和溶液。在小火下蒸发溶剂直到晶膜出现,停火利用余热蒸发溶剂。过滤后用少量乙醇洗涤,得到硫酸亚铁铵晶体。
①碱溶液洗涤的目的是__________________________________。
②硫酸过量的原因是___________________________________。
(3)硫酸铵高温下完全分解生成氨气和其他几种气体(含硫产物只有一种)。为探究硫酸铵的其他分解产物,通过下列装置进行实验,通入分解产物一段时间后,再点燃装置E中的酒精灯并开始用装置F收集气体。实验中观察到E中无明显现象,F中排水收集的气体能使燃着的木条熄灭,经测定其相对分子质量为28。

①装置A、B中的溶液分别是______(填标号)。B中可观察到的现象是_____________________。
a.NaOH溶液 b.硫酸溶液 c.BaCl2溶液 d.品红溶液
②装置E的作用是__________________________________。
③写出(NH4)2SO4高温分解的化学方程式:________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(化学-物质结构与性质)氮及其化合物广泛存在于自然界中,回答下列问题:
(1)在基态15N原子的p能级上存在_____个自旋方向相同的电子;CN—中σ键与π键数目之比为_____。
(2)碱性肥料氰氨化钙(CaCN2)的组成元素中第一电离能最小的是_______(填名称)。
(3)化合物(CH3)3N能溶于水,其原因是____________________________________,(CH3)3N与盐酸反应生成[(CH3)3NH]+,该过程新生成的化学键类型为_______________。
(4)阳离子[(CH3)3NH]+和阴离子A按个数比4:1组成化合物,阴离子A的结构如下图所示,则s原子的杂化轨道类型是__________,阴离子A的化学式为_______________。
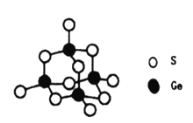
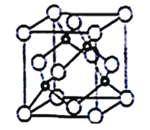
(5)立方氮化硼晶胞如下图所示(白球为氮原子,黑球为硼原子),则硼原子的配位数为___;若晶胞边长为acm,则立方氮化硼的密度是______g·cm-3(只要求列算式,阿伏加德罗常数用NA表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学课外小组所做实验的示意图如图所示:图中“→”表示气体流向, M是一种纯净而干燥的气体,Y为另一种气体,E内有红棕色气体产生,实验所用物质只能由下列物质中选取:Na2CO3、Na2O2、NaCl、Na2O、CaCl2、(NH4)2CO3、碱石灰等固体及蒸馏水。据此实验,完成下列填空:

(1)A中所用装置的主要仪器和药品是______________________。
(2)B中所选的干燥剂是________,其作用是______________________________。
(3)C中发生的主要反应的化学方程式:________________________________。
(4)制取Y气体的D装置所用的主要仪器是__________________________。
制取Y气体的化学方程式是________________________。
(5)F中发生反应的化学方程式为__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】可逆反应N2+3H2![]() 2NH3是工业上合成氨的重要反应。
2NH3是工业上合成氨的重要反应。
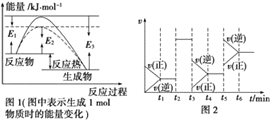
(1)根据图1请写出合成氨的热化学方程式__________________(热量用El、E2或E3表示)。
(2)图1中虚线部分是通过改变化学反应中的_________条件,该条件的改变与图2中哪一时刻条件的改变相同_________(用“t1……t6”表示)。
(3)图2中t3时刻改变的条件是_________,t5与时刻改变的条件是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】为有效提升空气质量,国家强制各燃煤企业要对燃煤烟气进行脱硫、脱硝处理后排放。回答下列问题:
(1)燃煤烟气“脱硝”中涉及到的部分反应如下:
a.4NH3(g)+6NO(g) ![]() 5N2(g)+6H2O(g) △H 1
5N2(g)+6H2O(g) △H 1
b.4NH3(g)+5O2(g) ![]() 4NO(g)+6 H2O(g)△H2 =-925kJ·mol-1
4NO(g)+6 H2O(g)△H2 =-925kJ·mol-1
c.N2(g)+O2(g) ![]() 2NO(g)△H 3=+175kJ·mol-1
2NO(g)△H 3=+175kJ·mol-1
则△H 1=_____kJ/mol。
(2)向某恒容密闭容器中加入2molNH3、3molNO,在适当条件下发生(1)中反应a,反应过程中NO的平衡转化率随温度T、压强p的变化曲线如图所示:
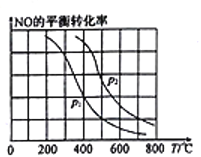
①p1________p2(填“>”“<”或“=”)。
②若在压强为加p2、温度为600℃时,达到平衡时反应体系内化学能降低了300kJ,则NO的转化率为_______________________。
③600℃时,下列各项数据中能表明该反应已达到化学平衡状态的是______。
a.水与NO的生成速率相等 b.混合气体的密度保持不变
c. NH3、NO生成速率比为5:4 d.容器的总压强保持不变
(3)将2molN2、3molH2O、0.5molNO的混合气体置于x、y、z三个容积相同的恒容密闭容器中,控制适当的条件发生反应,反应过程中c(NO)随时间的变化如图所示。
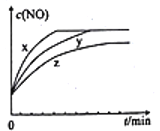
①在建立平衡的过程中,三个容器中反应速率的相对大小为______________。
②与y容器中反应相比,z容器中反应改变的条件及判断依据分别是_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铬铁矿主要成分为FeO、Cr2O3,含有SiO2、Al2O3等杂质。工业上用铬铁矿制备红矾钠晶体(Na2Cr2O7)的流程如图所示:

(1)步骤①的主要反应为FeO·Cr2O3+O2+NaOH![]() Na2CrO4+NaFeO2+H2O,该反应配平后FeO·Cr2O3与O2的系数比为___________。该步骤是在坩埚中进行煅烧,可用此坩埚材料的是______________(填标号)。
Na2CrO4+NaFeO2+H2O,该反应配平后FeO·Cr2O3与O2的系数比为___________。该步骤是在坩埚中进行煅烧,可用此坩埚材料的是______________(填标号)。
A.铁 B.氧化铝 C.石英 D.陶瓷
(2)步聚①煅烧反应极慢,需要升温至NaOH呈熔融状态,反应速率才加快,其原因是____________________________________________________。
(3)步骤②中NaFeO2会强烈水解生成氢氧化铁沉淀,反应的化学方程式为________________。
(4)将五份滤液1分别在130℃蒸发1小时,各自冷却到不同温度下结晶,保温过滤,所得实验数据如下表。根据数据分析,步骤③的最佳结晶温度为___________℃。
结晶温度/℃ | Na2CrO4粗晶中各物质含量/% | |||
Na2CrO4 4H2O | NaOH | NaAlO2 | Na2SiO3 | |
30 | 52.45 | 29.79 | 8.69 | 12.21 |
40 | 68.81 | 20. 49 | 8.46 | 10.84 |
50 | 60.26 | 27. 96 | 10.36 | 9.32 |
60 | 50.74 | 29.66 | 10.40 | 12.25 |
70 | 46.77 | 33.06 | 8.10 | 6.48 |
(5)步骤④中滤渣3的成分是_____________(写化学式)。
(6)若该流程中铬元素完全转化为红矾钠晶体,则该铬铁矿中铬元素的质量分数为____________(用含m1、m2的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com