
科目: 来源: 题型:
【题目】根据某有机物的结构:
(1)测定实验式:某含碳、氢、氧三种元素的有机物,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则其实验式是________。
(2)确定分子式:下图是该有机物的质谱图,则其相对分子质量为______,分子式为________。
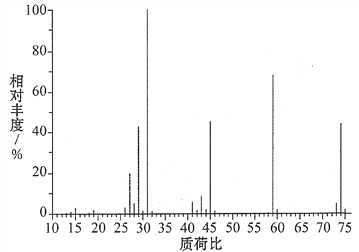
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A为淡黄色固体,T、R 为两种常见的用途广泛的金属单质,D具有磁性的黑色晶体,C是无色无味的气体,M为红褐色固体。回答相关问题
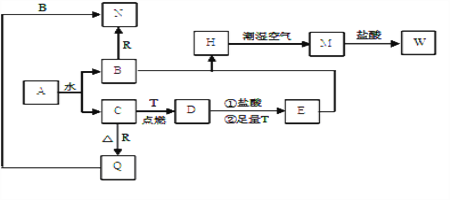
(1)写出D的化学式: ____________
(2)写出A的电子式: _____________
(3)H在潮湿空气中变为M的现象是:______________化学方程式为: ________________
(4)B与R反应的化学方程式为: __________________________
(5)向沸水中加入W饱和溶液,可制得一种红褐色透明液体,区别该液体和溶液W的简单实验方法是 ____________________
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)高铁酸钾![]() 是一种新型、高效、多功能水处理剂。某学习小组设计如下方案制备高铁酸钾:
是一种新型、高效、多功能水处理剂。某学习小组设计如下方案制备高铁酸钾:
![]()
①高铁酸钾中铁元素的化合价为________,据此推测它具有的化学性质是____________。
②其中第一步操作是:在NaClO溶液中加入烧碱固体形成强碱性环境,将研磨过的硝酸铁少量多次地加入上述溶液中,冰水浴中反应1 h。发生的离子反应为2Fe3++3ClO-+10OH-===2FeO![]() +3Cl-+5H2O,还原剂是_____________。
+3Cl-+5H2O,还原剂是_____________。
③高铁酸钾和水发生反应,生成物能吸附杂质净水,同时还产生气体,写出反应的离子方程式:___________________。
(2)某Fe 2(SO4) 3样品含有少量FeSO4杂质,为了测定该样品中铁元素的含量,设计如下实验:
Ⅰ.称取样品m g,加入稀H2SO4,后加水配制成250.00 mL溶液;
Ⅱ.取25.00 mL溶液,先加入![]() ,然后再加过量的氨水,过滤;
,然后再加过量的氨水,过滤;
Ⅲ.将沉淀用蒸馏水洗涤数次后,烘干;
Ⅳ.灼烧至质量不再减少为止,得到红棕色固体,冷却后称量,质量为n g。
请根据上面操作流程,回答以下问题:
①步骤Ⅰ中称量使用的仪器是________________,配制用到的仪器有烧杯、玻璃棒、胶头滴管,还要补充的玻璃仪器是____________________。
②步骤Ⅱ中过滤用的仪器有滤纸、铁架台、铁圈和烧杯,还要补充的玻璃仪器是_________;加入![]() 的主要目的是________________。
的主要目的是________________。
③步骤Ⅲ中检验该沉淀已经洗涤干净的操作是________________。
④若要检验溶液中的![]() ,则应该加入________________试剂。
,则应该加入________________试剂。
⑤计算该样品中铁元素的质量分数的表达式是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如下实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数。

(1)请将实验步骤补充完整
①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是 _____________________。
②称取样品,并将其放入硬质玻璃管中;并称量C、D装置的质量。
③打开活塞K1和K2,关闭K3,缓慢鼓入空气数分钟,其目的是____________________。
④关闭活塞K1和K2,打开K3,点燃酒精灯加热至不再产生气体。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后卸下装置,再次称量C、D装置的质量。
(2)关于该实验方案,请回答下列问题:
①若加热反应后不鼓入空气,对NaCl测定结果的影响是___________(“偏高”、“偏低”或“无影响”)
②E处干燥管中盛放的药品是_______________,其作用是_____________________________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量分数______________(“偏高”、“偏低”或“无影响”)
③若样品质量为wg,反应后C、D装置增加的质量分别为m1g和m2g,由此可知混合物中Na2CO3·10H2O的质量分数为______(用含w、m1、m2的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某有机物A的红外光谱和核磁共振氢谱如下图所示,下列说法中错误的是
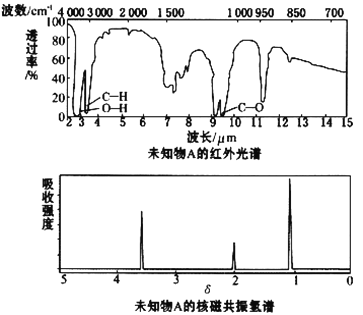
A. 由红外光谱可知,该有机物中至少含有三种不同的化学键
B. 由核磁共振氢谱可知,该有机物分子中有三种不同的氢原子且个数比为1:2:3
C. 仅由其核磁共振氢谱可知其分子中的氢原子总数
D. 若A的化学式为C2H6O,则其结构简式为CH3CH2OH
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学研究性学习小组对某无色水样的成分进行检验,已知该水样中只可能含有K+、Mg2+、Fe3+、Cu2+、Al3+、Ag+、Ca2+、CO32-、SO42-、Cl-中的若干种离子。该小组同学取100 mL水样进行实验,向水样中先滴加硝酸钡溶液,再滴加1 mol·L-1的硝酸,实验过程中沉淀质量的变化情况如图所示:

注明:Ob段表示滴加硝酸钡溶液;bd段表示滴加稀硝酸
(1)水样中一定含有的阴离子是________,其物质的量浓度之比为________。
(2)写出BC段所表示反应的离子方程式:__________________________________________。
(3)由B点到C点变化过程中消耗硝酸的体积为________。
(4)试根据实验结果推断K+是否存在?________(填“是”或“否”);若存在,K+的物质的量浓度c(K+)的范围是__________________。(若K+不存在,则不必回答该问)
(5)设计简单实验验证原水样中可能存在的离子:_____________________。(写出实验步骤、现象和结论)
查看答案和解析>>
科目: 来源: 题型:
【题目】石油加工能获得多种化工产品,从物质类别上看主要包含烷烃、烯烃和炔烃等。
(1)石油蒸馏可得分子式为C4H6的烃,其结构可能是1-丁炔,也可能是CH2=CHCH=CH2。下列事实能证明是炔烃而不是CH2=CHCH=CH2的是 __________。
①燃烧时有浓烟 ②能使酸性KMnO4溶液褪色 ③所有原子不在同一平面上 ④与足量溴水反应,生成物中只有2个碳原子上有溴原子
A.①② B.②③ C.③④ D.①④
(2)现有A、B两种烃,它们都来源于石化工业,已知A的分子式为C5Hm, 而B的最简式为C5Hn(m、n均为正整数)。
①下列关于烃A和烃B的说法中不正确的是________(填序号)。
A.烃A和烃B可能互为同系物
B.烃A和烃B可能互为同分异构体
C.当m=12时,烃A一定为烷烃
D.当n=11时,烃B可能的分子式有2种
②若烃A为链状烃,且分子中所有碳原子都在同一条直线上, 则A的结构简式为_____。
③若烃A为链状烯烃,分子中所有碳原子一定共平面,在一定条件下,1 molA最多可与1 molH2加成,则A的名称是____________。
(3)乙炔主要来源之一是石化工业,某研究小组同学为了探究乙炔与HBr发生加成反应后的有关产物,进行以下实验:![]() 。
。
①有机混合物可能含有的物质是_____________(写结构简式)。
②控制反应条件,乙炔经过三步反应可合成![]() ,请写出相应反应方程式___________、________、 ________(可不注明反应条件)。
,请写出相应反应方程式___________、________、 ________(可不注明反应条件)。
查看答案和解析>>
科目: 来源: 题型:
【题目】NaNO2可将正常的血红蛋白中的二价铁变为高铁血红蛋白中的三价铁,失去携氧能力。完成下列填空:
(1)N元素在元素周期表中位于第____族,N原子的结构示意图______________。
(2)Na、N、O三种元素形成的简单离子中,离子半径最小的是_______(用离子符号表示)。
(3)某工厂的废液中含有2%~5%的NaNO2直接排放会造成污染。下列试剂中,能使NaNO2转化为N2的是______________(选填编号)。
a.NaCl b.NH4Cl c.HNO3 d.H2SO4
(4)已知NaNO2能发生如下反应:NaNO2 + HI → NO↑+ I2 + NaI + H2O
①配平反应物的系数并标出电子转移的方向和数目__NaNO2 +__ HI → NO↑+ I2 + NaI + H2O 。
②当有0.75mol HI被氧化时,在标准状况下产生气体的体积是_______L。
(5)NaNO2外观与食盐相似,根据上述反应,可用于鉴别NaNO2和NaCl。现有 ①白酒、②碘化钾淀粉试纸、③淀粉、④白糖、⑤白醋,其中可选用的物质至少有______(选填编号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 标准状况下,2.24LCH3OH分子中共价键的数目为0.5NA
B. 1molNa2O2与足量CO2充分反应,转移的电子数为2 NA
C. 25℃1LpH=12的Na2CO3溶液中,由水电离出H+的数目为0.01NA
D. 0.1molH2和0.1molI2于密闭容器中充分反应后,HI分子总数为0.2NA
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据官能团的不同对下列有机物进行分类。
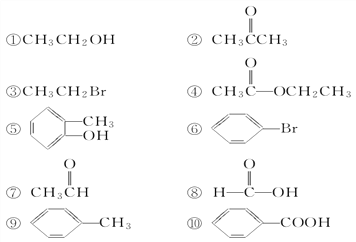
(1)芳香烃:________;
(2) 卤代烃:________;
(3) 醇:________;
(4)醛:________;
(5)羧酸:________;
(6)酯:________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com