
科目: 来源: 题型:
【题目】某活动小组为探究金属腐蚀的相关原理,设计了如图a所示的装置,图a的铁棒末端分别连上一块Zn片和Cu片,并置于含有K3Fe(CN)6及酚酞的混合凝胶上.一段时间后发现凝胶的某些区域(如图b所示)发生了变化.已知Fe2+可用K3Fe(CN)6来检验(呈蓝色).则下列说法不正确的是( )

A. 甲区发生的电极反应式为Fe-2e═Fe2+ B. 乙区产生Zn2+
C. 丙区呈红色 D. 丁区呈蓝色
查看答案和解析>>
科目: 来源: 题型:
【题目】铁、铝的混合物进行如下实验:
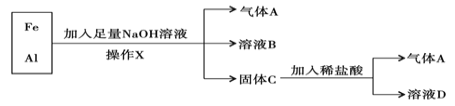
(1)操作X的名称是 ;
(2)气体A是 (填化学式);
(3)A与Cl2混合光照可能发生爆炸,生成 (填化学式),A在该反应中作为 (填“氧化剂”或“还原剂”);
(4)溶液B中阴离子除OH- 外还有________________ (填离子符号),溶液D中存在的金属离子为________________________ (填离子符号);
(5)加入足量NaOH溶液时发生反应的离子方程式为:_____________________;加入稀盐酸发生反应的离子方程式为: ___________________________;
(6)向溶液D加入NaOH溶液,观察到产生的白色絮状沉淀迅速变为灰绿色,最终变为红褐色,请写出沉淀转化的化学方程式:_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组为了制取、收集纯净干燥的氯气并探究氯气的性质,他们设计了如图所示的实验装置:

请回答下列问题:
(1)整套实验装置的连接顺序是f接( )( )接( )( )接( )(填各接口处的字母代号)。
(2)E装置中制取氯气的离子方程式是 。
(3)A装置中试剂X是 。
(4)C装置中的现象是 产生此现象的原因是 (用离子方程式和必要的文字解释)。
查看答案和解析>>
科目: 来源: 题型:
【题目】在T℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知T℃时AgCl的Ksp=2×10 -10,下列说法不正确的是( )
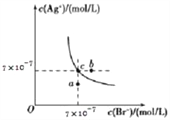
A. 在T℃时,AgBr的Ksp为4.9×10-13
B. 在AgBr的饱和溶液中加入NaBr固体,可使溶液由c点到b点
C. 图中a点对应的是含AgBr的不饱和溶液
D. 在T℃时,AgCl(s)+Br -(aq)![]() AgBr(s)+Cl -(aq)的平衡常数K≈408
AgBr(s)+Cl -(aq)的平衡常数K≈408
查看答案和解析>>
科目: 来源: 题型:
【题目】由几种离子化合物组成的混合物,含有以下离子中的若干种:K+、NH4+、Mg2+、Cu2+、Ba2+、C1—、SO42—、CO32-。将该混合物溶于水后得无色澄清溶液,现分别取3份100mL该溶液进行如下实验:
实验序号 | 实验内容 | 实验结果 |
a | 加AgNO3溶液 | 有白色沉淀生成 |
b | 加足量NaOH溶液并加热 | 收集到气体1.12L(已折算成标准状况下的体积) |
c | 加足量BaC12溶液时,对所得沉淀进行洗涤、干燥、称量;再向沉淀中加足量稀盐酸,然后干燥、称量 | 第一次称量读数为6.27g,第二次称量读数为2.33g |
试回答下列问题:
(1)该混合物中一定不存在的离子是 。
(2)试写出实验b发生反应的离子方程式 。
(3)溶液中一定存在的阴离子及其物质的量浓度(可不填满):
阴离子符号 | 物质的量浓度(mol·L—1) |
(4)判断混合物中是否存在K+,如果不存在,请说明理由,如果存在,请求出C(K+)的取值范围? 。
(5)Ba2+是一种重金属离子,某环境监测小组欲利用Na2S2O3、KI、K2Cr2O7等试剂测定某工厂废水中Ba2+的浓度。取废水50.00mL,控制适当的酸度加入足量的K2Cr2O7溶液,得BaCrO4沉淀;沉淀经洗涤、过滤后,用适量的稀盐酸溶解,此时CrO42-全部转化为Cr2O72-;再加过量KI溶液反应,反应液中再滴加0.100 mol·L-1Na2S2O3溶液,反应完全时,消耗Na2S2O3溶液36.00mL。已知有关的离子方程式为:
①Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O/span>;
②I2+2S2O32-=2I-+S4O62-。
试计算该工厂废水中Ba2+的物质的量浓度。(写出具体计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验设计及其对应的离子方程式均正确的是( )
A. 醋酸溶液除去水垢中的CaCO3:CaCO3+2H+![]() Ca2++H2O+CO2↑
Ca2++H2O+CO2↑
B. 向稀盐酸溶液中加入铁粉:2Fe+6 H+![]() 2Fe3+ + 3H2↑
2Fe3+ + 3H2↑
C. 用FeCl3溶液腐蚀铜线路板:Cu + 2Fe3+ ![]() Cu2+ + 2 Fe2+
Cu2+ + 2 Fe2+
D. 向氯化亚铁溶液中通入氯气:Fe2+ +Cl2=Fe3+ +2Cl-
查看答案和解析>>
科目: 来源: 题型:
【题目】奶粉中蛋白质含量的测定往往采用“凯氏定氮法”,其原理是食品与硫酸和催化剂一同加热,使蛋白质分解,分解的氨与硫酸结合生成硫酸铵。然后碱化蒸馏使氨游离,用硼酸吸收后再以硫酸或盐酸标准溶液滴定,根据酸的消耗量乘以换算系数,即为蛋白质含量。
操作步骤:
①样品处理:准确称取一定量的固体样品奶粉,移入干燥的烧杯中,经过一系列的处理,待冷却后移入一定体积的容量瓶中。
②NH3的蒸馏和吸收:把制得的溶液(取一定量),通过定氮装置,经过一系列的反应,使氨变成硫酸铵,再经过碱化蒸馏后,氨即成为游离态,游离氨经硼酸吸收。
③氨的滴定:用标准盐酸溶液滴定所生成的硼酸铵,由消耗的盐酸标准液计算出总氮量,再折算为粗蛋白含量。
请回答下列问题:
(1)在样品的处理过程中使用到了容量瓶,怎样检查容量瓶是否漏水_________。
(2)在配制过程中,下列哪项操作可能使配制的溶液的浓度偏大_______。
A.烧杯中溶液转移到容量瓶中时,未洗涤烧杯 B.定容时,俯视刻度线
C.定容时,仰视刻度线 D.移液时,有少量液体溅出
(3)若称取样品的质量为1.5g,共配制100mL的溶液,取其中的20mL,经过一系列处理后,使N转变为硼酸铵然后用0.1mol·L-1盐酸滴定,其用去盐酸的体积为23.0mL,则该样品中N的含量为________。
(滴定过程中涉及到的反应方程式:(NH4)2B4O7+2HCl+5H2O=2NH4Cl+4H3BO3)
(4)一些不法奶农利用“凯氏定氮法”只检测氮元素的含量而得出蛋白质的含量这个检测法的缺点,以便牛奶检测时蛋白质的含量达标,而往牛奶中添加三聚氰胺(C3N6H6)。则三聚氰胺中氮的含量为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】连二亚硫酸钠(Na2S2O4)俗称保险粉,广泛用于纺织工业的还原性染色、清洗、印花、脱色以及织物的漂白等。制取保险粉通常需要二氧化硫。
(1)制备二氧化硫
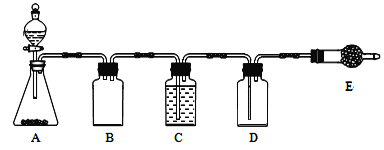
若使用上图所示装置制备干燥的SO2气体,回答以下问题:
①A中盛液体的玻璃仪器名称是____________,实验开始后A中反应的化学方程式为
______________________________________________________。
②B装置的作用是_______________________;C装置的试剂为__________________。
③E中固体试剂为________________。
(2)制备保险粉(略)
(3)测定保险粉纯度
Na2S2O4属于强还原剂,暴露于空气中易被氧气氧化。Na2S2O4遇KMnO4酸性溶液发生反应:5Na2S2O4 + 6KMnO4 + 4H2SO4 = 5Na2SO4 + 3K2SO4 + 6MnSO4 + 4H2O,称取3.0g Na2S2O4样品溶于冷水中,配成100mL溶液,取出10mL该溶液于试管中,用0.10mol·L-1的KMnO4溶液滴定。
①滴定时KMnO4溶液装在__________________(玻璃仪器)中。
②滴定终点的标志_______________________________________________________。
重复上述操作2次,平均消耗KMnO4溶液18.00 mL则该样品中Na2S2O4的质量分数为____________(杂质不参与反应)。
查看答案和解析>>
科目: 来源: 题型:
【题目】10℃时加热NaHCO3饱和溶液,测得该溶液的pH发生如下变化:
温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
pH | 8.3 | 8.4 | 8.5 | 8.8 |
根据上述数据:甲同学认为,该溶液的pH升高的原因是HCO3-的水解程度增大,故碱性增强,该反应的离子方程式为____________________________。乙同学认为,溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度_______(填“大于”或“小于”)NaHCO3。丙同学认为甲、乙的判断都不充分。丙认为:
(1)只要在加热煮沸的溶液中加入足量的试剂X,若产生沉淀,则____(填“甲”或“乙”判断正确。试剂X是_____________(填序号)。
A.Ba(OH)2溶液 B.BaCl2溶液 C.NaOH溶液 D.澄清的石灰水
(2)将加热后的溶液冷却到10℃,若溶液的pH_____(填“高于”、“低于”或“等于”)8.3,则_____(填“甲”或“乙”)判断正确。
(3)查阅资料,发现NaHCO3的分解温度为150℃,丙断言_____(填“甲”或“乙”)判断是错误的,理由是_____________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)25℃时,0.1 mol L-1 HCl溶液中,Kw=__________________,c(Cl-)=____________,c(OH-)=______________, pH=_______。
(2)25℃时,将等体积、等物质的量浓度的醋酸和氢氧化钠溶液混合后,溶液呈______(填“酸性”,“中性”或“碱性”),溶液中c(Na+ ) ______c(CH3COO-)(填“ >”,“=”或“<” )。
(3)25℃时, pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈__________(填“酸性”,“中性”或“碱性”),溶液中c(Na+ ) ______c(CH3COO-) (填“ >” ,“=”或“<” )。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com