
科目: 来源: 题型:
【题目】下列关于Na2CO3和NaHCO3的说法中,不正确的是
A. 均属于盐
B. 焰色反应均为黄色
C. 可以用加热的方法除去Na2CO3固体中的NaHCO3杂质
D. 物质的量相同的两种固体分别与足量盐酸反应,Na2CO3产生的二氧化碳多
查看答案和解析>>
科目: 来源: 题型:
【题目】结合某城市某日空气质量报告内容,以下叙述正确的是

A. 该日空气首要污染物是PM2.5
B. 该日空气质量等级属于优
C. 污染物NO2、CO可能主要来源于机动车尾气
D. PM2.5、PM10指的是悬浮颗粒物,不会影响人体健康
查看答案和解析>>
科目: 来源: 题型:
【题目】氯气是一种重要的工业原料,某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4![]() 2CaSO4+2Cl2↑+2H2O。他们利用该反应设计如图所示装置制取氯气并验证其性质的实验。(B中装淀粉KI溶液,C中装Na2SO3溶液,D中装FeCl2溶液)
2CaSO4+2Cl2↑+2H2O。他们利用该反应设计如图所示装置制取氯气并验证其性质的实验。(B中装淀粉KI溶液,C中装Na2SO3溶液,D中装FeCl2溶液)

回答下列问题:
(1)该实验中A部分的装置是______(填标号)。

(2)装置B中产生的现象为______。
(3)请设计实验验证装置C中的Na2SO3已被氧化______。
(4)写出D装置中发生反应的离子方程式______。
(5)该实验存在明显的缺陷,请你提出改进的方法______。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定温度下的定容容器中,当下列哪些物理量不再发生变化时,表明反应:
A(s)+2B(g)![]() C(g)+D(g)已达到平衡状态的是( )
C(g)+D(g)已达到平衡状态的是( )
① 混合气体的压强;② 混合气体的密度;③ B的物质的量浓度;④ 气体总物质的量;⑤ 混合气体的平均相对分子质量;⑥ C、D反应速率的比值
A. ②③⑤ B. ①②③ C. ②③④⑥ D. ①③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示.下列判断正确的是( )
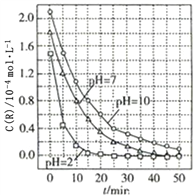
A. 在20~25min之间,pH=10时R的平均降解速率为0.04molL-1min-1
B. 溶液酸性越强,R的降解速率越小
C. R的起始浓度越小,降解速率越大
D. 50min时,pH=2和pH=7时R的降解百分率相等
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组欲进行如下的实验探究金属与浓硫酸反应。试回答下列问题:
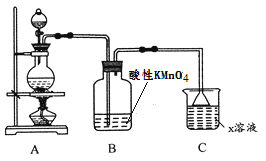
(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为_____________________。
(2)C装置的作用___________________。
(3)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是_______________。在加热条件下,实验的后阶段可观察到倒立的漏斗边沿有气体冒出,该气体可能为_______。
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、Al2O3及不溶于强酸的SiO2)可制备Fe2O3。①用稀盐酸浸取炉渣,过滤;②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。据以上信息回答下列问题:
a.除去Al3+的离子方程式是______________________________。
b.步骤②中滤液氧化的目的是_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g)![]() 2HI(g)△H=-a kJmol-1。
2HI(g)△H=-a kJmol-1。
已知:

下列说法正确的是( )
A. 该反应为吸热反应
B. 断开2 mol HI分子中的化学键所需能量约为(c+b+a)kJ
C. 反应物的总能量低于生成物的总能量
D. 向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室里迅速制备少量氯气可利用以下反应: KClO3+6HCl = KCl + 3 Cl2↑ +3 H2O此反应不需要加热,常温下就可以迅速进行,而且对盐酸的浓度要求不高。
(1)用“双线桥法”表示出电子转移情况:KClO3+6HCl =KCl + 3Cl2↑ +3H2O______
(2)该反应中,氧化剂是__________。
(3)在标准状况下,若生成4.48L Cl2,则所含氯原子数目为_______个(用NA表示)
(4)当有0.5molHCl被氧化时,则 有_____________mol KClO3被还原。
(5)浓盐酸在反应中表现出来的性质是__________(填写编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性。
查看答案和解析>>
科目: 来源: 题型:
【题目】意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的气态N4分子,其分子结构如右图所示。已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N![]() N放出942 kJ热量,根据以上信息和数据,判断下列说法正确的是
N放出942 kJ热量,根据以上信息和数据,判断下列说法正确的是

A.N4属于一种新型的化合物
B.N4分子中存在非极性键
C.N4分子中N—N键角为109°28′
D.1 mol N4转变成N2将吸收882 kJ热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com