
科目: 来源: 题型:
【题目】向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化的情况如图甲所示。图乙为t2时刻后改变反应条件,该平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3~t4阶段为使用催化剂;图甲中t0~t1阶段c(B)未画出。
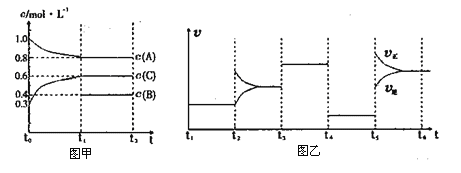
下列说法不正确的是
A. 该反应为吸热反应
B. B在t0~t1阶段的转化率为60%
C. t4~t5阶段改变的条件为减小压强
D. 此温度下该反应的化学平衡常数K=0.84
查看答案和解析>>
科目: 来源: 题型:
【题目】下列实验的反应原理用离子方程式表示正确的是( )
A. 室温下,测的氯化铵溶液pH<7,证明一水合氨的是弱碱:NH4++2H2O=NH3·H2O+H3O+
B. 用氢氧化钠溶液除去镁粉中的杂质铝:2Al+2OH-+2H2O=2AlO2-+3H2↑
C. 用碳酸氢钠溶液检验水杨酸中的羧基:
 +2HCO3-→
+2HCO3-→ +2H2O+2CO2↑
+2H2O+2CO2↑
D. 用高锰酸钾标准溶液滴定草酸:2MnO4-+16H++5C2O42-=2Mn2++10CO2↑+8H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于浓硫酸特性的叙述不正确的是
A. 浓硫酸具有吸水性、脱水性和强氧化性等特性
B. 浓硫酸能吸收气体中的水蒸气,常作氨气、二氧化硫等气体的干燥剂
C. 浓硫酸可以吸收固体中的湿存水、结晶水合物中的结晶水
D. 在反应C12H22O11![]() 12C+11H2O,浓硫酸作脱水剂
12C+11H2O,浓硫酸作脱水剂
查看答案和解析>>
科目: 来源: 题型:
【题目】药物贝诺酯可由乙酰水杨酸和对乙酰氨基酚在一定条件下反应制得:
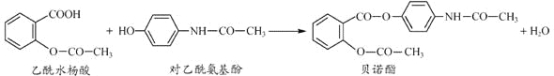
下列有关叙述正确的是( )
A. 贝诺酯分子中有三种含氧官能团
B. 可用FeCl3溶液区别乙酰水杨酸和对乙酰氨基酚
C. 乙酰水杨酸和对乙酰氨基酚均能与NaHCO3溶液反应
D. 贝诺酯与足量NaOH 溶液共热,最终生成乙酰水杨酸钠和对乙酰氨基酚钠
查看答案和解析>>
科目: 来源: 题型:
【题目】一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg![]() 3Fe+4MgS,装置如图所示。下列说法不正确的是
3Fe+4MgS,装置如图所示。下列说法不正确的是
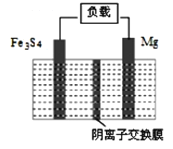
A. 放电时,电路中转移0.5mol电子则阴离子交换膜上移动0.5molS2—
B. 放电时,正极的电极反应式为Fe3S4+8e-=3Fe+4S2—
C. 充电时,阴极的电极反应式为MgS+2e-=Mg+S2—
D. 充电时,S2—从阴离子交换膜左侧向右侧迁移
查看答案和解析>>
科目: 来源: 题型:
【题目】室温时,向20 mL 0.1 mol·L-1NH4HSO4溶液中滴加0.1 mol·L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生,且混合溶液的体积可看成混合前两溶液的体积之和),下列说法不正确的是:
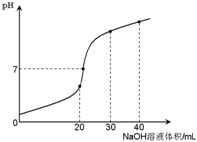
A. pH=7时,溶液中c(Na+)>c(SO42-)>c(NH4+)>c(OH-)=c(H+)
B. 当V(NaOH)=20mL时,溶液中水的电离程度比纯水大
C. 当V(NaOH)=30mL时,溶液中 c(SO42-)+ c(H+)= c(NH3·H2O) + c(OH-)
D. 滴加NaOH溶液从30mL至40mL,溶液中Na+与SO42-浓度之和始终为0.1 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】锎是锕系中的一种元素,1 mg锎(![]() )每秒钟约能释放出2.34×109个中子,在医学上常用作治疗恶性肿瘤的中子源。下列有关说法错误的是 ( )
)每秒钟约能释放出2.34×109个中子,在医学上常用作治疗恶性肿瘤的中子源。下列有关说法错误的是 ( )
A. ![]() 中,质子数和电子数均为98 B.
中,质子数和电子数均为98 B. ![]() 和
和![]() 互为同位素
互为同位素
C. 锎位于元素周期表第六周期 D. ![]() 的中子数与质子数之差为56
的中子数与质子数之差为56
查看答案和解析>>
科目: 来源: 题型:
【题目】向50 mL 18 mol·L-1的H2SO4溶液中加入适量的铜片并加热。充分反应后,被还原的H2SO4的物质的量( )
A. 小于0.45 mol B. 等于0.45 mol
C. 在0.45~0.90 mol之间 D. 大于0.45 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个化学反应:SO2+2Fe3++2H2O===![]() +2Fe2++4H+,Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++ 7H2O,有关说法正确的是
+2Fe2++4H+,Cr2O72-+6Fe2++14H+===2Cr3++6Fe3++ 7H2O,有关说法正确的是
A. 还原性Cr3+>Fe2+>SO2
B. 氧化性Cr2O72->SO2>Fe3+
C. 两个反应中Fe2(SO4)3均作还原剂
D. Cr2O72-能将Na2SO3氧化成Na2SO4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com