
科目: 来源: 题型:
【题目】下列有关物质分类说法正确的是( )
A.纯碱、液态氧、碘酒、稀盐酸依次是盐、单质、混合物、电解质
B.干冰、生石灰、硫酸、碳酸氢铵依次是电解质、氧化物、酸、盐
C.氯化氢、氨气、水银、草木灰依次是电解质、非电解质、单质、混合物
D.冰水、空气、泥水依次是溶液、胶体、浊液
查看答案和解析>>
科目: 来源: 题型:
【题目】鲍林被认为是20世纪对化学科学影响最大的人之一,他也是两位获得诺贝尔奖不同奖项的人之一。杂化轨道是鲍林为了解释分子的立体构型提出的,下列对sp3、sp2、sp杂化轨道的夹角的比较,得出结论正确的是( )
A.sp杂化轨道的夹角最大
B.sp2杂化轨道的夹角最大
C.sp3杂化轨道的夹角最大
D.sp3、sp2、sp杂化轨道的夹角相等
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关酶的叙述中,正确的是
A.酶的催化效率总是高于无机催化剂
B.一个酶分子只起一次作用
C.酶催化反应能放出更多的能量
D.催化蛋白质水解的酶的化学本质是蛋白质
查看答案和解析>>
科目: 来源: 题型:
【题目】向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化曲线如图所示.有关说法不正确的是( )

A. 线段BC代表Fe3+的物质的量的变化情况
B. 原混合溶液中c(FeBr2)=6 mol/L
C. 当通入 2mol Cl2时,溶液中已发生的离子反应可表示为2Fe2++2I-+2Cl2═2Fe3++I2+4Cl-
D. 原溶液中n(Fe2+):n(I-):n(Br-)=2:1:3
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,在镁屑和无水乙醚的混合体系中,滴加卤代烷,反应后得到的有机镁化合物称为格氏试剂。制备的格氏试剂不需要分离就可直接用于有机合成,是重要的有机合成中间体。反应原理为:![]()
利用A(![]() )来合成
)来合成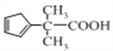 的流程如图所示:
的流程如图所示:

(1)物质A的名称为________;
(2)A![]() B的反应类型是_________;
B的反应类型是_________;
(3)写出由F生成G、G生成H的化学方程式:_____________________________;
(4)D的同分异构体中含有六元环且能发生银镜反应的有___________种;
(5)写出符合下列要求的I的同分异构体的结构简式_________;(写一种即可,已知同一个碳原子上不能连接2个羟基)
①芳香族化合物 ②二元醇 ③分子中有5种不同化学环境的H原子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列所给的化学反应中,不属于氧化还原反应的是
A. CaCO3+2HCl = CaCl2+CO2↑+H2O
B. Fe+CuSO4 =Cu+FeSO4
C. Fe2O3+3CO![]() 2Fe+3CO2↑
2Fe+3CO2↑
D. 2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】合金是金属与一些非金属或其他金属在熔化状态下形成的一种熔合物,根据下表中提供的数据,判断可以形成合金的是( )
金属或非金属 | 钠 | 铝 | 铁 | 硅 | 硫 |
熔点/℃ | 97.8 | 660.4 | 1535 | 1410 | 112.8 |
沸点/℃ | 886 | 2467 | 2750 | 2353 | 444.6 |
A.铝与硫B.铝与硅C.钠与铁D.钠与硅
查看答案和解析>>
科目: 来源: 题型:
【题目】请按下列要求填空:
(1)已知99 ℃时,水的离子积常数Kw=1.0×10-12,该温度下测得0.1 mol·L-1 Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为_________________________。
②体积相等、pH=1的盐酸与H2A溶液分别与足量Zn反应,产生的氢气___(填编号)。
A.盐酸多 B.H2A多 C.一样多 D.无法确定
③将0.1 mol·L-1 H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为__________________________________。
(2)常温下,HNO2 的电离常数Ka=7.1×10-4mol·L-1,NH3·H2O的电离常数Kb=1.7×10-5mol·L-1。0.1mol·L-1 NH4NO2 溶液中离子浓度由大到小的顺序是__________________
(3)在强酸性的电解质水溶液中,惰性材料做电极,电解CO2可得到多种燃料,其原理如图所示。

① 乙烯电子式为_________
②b电极的名称是_________
③请写出电解时生成乙烯的电极反应式____________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】化学反应原理在科研和生产中有广泛应用。
(1)用生物质热解气(主要成分为CO、CH4、H2)将SO2在一定条件下还原为单质硫进行烟气脱硫。已知:
①C(s)+O2(g)=CO2(g) △H1=-393.5 kJ·mol-1
②CO2(g)+C(s)=2CO(g) △H2= + 172.5 kJ·mol-1
③S(s)+O2(g)=SO2(g) △H3=- 296.0 kJ·mol-1
CO将SO2还原为单质硫的热化学方程式为________________________。
(2)CO可用于合成甲醇,一定温度下,向体积为2 L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)![]() CH3OH(g),5分钟后达到平衡测得各组分物质的量如下:
CH3OH(g),5分钟后达到平衡测得各组分物质的量如下:
物质 | CO | H2 | CH3OH |
物质的量(mol) | 1.8 | 2.0 | 1.2 |
①反应达到平衡时,CO的转化率为_______,5分钟内用H2表示的速率为________
②该反应的平衡常数K=__________。
③恒温恒容条件下,可以说明反应已达到平衡状态的是__________(填标号)。
A.v正(CO)=2v逆(H2) B.混合气体的密度不变
C.混合气体的平均相对分子质量不变 D.CO、H2的浓度之比为1:2
E.单位时间内,每生成1mol H2消耗2mol CH3OH
④若将容器体积压缩到1L,则达到新平衡时c(H2)的取值范围是_____________。
⑤若保持容器体积不变,再充入0.6 mol CO 和0.4 mol CH3OH,此时v正 __________v逆(填“ >” < ”或“= ”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列几种物质的保存方法中不正确的是
A.碘易升华,可保存在酒精中
B.少量金属钠保存在煤油中
C.氯水通常保存在棕色细口瓶并置于阴凉处
D.在盛液溴的试剂瓶中加水,形成“水封”,以减少溴的挥发
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com