
科目: 来源: 题型:
【题目】下列有关问题,与盐的水解有关的是( )
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
②用NaHCO3与Al2(SO4)3两种溶液可作泡沫灭火剂
③草木灰与铵态氮肥不能混合施用
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤加热蒸干AlCl3溶液得到Al(OH)3固体
A. ①②③ B. ②③④
C. ①④⑤ D. ①②③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.电离时能生成H+的化合物是酸
B.水溶液显碱性的物质是碱
C.电解质电离时产生的阴离子全部是OH-的化合物是碱
D.能与碱发生反应生成水的化合物是酸
查看答案和解析>>
科目: 来源: 题型:
【题目】汽水是CO2的饱和溶液,其中存在如下平衡:
H2CO3![]() H++HCO3-……① HCO3-
H++HCO3-……① HCO3-![]() H++CO32-……②
H++CO32-……②
将汽水倒入试管中分别进行下列实验,相应分析结论错误的是
A.加热、平衡①、②可能都向左移动
B.加入澄清石灰水,平衡①、②均向右移动
C.加入CaCO3悬浊液,CaCO3的溶解平衡向正方向移动
D.通入过量CO2或滴加氯水,溶液pH均减小
查看答案和解析>>
科目: 来源: 题型:
【题目】生活中处处有化学。请回答下列问题
(1)苏打水是很多人喜爱的饮品,请写出小苏打在水中的电离方程式__________
(2)“84消毒液”与洁厕灵(主要成分是浓盐酸)不能混用,混合会产生黄绿色的有毒气体,请用离子反应方程式解释原因____________
(3)咖啡中含有咖啡因(C8H10N4O2),咖啡因可以使我们的神经兴奋,若一杯咖啡中含有0.194g咖啡因,则这杯咖啡中有______________个咖啡因分子。
查看答案和解析>>
科目: 来源: 题型:
【题目】经过多方努力,郑州市的空气质量有明显改善。造成雾霾的重要原因之一是汽车尾气的排放,汽车加装尾气处理装置可以减少有害尾气的排放。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如下图所示。下列说法错误的是
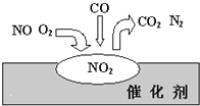
A. NO2是该过程的中间产物
B. 汽车尾气的主要污染成分为CO和NO
C. NO和O2必须在催化剂表面才能反应
D. 该催化转化的总反应方程式:2NO+O2+4CO![]() 4CO2+N2
4CO2+N2
查看答案和解析>>
科目: 来源: 题型:
【题目】下列表示不正确的是( )
A. 氯离子的结构示意图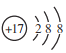 B. 四氯化碳分子的电子式:
B. 四氯化碳分子的电子式: 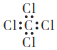
C. CH4的球棍模型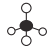 D. 明矾的化学式:KAl(SO4)2·12H2O
D. 明矾的化学式:KAl(SO4)2·12H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备氧化铝的主要原料。工业上提取氧化铝的工艺流程如下:
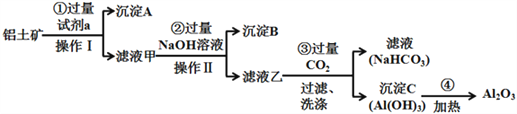
(1)沉淀A的成分是(填化学式)_________。
(2)步骤②中加入过量NaOH溶液发生反应的离子方程式,除了H++OH﹣=H2O外,还有:
_____________________________、________________________________;
(3)步骤③中加入(或通入)的过量试剂b是______________。
Ⅱ. 利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
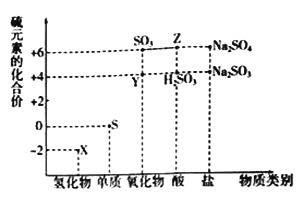
(4)从硫元素化合价的角度分析,图中既有氧化性又有还原性的化合物有______________(填化学式)。
(5)将X与Y混合,可生成淡黄色固体,该反应的化学方程式为_________________________。
(6)Na2S2O3是重要的化工原料,从氧化还原反应的角度分析,下列制备Na2S2O3的方案理论上可行的是______(填代号).
a.Na2S+S b.Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+Na2SO4
查看答案和解析>>
科目: 来源: 题型:
【题目】判断含氧酸强弱的一条经验规律:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。几种实例如下表所示。
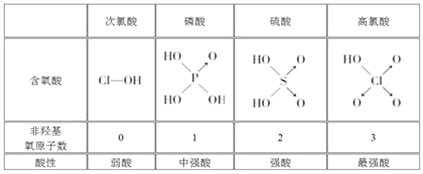
(1)亚磷酸(H3PO3)和亚砷酸(H3AsO3)的分子式相似,但它们的酸性差别很大。亚磷酸是中强酸,亚砷酸既有弱酸性又有弱碱性,由此可推出它们的结构式分别为:亚磷酸______________________,亚砷酸________________________。
(2)亚磷酸和亚砷酸与过量的NaOH溶液反应的化学方程式分别是:
亚磷酸:______________________________________,
亚砷酸:_______________________________________。
(3)在亚磷酸和亚砷酸中分别加入浓盐酸,分析反应情况,写出化学方程式_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】二氧化氯是一种黄绿色有刺激性气味的气体,其熔点为-59℃,沸点为11.0℃,易溶于水。工业上用稍潮湿的KC1O3和草酸(H2C2O4)在60℃时反应制得。某学生用下图所示的装置模拟工业制取及收集C1O2,其中A为C1O2的发生装置,B为C1O2的凝集装置,C为尾气吸收装置。
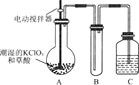
请回答下列问题:
(1)A中反应产物有K2CO3、C1O2和CO2等,请写出该反应的化学方程式:________________________。
A部分还应添加温水浴控制温度在60 °C,B部分还应补充什么装置:_________________。
(2)该装置按(1)补充完整后,装置A、B、C中还有一处设计明显不合理的是_____(填“A”“B”或“C”)。
(3)C中的试剂为NaOH溶液,反应时生成氯酸钠和亚氯酸钠(NaClO2),该反应的离子方程式为____________。若实验时需要450 mL 4 mol L-1的NaOH溶液,则在精确配制时,需要称取NaOH的质量是____g,所使用的仪器除托盘天平、量筒、胶头滴管、玻璃棒外,还必须有_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com