
科目: 来源: 题型:
【题目】在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下进行反应,一段时间后测得反应前后各物质质量如表.该密闭容器中发生化学反应的基本类型可能是
物质 | X | Y | Z | Q |
反应前质量/g | 20 | 20 | 20 | 20 |
反应后质量/g | 20 | 30 | 16 | 14 |
A.分解反应B.置换反应C.复分解反应D.化合反应
查看答案和解析>>
科目: 来源: 题型:
【题目】R2O8n-在一定条件下可以把 Mn2+氧化为 MnO4-,若反应后 R2O8n-变成 RO42-,又知反应中氧化剂与还原剂的物质的量之比为 5:2,则 R2O8n-中 R 元素的化合价为( )
A. +7 B. +6 C. +3 D. +5
查看答案和解析>>
科目: 来源: 题型:
【题目】为了探究过氧化钠的强氧化性,某研究性学习小组设计了如图所示的实验装置。
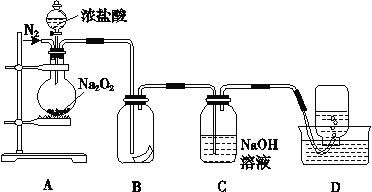
实验步骤及现象如下:
①检查装置气密性后,装入药品Na2O2并连接仪器。
②缓慢通入一定量的N2后,将装置D连接好(导管末端未伸
入集气瓶中),再向圆底烧瓶中缓慢滴加浓盐酸,剧烈反应,产生黄绿色气体。
③一段时间后,将导管末端伸入集气瓶中收集气体。装置D中收集到能使带火星的木条复燃的无色气体。
④反应结束后,关闭分液漏斗的活塞,再通入一定量的N2,至装置中气体无色。
回答下列问题:
(1)装置B中湿润的红色纸条褪色,证明A中反应有______(填化学式)生成。若将B中红纸条改为湿润的紫石蕊试纸,现象为 _______
(2)实验前通N2的目的 ____,装置C的作用是_______
(3)甲同学认为O2是Na2O2被盐酸中的HCl还原所得。乙同学认为此结论不正确,其不赞成的理由可能为: ①_______;②O2有可能是Na2O2与盐酸中的H2O反应所得.
查看答案和解析>>
科目: 来源: 题型:
【题目】小苏打长期放置在空气中会变质(部分转变为Na2CO3),某研究小组欲测定某小苏打样品中NaHCO3的质量分数,设计如下实验方案:
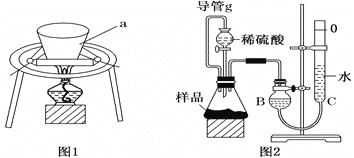
Ⅰ、加热分解法
利用图1装置,充分加热小苏打样品。
(1)仪器a的名称为___________________。
(2)在实验过程中,需要测量的实验数据有:
①仪器a的质量W1g;
②加热前,仪器a和样品的总质量W2g;
③加热冷却后,仪器a和残留物的总质量W3g。
(3)列出小苏打样品中NaHCO3的质量分数的计算式____________________
Ⅱ、测量气体体积法
利用图2装置,测定反应生成气体的体积。
(1)组装好仪器后,首先进行的操作为_________________________________________。
(2)导管g的作用为_________________________________________________________。
(3)为了减小实验误差,B、C中最好用________________溶液代替水。
(4)待反应结束,气体冷却至室温后,利用图示装置读取气体体积时,应注意的事项有:
①读数时应上下移动C管,使B、C两管液面相平;
②视线与液面最低处相平。
(5)若所取样品的质量为m g,反应前滴定管C的读数为V1 mL,反应结束后滴定管C的读数为V2 mL,则样品中NaHCO3和Na2CO3的物质的量之和为_______________(气体体积均已换算为标准状况下的体积)。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙、丁均为中学化学常见的纯净物,它们之间有如下图所示的反应关系。下列物质组不满足上述转化关系的是
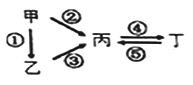
选项 | 甲 | 乙 | 丙 | 丁 |
A | Fe | FeCl2 | FeCl3 | Fe(OH)3 |
B | Si | SiO2 | Na2SiO3 | Na2CO3 |
C | Na | Na2O | Na2O2 | NaOH |
D | Al | Al2O3 | NaAlO2 | Al(OH)3 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】在强酸性溶液中能大量共存的无色透明离子组是( )
A. K+、Na+、CO32-、Cl- B. NH4+、Na 十、Br-、Cu2+
C. Mg2+、Na+、NO3-、SO42- D. Na十、Ba2+、OH-、SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】钠和钠的化合物有许多重要的用途。
(1)碳酸钠可用于从海水提取溴,涉及的反应如下:3Br2+6Na2CO3+3H2O=5NaBr+NaBrO3+6NaHCO3,在上述反应中用双线桥法标出电子转移的方向和数目_______________;该反应中氧化剂与还原剂的物质的量之比是 __________。
(2)少量的钠应保存在_________中;钠着火时应采取的灭火措施是_______。
(3)过氧化钠作潜艇供氧剂时发生的化学反应方程式是__________________;该反应的氧化产物是_____________。
(4)厨房中存放的纯碱和小苏打无法用外观区别时,请你设计用厨房现有的物质来区分它们的方法_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有X、Y、Z三种物质,它们之间存在如下转化关系:
![]()
(1)若X、Y、Z三种物质的焰色反应均为黄色,三个反应均为化合反应,则Y的化学式为_________,Z的电子式为_________;Y、Z两种物质相比,相同的化学键类型为__________,当由X制取Z的上述两种途径生成Z的量相等时,转移电子数目比为________。
(2)若X、Y、Z三种均为常见化合物且三种物质中均含有相同的两种短周期元素,0.1 mol/L的三种物质的溶液pH:Y>X>Z>7,则①的化学方程式为___________________,③的离子方程式为__________________。
(3)若X、Y、Z三种物质均含有同一种金属元素,X是单质,Y是日常生活中最重要的盐,②的反应条件为电解,则②的化学方程式为_________________,③的离子方程式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】镁和铝的碱式碳酸盐是中和胃酸药物的主要成分。欲测定某种镁和铝的碱式碳酸盐的成分进行了以下实验,根据以下实验记录,回答下列问题:
(1)称取6.02g该碱式碳酸盐,加入4.0mol/L盐酸使其溶解,当加入42.5mL时开始产生CO2,当加入盐酸至45.0mL时恰好完全溶解,该碱式碳酸盐中OH-与CO32- 的物质的量之比n(OH-)︰n(CO32-)=__________;
(2)在上述碱式碳酸盐恰好完全溶解所得溶液中加入过量的NaOH溶液,过滤,干燥(不分解)后得3.48g沉淀物。若该碱式碳酸盐中镁元素与氢元素的质量分数之比为6:1,试计算确定该碱式碳酸盐的化学式 __________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com