
科目: 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,其一种生产工艺如下:
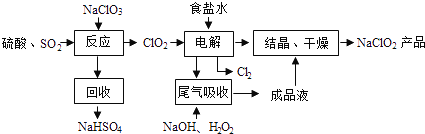
回答下列问题:
(1)NaClO2中Cl的化合价为__________价。
(2)写出“反应”步骤中生成ClO2的化学方程式___________________。
(3)“电解”中阴极反应的主要产物是_________________。
(4)“尾气吸收”是吸收“电解”过程排出的少量ClO2,此吸收反应中,氧化剂与还原剂的物质的量之比为_________, 该反应中氧化产物是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知某有机物A:
①由C、H、O三种元素组成,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%;
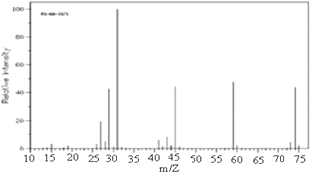
②如图是该有机物的质谱图
③A的红外光谱图上有C-H键、O-H键、C-O键的振动吸收峰.
④A的核磁共振氢谱有两个峰.请回答:
(1)A的实验式(最简式)为_____________,分子式为_____________;
(2)已知A的最简式能否确定A的分子式(填“能”或“不能”)_______,为什么?________;
查看答案和解析>>
科目: 来源: 题型:
【题目】H2O2在工业、农业、医药上都有广泛的用途.
(1)H2O2是二元弱酸,写出第一步的电离方程式__,第二步的电离平衡常数表达式Ka2=_________.
(2)许多物质都可以做H2O2分解的催化剂.一种观点认为:在反应过程中催化剂先被H2O2氧化(或还原),后又被H2O2还原(或氧化).下列物质都可做H2O2分解的催化剂,在反应过程中先被氧化,后被还原的是________.
①I - ②Fe3+ ③Cu2+ ④Fe2+
(3)H2O2是一种环境友好的强氧化剂.电镀废水(主要含Cu2+、Ni2+,还含少量Fe3+、Fe2+、Cr3+等)制备硫酸镍的一种流程如下:
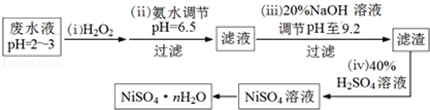
①第(ⅰ)步,加入H2O2反应的离子方程式_________________.
②为测定NiSO4nH2O的组成,进行如下实验:称取2.627g样品,配制成250.00mL溶液.准确量取配制的溶液25.00mL,用0.04000molL﹣1的EDTA(Na2H2Y)标准溶液滴定Ni2+(离子方程式为Ni2++H2Y2﹣=NiY2﹣+2H+),消耗EDTA标准溶液25.00mL.则硫酸镍晶体的化学式为__________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
(1)该浓盐酸中HCl的物质的量浓度为______molL-1。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是______。
A.溶液中HCl的物质的量 B.溶液的浓度 C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.400molL-1的稀盐酸。
①该学生需要量取______mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”、填B表示“偏小”、填C表示“无影响”)。
a.用量筒量取浓盐酸时俯视观察凹液面______。
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水______。
(4)假设该同学成功配制了0.400molL-1的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取______mL盐酸。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子,能在溶液中大量共存的是
A. H+ 、Ca2+ 、Cl—、CO3— B. Na+ 、Mg2+、SO42—、OH-
C. K+ 、Na+ 、OH-、Cl— D. Cu2+ 、Ba2+、Cl—、SO42—
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D都是中学化学中常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转换关系 (部分反应中得水已忽略)

(1)若A为氯碱工业的产品,C为厨房中的用品。
①反应Ⅰ的离子方程式为____________________________________________;
②氯碱工业制备A的化学方程式是__________________________________________________。
(2)若A、D均为单质,且A为气体,D元素的一种红棕色氧化物常用作颜料。
①B溶液可净水的原因是____________________________________________;
②A的实验制法的化学方程式____________________________________________。
(3)若B是一种两性氢氧化物,请写出反应Ⅲ的离子方程式____________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ、选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.加热分解 C.结晶法 D.分液法 E.渗析法 F.蒸馏法 G.过滤法
(1)___________分离水和煤油的混合物。
(2)___________分离水和酒精。
(3)___________分离溴水中的溴和水。
Ⅱ、欲用98%的浓硫酸(g=1.84g/cm3)配制浓度为0.5mol/L的稀硫酸480ml。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥托盘天平⑦药匙。
请回答下列问题:
(4)上述仪器中,在配制稀H2SO4时不需要使用的有___________(填代号),还缺少的仪器是______________________;
(5)经计算,需浓H2SO4的体积为___________;如果实验室有15mL、20mL、50mL的量筒应选用_______mL的量筒最好,量取时俯视量筒读数将使浓度__________(“偏高”、“偏低”、“无影响”);
(6)将浓硫酸沿烧杯内壁慢慢注入盛水的烧杯中,并用玻璃棒不断搅拌的目的是____________,若未冷却至室温便将溶液转移至容量瓶会使浓度偏________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关说法中正确的是( )
A. 已知25 ℃时NH4CN溶液显碱性,则25 ℃时的电离常数K(NH3·H2O)>K(HCN)
B. 室温时, 相同体积、相同pH的盐酸和醋酸溶液中由水电离出的c(H+):盐酸小于醋酸溶液
C. 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向含有Cl-、CrO42-且浓度均为0.010 mol·L-1溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时, CrO42-先产生沉淀
D. 常温下pH=7的CH3COOH和NaOH混合溶液中,c(Na+)>c(CH3COO-)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知乙烯和丙烯的混合物的质量为m g,NA代表阿伏加德罗常数,则该混合物
A. 所含共用电子对数目为(![]() +1)NA B. 所含碳氢键数目为
+1)NA B. 所含碳氢键数目为![]() NA
NA
C. 燃烧时消耗的O2一定是![]() L D. 所含原子总数为
L D. 所含原子总数为![]() NA
NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com