
科目: 来源: 题型:
【题目】关于钠元素的单质及其化合物的叙述不正确的是( )
A. 钠是银白色金属,质软,熔点相对较低,密度比水小
B. Na2O2中阴阳离子个数比为1∶1
C. 金属钠在空气中长期放置,最终变为碳酸钠
D. Na2O和Na2O2都能由金属钠和氧气化合生成,但Na2O和Na2O2中O的价态不同
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A.SO2、CO2、SiO2中的S、C、Si均为sp3杂化
B.H3O+、NH4+、[Cu(NH3)4]2+均含有配位键
C.SO32—、CO32—、SiO32—均为平面三角形
D.石墨、新型高分子导电材料、聚乙烯、金属晶体均含有金属键
查看答案和解析>>
科目: 来源: 题型:
【题目】原子序数依次增大的四种短周期主族元素A、B、C、D,A元素的一种同位素原子核内无中子;B元素形成的化合物种类最多;C、D元素同主族且最外层电子数为偶数。下列叙述正确的是
A. A元素的各同位素形成的双原子分子A2最多有3种
B. 化合物BC2的电子式为 ![]()
C. B、C、D三种元素的非金属性强弱顺序为C>D>B
D. 化合物A2C的沸点高于A2D是因为C—A键比D—A键稳定
查看答案和解析>>
科目: 来源: 题型:
【题目】阿伏加德罗常数的值为![]() 。下列说法正确的是
。下列说法正确的是
A. 1L0.1mol·![]() NH4Cl溶液中,
NH4Cl溶液中, ![]() 的数量为0.1
的数量为0.1![]()
B. 2.4gMg与H2SO4完全反应,转移的电子数为0.1![]()
C. 标准状况下,2.24LN2和O2的混合气体中分子数为0.2![]()
D. 0.1mol H2和0.1mol I2于密闭容器中充分反应后,其分子总数为0.2![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】已知有以下物质相互转化:
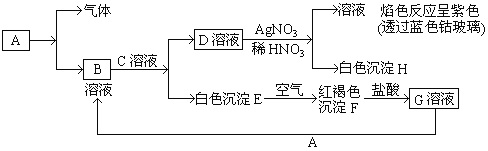
试回答
(1)写出C的化学式____________;
(2)A与水蒸气反应方程式为:__________________________ ;
(3)写出由E转变成F的化学方程式_______________________;
(4)鉴别G溶液中阳离子的方法是:____________________,现象为:________;用G溶液可以腐蚀铜印刷电路板,离子反应方程式为___________________________;
(5)金属铝与A的氧化物可用来焊接火车铁轨,实验室中该反应所需药品有_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上用净化后的水煤气在催化剂作用下,与水蒸气发生反应制取氢气,化学方程式为CO(g)+H2O(g) ![]() H2(g)+CO2(g)。一定条件下,将4 mol CO与2 mol H2O(g)充入体积为2 L的密闭容器中,体系中各物质的浓度随时间的变化如图所示:
H2(g)+CO2(g)。一定条件下,将4 mol CO与2 mol H2O(g)充入体积为2 L的密闭容器中,体系中各物质的浓度随时间的变化如图所示:
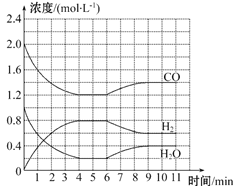
(1)在0~4 min时段,反应速率v(H2O)为_______mol·L-1·min-1,该条件下反应的平衡常数K为______(保留两位有效数字)。
(2)该反应到4 min时,CO的转化率为________。
(3)若6 min时改变的外部条件为升温,则该反应的ΔH________0(填“>”“=”或“<”),此时反应的平衡常数________(填“增大”“减小”或“不变”)。
(4)判断该反应达到化学平衡状态的依据是________。
a.混合气体的密度不变 b.混合气体中c(CO)不变
c.v(H2O)正=v(H2)逆 d.断裂2 mol H—O键的同时生成1 mol H—H键
(5)若保持与4 min时相同的温度,向一容积可变的密闭容器中同时充入0.5 mol CO、1.5 mol H2O(g)、0.5 mol CO2和a mol H2,则当a=2.5时,上述反应向________(填“正反应”或“逆反应”)方向进行。若要使上述反应开始时向逆反应方向进行,则a的取值范围为___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下:
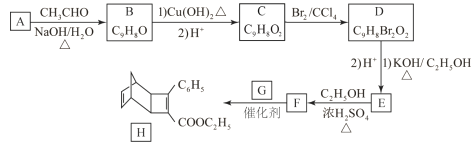
已知:①RCHO+CH3CHO![]() RCH=CHCHO+H2O
RCH=CHCHO+H2O
②![]()
回答下列问题:
(1)A的化学名称为为__________。
(2)由C生成D的反应类型为__________。
(3)E的结构简式为______________________________。
(4)写出用环戊烷和2-丁炔为原料制备化合物 的合成路线 (其他试剂任选)。______ 。
的合成路线 (其他试剂任选)。______ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室中可用如下反应制取氯气:2KMnO4+16HCl(浓)= 2KCl+2MnCl2+5Cl2↑+8H2O,此反应中氧化剂与还原剂的物质的量之比为( )
A.1:8B.1:5C.2:5D.5:1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A.IA族和ⅦA族原子化合时,一定生成离子键
B.具有共价键的化合物就是共价化合物
C.由非金属元素形成的化合物一定是共价化合物
D.离子化合物中一定有离子键
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D、E、F 六种短周期元素,已知相邻的A、B、C、D四种元素原子核外共有56个电子,在周期表中的位置如图所示。E的单质可与酸反应,1molE单质与足量酸作用,在标准状况下能产生33.6 L H2,E的阳离子与A的阴离子核外电子层结构完全相同,F原子半径在短周期元素中最大,回答下列问题:
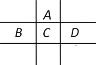
(1)元素的名称:B_____________;
(2)画出C离子的结构示意图:______________;
(3)写出D元素在周期表中的位置:__________;D元素的单质可用于制漂白液和漂白粉,写出制漂白液的离子方程式:____________,漂白粉的有效成分是______________;
(4)B的同族上一周期元素的氢化物为__________(化学式) ,实验室制取该物质的方程式为_________,制取该气体时用______________做干燥剂。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com