
科目: 来源: 题型:
【题目】已知:A.金刚石、B.MgF2、C.NH4Cl、D.NaNO3、E.干冰、F.固体碘,填写下列空白。(用序号填写)
(1)熔化时不需破坏化学键的是________,熔化时只需破坏共价键的是________,熔点最低的是________,
晶体中既存在离子键又存在共价键的是________。
(2)意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1 mol N—N键吸收167 kJ热量,生成1 mol N≡N键放出942 kJ热量。根据以上信息和数据,则1 mol N4生成N2的ΔH=______ kJ·mol-1

(3) 50 mL 0.50 mol/L的盐酸与50 mL 0.55 mol/L的NaOH溶液在如图所示的装置中进行中和反应。

请回答下列问题:
从实验装置上看,图中尚缺少的一种玻璃仪器是_____,烧杯间填满碎泡沫塑料的作用是______。大烧杯上如不盖硬纸板,则求得的中和热数值_______(填“偏大”、“偏小”或“无影响”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组的同学用如图所示装置研究有关电化学的问题。当闭合该装 置的开关时,观察到电流表的指针发生了偏转。
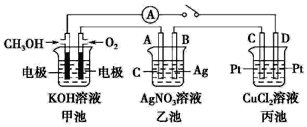
请回答下列问题:
(1)甲池为原电池,通入 CH3OH 电极的电极反应为________。
(2)乙池中A(石墨)电极的名称为_____(填“正极”“负极”或“阴极”“阳极”),总反应为_____。
(3)当乙池B极质量增加 5.4 g 时,甲池中理论上消耗 O2 的体积为_____mL(标准状况),丙池D极析出_____g 铜。
查看答案和解析>>
科目: 来源: 题型:
【题目】按照物质的树状分类和交叉分类,HNO3应属于
①酸 ②氧化物 ③含氧酸 ④一元酸 ⑤电解质 ⑥混合物 ⑦无机化合物
A.①③④⑤⑦B.①②③④⑤⑦
C.①②③④⑥D.①④⑥⑦
查看答案和解析>>
科目: 来源: 题型:
【题目】对于下图所示实验,下列实验现象预测或操作正确的是
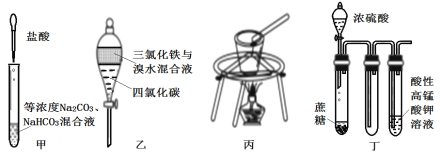
A. 实验甲:匀速逐滴滴加盐酸时,试管中没气泡产生和有气泡产生的时间段相同
B. 实验乙:充分振荡后静置,下层溶液为橙红色,上层为无色
C. 实验丙:将MgCl26H2O置于坩埚中加热以制备无水MgCl2
D. 装置丁:酸性KMnO4溶液中有气泡出现,且溶液颜色会逐渐变浅乃至褪去
查看答案和解析>>
科目: 来源: 题型:
【题目】明代《天工开物》记载“火法”冶炼锌:“炉甘石十斤,装载入一泥罐内,……然后逐层用煤炭饼垫盛,其底辅薪,发火煅红,……冷淀,毁罐取出,……即倭铅也”(注:炉甘石的主要成分为碳酸锌,泥罐中掺有煤炭)。下列说法不正确的是
A. 倭铅就是金属锌
B. 该冶炼锌的方法属于热还原法,煤炭中起作用的主要成分是C
C. 冶炼Zn的反应方程式为ZnCO3+2C![]() Zn+3CO↑
Zn+3CO↑
D. 能用类似于此方法冶炼的金属有:Mg、Fe、Cu
查看答案和解析>>
科目: 来源: 题型:
【题目】温度为T℃时,向2.0 L恒容密闭容器中充入2.08 mol PCl5,反应PCl5(g) ![]() PCl3(g) + Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
PCl3(g) + Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表:
t / s | 0 | 50 | 150 | 250 | 350 |
n(PCl3) / mol | 0 | 0. 56 | 0. 75 | 0. 80 | 0. 80 |
回答下列问题:
(1)反应在前50 s 的平均速率v(PCl3)= _______mol/( L·s) 。
(2)T℃时,起始时向容器中充入1. 2 mol PCl5、0. 40 mol PCl3 和0. 20 mol Cl2,反应达到平衡前v(正)__________(选填“>”、“=”或“ <”)v(逆) 。
(3)T℃时,若起始时向容器中充入6. 0 mol PCl3 和6. 0 mol Cl2,达到平衡时,平衡混合气体中PCl5的体积分数为多少?(写出解题过程)。_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】溴化钙可用作阻燃剂、制冷剂,具有易溶于水、易吸潮等性质。实验室用工业大理石(含有少量Al3+、Fe3+等杂质)制备溴化钙的主要流程如下:
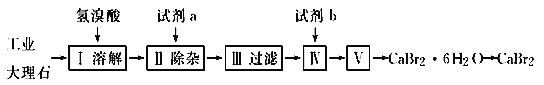
完成下列填空:
(1)上述使用的氢溴酸的质量分数为26%,若用47%的氢溴酸配置26%的氢溴酸500 mL,所需的玻璃仪器有玻璃棒、________________________。
(2)已知步骤Ⅲ的滤液中不含NH4+。步骤Ⅱ加入的试剂a是__________,控制溶液的pH约为8.0的目的是________________________。
(3)试剂b是__________,步骤Ⅳ的目的是________________________________。
(4)步骤Ⅴ所含的操作依次是____________________。
(5)制得的溴化钙可以通过如下步骤测定其纯度:①称取4.00 g无水溴化钙样品;②溶解;③滴入足量Na2CO3溶液,充分反应后过滤;④__________;⑤称量。若得到1.88 g碳酸钙,则溴化钙的质量分数为__________(保留两位有效数字)。若实验操作规范而测定结果偏低,其原因是_______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com