
科目: 来源: 题型:
【题目】已知A为淡黄色固体,R是地壳中含量最多的金属元素的单质,T为生活中 使用最广泛的金属单质,D是具有磁性的黑色晶体,C、F是无色无味的气体,H是白色沉淀。
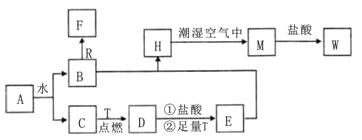
(1)物质A的化学式为 ________,F化学式为 ________;
(2)B和R在溶液中反应生成F的离子方程式为__________________________;
(3)H在潮湿空气中变成M的实验现象是________,化学方程式为______________;
(4)A和水反应生成B和C的化学方程式为__________________________
(5)印刷行业刻制印刷电路板(含有铜箔)时,要用W溶液中作为“腐蚀液”,写出该反应的离子方程式______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】K2Cr2O7溶液中存在平衡:Cr2O72-(橙色)+H2O![]() 2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是
2CrO42-(黄色)+2H+。用K2Cr2O7溶液进行下列实验:结合实验,下列说法不正确的是

A. ①中溶液橙色加深,③中溶液变黄
B. ②中Cr2O72-被C2H5OH还原
C. 对比②和④可知K2Cr2O7酸性溶液氧化性强
D. 若向④中加入70%H2SO4溶液至过量,溶液变为橙色
查看答案和解析>>
科目: 来源: 题型:
【题目】化合物M是一种合成药品的中间体,其合成路线如图所示。
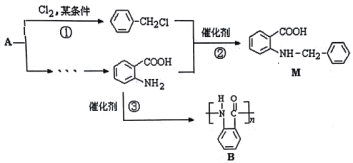
已知: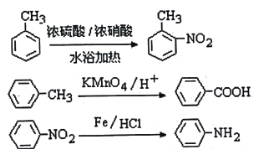
(弱碱性,易被氧化)
(1)写出反应①的化学方程式_____________。
(2)反应②属于____反应(填有机反应类型)。
(3)写出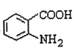 中官能团的名称__________。
中官能团的名称__________。
(4)H为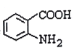 的同分异构体,则满足下列条件的H的同分异构体共有______种,其中满足下列条件且含4种不同氢原子的同分异构体的结构简式是___________。
的同分异构体,则满足下列条件的H的同分异构体共有______种,其中满足下列条件且含4种不同氢原子的同分异构体的结构简式是___________。
①显弱碱性,易被氧化 ②分子内含有苯环 ③能发生水解反应
(5)请你设计由A合成B的合成路线_________________________________________________________。
提示:①合成过程中无机试剂任选; ②合成路线表示方法示例如图所示。
![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】高温下,超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为-2价。如图所示为超氧化钾晶体的一个晶胞,则下列说法正确的是

A.超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2-
B.晶体中每个K+周围有8个O2-,每个O2-周围有8个K+
C.晶体中与每个K+距离最近的K+有8个
D.晶体中与每个K+距离最近的K+有6个
查看答案和解析>>
科目: 来源: 题型:
【题目】下面的排序不正确的是
A. 酸性由大到小:HPO3>H3PO4>H3PO3 B. 硬度由大到小:金刚石>碳化硅>晶体硅
C. 熔点由高到低:Na>Mg>Al D. 晶格能由大到小:NaF>NaCl>NaBr>NaI
查看答案和解析>>
科目: 来源: 题型:
【题目】亚硝酸钠广泛用于印染漂白、食品等行业,常作媒染剂、漂白剂、食品添加剂等。某兴趣小组用下列装證制备NaNO2。
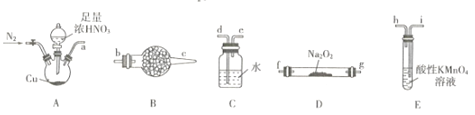
已知:①2NO+Na2O2=2NaNO2; ②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+。
请回答下列问题:
(1)利用上图中的装置制备NaNO2,其连接顺序为a→__________(按气流方向,用小写字母表示)。
(2)实验开始时,先通一段时间N2的目的是__________。
(3)装置B中盛放试剂的名称为____,装置C的作用是_______。
(4)装置E中发生反应的离子方程式为_____________。
(5)为测定亚硝酸钠的含量,称取3.000g样品溶于水配成500mL.溶液,量取25.00mL溶液于锥形瓶中,硫酸酸化后加入过量KI,发生反应:2NO2-+2I-+4H+=2NO↑+I2+2H2O(杂质不参与反应)。然后用0.1000mol/LNa2S2O3标准溶液滴定至终点(发生反应:I2+2S2O32-=S4O62-+2I-),消耗20.00mL。
①该实验可选用的指示剂为_____,达到滴定终点时的现象是__________。
②所得样品中亚硝酸钠的质量分数为____________。
③下列操作会导致测定结果偏高的是_______(填代号)。
a.滴定过程中向锥形瓶中加少量水
b.消定前滴定管尖嘴部分有气泡,滴定后气泡消失
c.读数时,滴定前仰视,滴定后府视
d.滴定时,标准被滴到锥形瓶外
查看答案和解析>>
科目: 来源: 题型:
【题目】已知硼与铝的性质相似,能与氧气、氢氧化钠溶液等物质反应,硼与氯气反应生成三氯化硼(BC13),生成的三氯化硼遇水水解产生白雾(已知:BC13的熔点为 -107. 3℃,沸点为12.5 ℃)。某兴趣小组设计如图所示装置制备三氯化硼。
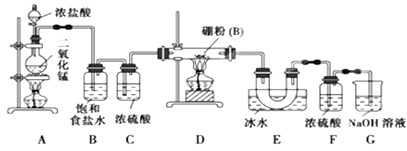
回答下列问题:
(1)写出装置A中发生反应的离子方程式________________。
(2)写出装置D中发生反应的化学方程式为_____________________。
(3)装置B、E的作用分别是________________、________________。
(4)可以用盛装____________(填试剂名称)的干燥管代替装置F和G,使实验更简便。
(5)为了顺利完成实验,点燃酒精灯的正确操作是______(填字母),
a.先点燃A处酒精灯,后点燃D处酒精灯
b.先点燃D处酒精灯,后点燃A处酒精灯
c.同时点燃A、D两处酒精灯
其理由是______________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】钴的氧化物广泛应用于磁性材料及超导材料等领域。一种利用含钴废料(主要成分Co2O3,含少量Al2O3、MgO、SiO2等)制备Co2O3的工艺流程如下图所示。
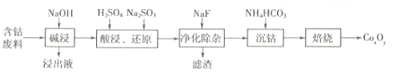
(1)“浸出液”的主要成分是________(写化学式)。
(2)“酸浸,还原”过程中溶解Co2O3的离子方程式为______________。稀硫酸和Na2SO3也可用盐酸替代,工业生产中不用盐酸的理由是_____________。
(3)NaF的作用是____________。
(4)“沉钴”时生成CoCO3的化学方程式为___________。检验CoCO3是否洗涤干净的操作方法是_______________。
(5)在空气中焙烧CoCO3生成CoxOy和CO2,测得充分煅烧后固体质量为4.82g,CO2的体积为1.344L(标准状况),则CoxOy的化学式为_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室利用如下图所示装置制取无水氯化铁和无水氯化亚铁。

已知:炽热铁屑
回答下列问题:
I制取无水氯化铁。
(1)盛装浓盐酸的仪器a的名称为_____。装置A中反应的离子方程式为_______________。装置B中加入的试剂是__________。
(2)制取的无水氯化铁中混有少量氯化亚铁,为防止生成氯化亚铁,其改进的措施为___________。
II制取无水氯化亚铁。
(3)装置A用来制取HCl,尾气的成分是____,用D装置进行尾气处理,存在的问题是________________。
(4)欲制得纯净的FeC12,在实验操作中应先点燃____(填“A”或“B”)处酒精灯。验证制得的FeC12是否含有FeC13,常用的试剂是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中错误的是
A. 邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低
B. 水加热到很高温度都难分解是因水分子间存在氢键
C. ①CH4、NH4+ ②H2S、HCl ③CO2、N2O ④CO32-、NO3-以上各组微粒中不属于等电子体的是②
D. BrCH2CHOHCH2OH存在手性异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com