
科目: 来源: 题型:
【题目】铝和铁是日常生活中两种常见的金属,铝和铁的化合物是中学化学中常见的基础物质。请回答下列有关问题:
(1)氧化铝是一种_____氧化物(填“酸性”“碱性”或“两性”);
(2)实验室制备氢氧化铝时,最好向铝盐溶液中加入_____。(填“氨水”或“氢氧化钠溶液”);
(3)还原铁粉与水蒸气反应的化学方程式为3Fe+4H2O(g) ![]() X+4H2,试推测X的化学式为_____。
X+4H2,试推测X的化学式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下面图1是生物体细胞内部分有机化合物的概念图,请回答问题:
 图1
图1
(1)小麦种子中的储能物质c是_________,人和动物细胞中的储能物质c是__________。
(2)两个氨基酸发生脱水缩合反应时,产物是________和_________,图2方框内的结构简式是_________。
 图2
图2
(3)b结构的多样性决定其功能的多样性,如作为结构物质、免疫物质、__________、________、调节物质等。
(4)在小麦叶肉细胞中,e主要存在于___________中,可用________将其染色。
(5)d中__________具有生命调节作用。
查看答案和解析>>
科目: 来源: 题型:
【题目】某工厂废水中含游离态氯,通过下列实验测定其浓度。
①取水样10.00mL于锥形瓶中,加入10.00mL的KI溶液(足量),发生的反应为:Cl2+2KI=2KCl+I2,滴入指示剂2~3滴。
②取一滴定管依次用自来水、蒸馏水洗净后,马上注入0.01mol/L溶液,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+2Na2S4O6。
试回答下列问题:
(1)步骤①加入的指示剂是_____________。
(2)步骤②应使用______式滴定管。
(3)判断达到滴定终点的实验现象是_____________。
(4)用0.1032mol/LHCl溶液滴定未知浓度的NaOH溶液,下列情况对实验结果无影响的是___(填标号)。
A.酸式滴定管未用标准盐酸溶液润洗
B.锥形瓶未用待测液润洗
C.滴定滴定管尖嘴中有气泡,滴定后气泡消失了
D.滴定时将标准液溅出锥形瓶外
查看答案和解析>>
科目: 来源: 题型:
【题目】有下列三组液体:①75%的乙醇溶液;②氯化钠溶液和四氯化碳组成的混合液;③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A.分液、萃取、蒸馏B.蒸馏、分液、结晶
C.分液、结晶、萃取D.蒸馏、分液、萃取
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:
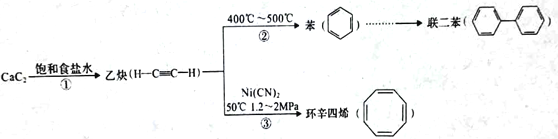
(1)反应①类似盐的水解,写出CaC2的电子式_________。
(2)苯是由哪位科学家首先发现的________,苯分子中有三个氢原子被-Br、-Br、-OH取代得到的芳香族化合物有_____种。将苯分子中的一个碳原子换成一个氮原子,得到一种类似苯环结构的稳定有机物,则此有机物的相对分子质量为________。
(3)写出反应③的化学反应方程式并注明反应类型__________。
(4)联二苯的化学式为__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(15分)ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。

(1)仪器D的名称是 。安装F中导管时,应选用图2中的 。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。
为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜 (填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是 。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为 ,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是 。
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是 ,原因是 。

查看答案和解析>>
科目: 来源: 题型:
【题目】废旧印刷电路板是一种电子废弃物,其中铜的含量达到矿石中的几十倍。湿法技术是将粉碎的印刷电路板经溶解、萃取、电解等操作得到纯铜等产品。某化学小组模拟该方法回收铜和制取胆矾,流程简图如下:

回答下列问题:
(1)反应Ⅰ是将Cu转化为Cu(NH3)42+,反应中H2O2的作用是____________。写出操作①的名称:________。
(2)反应Ⅱ是铜氨溶液中的Cu(NH3)42+与有机物RH反应,写出该反应的离子方程式:__________________________________________。操作②用到的主要仪器名称为______________,其目的是(填序号)________。
a.富集铜元素
b.使铜元素与水溶液中的物质分离
c.增加Cu2+在水中的溶解度
(3)反应Ⅲ是有机溶液中的CuR2与稀硫酸反应生成CuSO4和________。若操作③使用如图装置,图中存在的错误是__________________________________________。

(4)操作④以石墨作电极电解CuSO4溶液。阴极析出铜,阳极产物是________________。 流程中有三处实现了试剂的循环使用,已用虚线标出两处,第三处的试剂是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】FeCl3 具有净水作用,但腐蚀设备,而聚合氯化铁是一种新型的絮凝剂,处理污水比FeCl3 高效,且腐蚀性小。请回答下列问题:
(1)FeCl3 净水的原理是__________________________________________________。FeCl3 溶液腐蚀钢铁设备,除H+作用外,另一主要原因是(用离子方程式表示)______________________________。
(2)为节约成本,工业上用NaClO3氧化酸性FeCl2废液得到FeCl3。
①若酸性FeCl2废液中c(Fe2+)=2.0×10-2 mol·L-1, c(Fe3+)=1.0×10-3 mol·L-1,c(Cl-)=5.3×10-2 mol·L-1,则该溶液的pH约为________。
②完成NaClO3氧化FeCl2的离子方程式:
![]() ClO3-+
ClO3-+![]() Fe2++________===
Fe2++________===![]() Cl-+
Cl-+![]() Fe3++
Fe3++![]() ________,______________
________,______________
(3)FeCl3在溶液中分三步水解:
Fe3++H2O ![]() Fe(OH)2++H+ K1
Fe(OH)2++H+ K1
Fe(OH)2++H2O![]() Fe(OH)2++H+ K2
Fe(OH)2++H+ K2
Fe(OH)2++H2O![]() Fe(OH)3+H+ K3
Fe(OH)3+H+ K3
以上水解反应的平衡常数K1、K2、K3由大到小的顺序是________________。
通过控制条件,以上水解产物聚合,生成聚合氯化铁,离子方程式为xFe3++yH2O![]() Fex(OH)
Fex(OH)![]() +yH+,欲使平衡正向移动可采用的方法是(填序号)________。
+yH+,欲使平衡正向移动可采用的方法是(填序号)________。
a.降温 b.加水稀释
c.加入NH4Cl d.加入NaHCO3
(4)天津某污水处理厂用聚合氯化铁净化污水的结果如图所示。由图中数据得出每升污水中投放聚合氯化铁[以Fe(mg·L-1)表示]的最佳范围约为________mg·L-1。

查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。回答下列问题:
(1)四种元素中电负性最大的是________(填元素符号),其中C原子的核外电子排布式为__________________。
(2)单质A有两种同素异形体,其中沸点高的是______(填分子式),原因是__________________________________________;A和B的氢化物所属的晶体类型分别为________和________。
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为______________,中心原子的杂化轨道类型为________。
(4)化合物D2A的立体构型为________,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为_______________________________________________。
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566 nm,F的化学式为________;晶体F的密度(g·cm-3 )________________________________。(列出表达式)
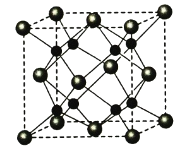
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com