
科目: 来源: 题型:
【题目】下列各组溶液,能在强酸性或强碱性中都能大量共存且无色的离子组是
A. Cu2+、K+、CO32-、NH4+ B. Ba2-、Na+、SO42-、NO3-
C. Na+、H+、HCO3-、Cl- D. K+、Na+、NO3-、SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】根据离子反应发生的条件,判断下列各组物质中不能发生离子反应的是
A.H2SO4溶液与BaCl2溶液B.NaOH溶液与CuSO4溶液
C.Na2CO3溶液与HNO3溶液D.NaOH溶液与KCl溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】阿伏加德罗常数的值为NA。下列说法正确的是
A. 1g氢气含有NA个H2分子
B. 1mol铁与过量稀盐酸反应生成NA个H2分子
C. 14g由N2与CO组成的混合气体含有的原子数目为0.5 NA
D. 标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1 NA
查看答案和解析>>
科目: 来源: 题型:
【题目】钴(Co)及其化合物在工业上有广泛应用。为从某工业废料中回收钴,某学生设计流程如下(废料中含有Al、Li、Co2O3和Fe2O3等物质).

已知:①物质溶解性:LiF难溶于水,Li2CO3微溶于水;
②部分金属离子形成氢氧化物沉淀的pH见下表.
Fe3+ | Co2+ | Co3+ | Al3+ | |
pH(开始沉淀) | 1.9 | 7.15 | ﹣0.23 | 3.4 |
pH(完全沉淀) | 3.2 | 9.15 | 1.09 | 4.7 |
请回答:
(1)步骤Ⅰ中得到含铝溶液的反应的离子方程式是______.
(2)写出步骤Ⅱ中Co2O3与盐酸反应生成Cl2的离子方程式:______.
(3)步骤Ⅲ中Na2CO3溶液的作用是调节溶液的pH,应使溶液的pH不超过______;废渣中的主要成分除了LiF外,还有______.
(4)NaF与溶液中的Li+形成LiF沉淀,此反应对步骤Ⅳ所起的作用是______.
(5)在空气中加热5.49g草酸钴晶体(CoC2O42H2O)样品,受热过程中不同温度范围内分别得到一种固体物质,其质量如表.
温度范围/℃ | 固体质量/g |
150~210 | 4.41 |
290~320 | 2.41 |
890~920 | 2.25 |
①加热到210℃时,固体质量减轻的原因是______.
②经测定,加热到210~290℃过程中的生成物只有CO2和钴的氧化物,此过程发生反应的化学方程式为:____.
查看答案和解析>>
科目: 来源: 题型:
【题目】物质的类别和核心元素的化合价是研究物质性质的两个重要维度。下图为硫及其部分化合物的“价类二维图”, 根据图示回答下列问题:
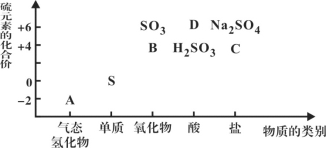
(1)图中A、B、C、D四种物质中,属于非电解质的是__________(用化学式表示)。
(2)足量B通入紫色石蕊试液的现象是______________________________________;
FeCl3溶液(酸性)中通入B的离子方程式为___________________________。
(3)C在反应中既可作氧化剂,又可作还原剂。当它作氧化剂时,理论上其可被还原为____(填标号)。
A.Na2S B.S C.H2SO3 D.Na2SO4 E.H2SO4
(4)从硫元素化合价分析,硫单质具有氧化性和还原性。请举一例说明其具有氧化性(用化学方程式表示)_______________________________。
(5)将A与SO2混合,可生成淡黄色固体。该反应的氧化产物与还原产物的质量之比为__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某温度下,在固定容积的密闭容器中,可逆反应A(g)+3B(g)![]() 2C(g)达到平衡时,各物质的物质的量之比是n(A)∶n(B) ∶n(C)=2∶2∶l。保持温度不变,以2∶2∶1的物质的量之比再充入A,B,C,则( )
2C(g)达到平衡时,各物质的物质的量之比是n(A)∶n(B) ∶n(C)=2∶2∶l。保持温度不变,以2∶2∶1的物质的量之比再充入A,B,C,则( )
A. 平衡向正方向移动 B. 平衡不发生移动
C. C的体积分数减小 D. C的体积分数不变
查看答案和解析>>
科目: 来源: 题型:
【题目】氨与硝酸都是氮的重要化合物,在工农业生产中有广泛应用。回答下列问题:
(1)氨气的制备

①氨气制取的发生装置可以选择上图中的_________(填字母),反应的化学方程式为____________________。
②选择上图装置组装一套实验装置来收集一瓶干燥的氨气,所选装置的连接顺序为:发生装置→______→______,______→_____→i(按气流方向,用小写英文字母表示)。
③可用如装置进行氨的喷泉实验,引发喷泉的操作是__________。

(2)如图所示,NH3经一系列反应可以得到HNO3。

①反应①的化学方程式为________________________________________。
②产物NO是大气污染物之一。在400℃左右且有催化剂存在的情况下,可用氨将一氧化氮还原为无色无毒气体。该反应的化学方程式为_______________________。
(3)在某100mL硝酸与硫酸的混合液中,HNO3和H2SO4的物质的量浓度分别为0.6 mol·L-1和0.3mol·L-1。向该混合液中加入3.84g铜粉,加热,待充分反应后,所得溶液中的Cu2+的物质的量浓度是多少____________?(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】水溶液中只可能有K+、Mg2+、AlO2﹣、SiO32﹣、CO32﹣、SO42﹣中的若干种离子.某同学对溶液进行了如图实验:下列判断错误的是( )

A. 有气体甲生成,表明溶液X中一定含有CO32﹣
B. 沉淀甲可能是硅酸镁
C. K+一定存在于溶液X中
D. 不能确定SO42﹣是否存在于溶液X中
查看答案和解析>>
科目: 来源: 题型:
【题目】在一固定容积的密闭容器中充入气体A和B,发生如下可逆反应:A(g) +B(g)![]() xC(g);△H = Q。在不同的温度和压强下,C在反应混合物中的含量随反应时间的变化如图所示。下列判断正确的是
xC(g);△H = Q。在不同的温度和压强下,C在反应混合物中的含量随反应时间的变化如图所示。下列判断正确的是
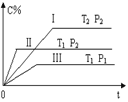
A. P1>P2,x=1 B. P1<P2,x≠1
C. T1<T2,Q>0 D. T1>T2,Q<0
查看答案和解析>>
科目: 来源: 题型:
【题目】制备纳米Fe3O4的过程如图所示:下列有关叙述不合理的是 ( )
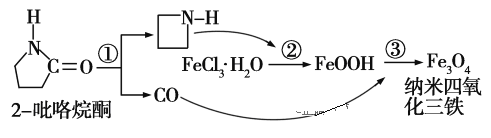
A. 反应①的反应类型为消去反应
B. 纳米Fe3O4分散在适当溶剂中,当强光照射时,会产生丁达尔现象
C. 反应②中,环丙胺的作用可能是促进氯化铁水解
D. 反应③的化学方程式为:6FeOOH+CO===2Fe3O4+3H2O+CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com