
科目: 来源: 题型:
【题目】氮化锂是一种优良的贮氢材料,它是一种紫色或红色的晶状固体,在空气中长期暴露,最终会变成碳酸锂。氮化锂易水解生成氢氧化锂和氨气,在空气中加热能剧烈燃烧,特别是细粉末状的氮化锂;锂与氨反应生成LiNH2和H2。实验室用干燥、纯净的N2与金属锂(密度为0.534g·cm3)反应制取氮化锂。某课题组拟选择下列装置完成实验(装置可重复使用):

回答下列问题:
(1)若实验室用生石灰与浓氨水混合制备少量氨气,气流从左至右,选择上述装置制备少量氮化锂。装置连接顺序为__________________________________________。
(2)E装置的作用是_____________________________;写出D中化学方程式为______________________________。
(3)实验步骤如下:①装药品②引发反应产生氨气③检查装置气密性④点燃C处酒精灯⑤点燃D处酒精灯。正确的先后顺序为________________________________。(填序号)
(4)实验室保存锂的方法是______________;写出C中的化学方程式________________________________。氮化锂的电子式为_______________________________________
(5)设计简单实验证明C中产物为氮化锂:___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】I、在一个固定体积的密闭容器中,加入2 mol A和1 mol B,发生反应:2A(g)+B(g)![]() 3C(g)+D(g),达到平衡时,C的浓度为W mol·L-1。若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度(用“大于”“小于”或“等于”表示)。
3C(g)+D(g),达到平衡时,C的浓度为W mol·L-1。若维持容器体积和温度不变,用下列物质作为起始反应物时,经反应达到平衡后C的浓度(用“大于”“小于”或“等于”表示)。
(1)加入1 mol A和1 mol B时,C的平衡浓度_________W mol·L-1。
(2)加入2mol A、1mol B、3mol C、1mol D时,C的平衡浓度_________W mol·L-1。
(3)加入3 mol C和1 mol D时,C的平衡浓度_________W mol·L-1。
II、现有反应:mA(g)+nB(g)![]() pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+n_________p(填“>”“<”或“=”)。(下列空填“增大”“减小”或“不变”,)
(2)若加入B(体积不变),则A的转化率_________。
(3)若升高温度,则平衡时B、C的浓度之比 c(B)/c(C)将_________。
(4)若加入催化剂,平衡时气体混合物的总物质的量_________。
(5)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______,而维持容器内压强不变,充入氖气时,混合物颜色_______(填“变深”“变浅”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】善于归纳元素及其化合物之间的转化关系,对学习元素化合物具有重要意义。现有下列物质:金属铁、钠、镁、氯气、氧气、二氧化硫、二氧化碳、水、NaOH溶液、氨水、HCl溶液、KI溶液、HNO3溶液、FeCl2溶液。根据要求回答问题:
(1)置换反应是中学常见基本反应类型之一。
①写出非金属单质置换出非金属单质的离子方程式______________________。
②写出金属单质置换出非金属单质的化学反应方程式______________________。
(2)“三角转化”是单质及其化合物间常见的转化关系之一。现有如图转化关系:
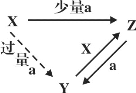
①若X是一种强碱,a是一种酸性氧化物,则Z为_________盐(填“正”或“酸式”)。
②若Z是一种能够与血红蛋白结合造成人体缺氧的气体,则a的名称为___________。
③若X是常见金属单质,a为含氧酸,则Z中金属元素的化合价为___________
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学购买了一瓶“84消毒液”,包装说明如下。请根据说明信息和相关知识

(1)该“84消毒液”中,NaClO的物质的量浓度约为_______ mol/L(保留至小数点后一位)
(2)某化学课外活动小组计划使用NaOH溶液制取消毒液,反应原理为:Cl2+2NaOH=NaCl+ NaClO+H2O。制取时,需要多少升4.0mol/L的NaOH溶液才能与2.24L(标准状况下)的氯气恰好完全反应_________。(简要计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】伪麻黄碱(D)是新康泰克的成分之一,能够缓解感冒时带来的鼻塞、流鼻涕和打喷嚏等症状,其中一种合成路线如下:
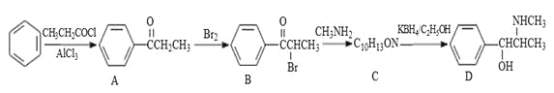
回答下列问题:
(1)伪麻黄碱(D)的分子式为 ;B中含有的官能团有 (写名称)。
(2)写出 B—C反应的化学方程式: 。C—D的反应类型为 。
(3)B的消去产物可以用于合成高分子化合物E,请写出 E的结构简式: 。
(4)满足下列要求的A的同分异构体有 种;
①能发生银镜反应
②苯环上的一氯代物有两种结构,其中核磁共振氢谱为4组峰,且峰面积之比为6:2:1:1的为 (写结构简式)。
(5)已知:![]() 。参照上述合成路线,设计一条由苯和乙酸为起始原料制备
。参照上述合成路线,设计一条由苯和乙酸为起始原料制备![]() 的合成路线: 。
的合成路线: 。
查看答案和解析>>
科目: 来源: 题型:
【题目】氨与硝酸都是氮的重要化合物,在工农业生产中有广泛应用。回答下列问题。
(1)氨气的制备
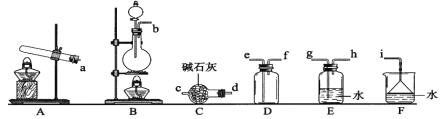

①氨气制取的发生装置可以选择上图中的_________(填字母),反应的化学方程式为__________。
②选择上图装置组装一套实验装置来收集一瓶干燥的氨气,所选装置的连接顺序为:发生装置→______→______,______→_____→i(按气流方向,用小写英文字母表示)。
③可用如右装置进行氨的喷泉实验,引发喷泉的操作是__________。
(2)如图所示,NH3经一系列反应可以得到HNO3。

①反应①的化学方程式为__________________________。
②产物NO是大气污染物之一。在400℃左右且有催化剂存在的情况下,可用氨将一氧化氮还原为无色无毒气体。该反应的化学方程式_______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】电解原理在化学工业中有广泛应用。下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
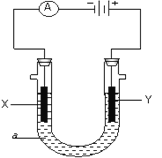
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则可观察到在X极附近观察到的现象是__________电极反应式是________________检验Y电极反应产物的方法是____________________电解一段时间之后溶液的PH将会________(升高、降低或不变),总方程式为_________________________。
(2)若X、Y都是铜电极,a是稀CuSO4溶液,开始实验,X极的电极反应式是__________________________。电解前后CuSO4溶液的浓度___________________(变大、变小或不变)若X电极质量增重64克,则在电路中有_________________mol的电子发生转移。
(3)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则①X电极的材料是_____,电极反应式是_____________。②Y电极的材料是______,电极反应式是____________________。(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com