
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A.用核磁共振氢谱鉴别1-丙醇和2-丙醇
B.![]() 和
和![]() 分子组成相差一个-CH2-,因此是同系物
分子组成相差一个-CH2-,因此是同系物
C.![]() 和
和![]() 均是芳香烃,
均是芳香烃,![]() 既是芳香烃又是芳香化合物
既是芳香烃又是芳香化合物
D.分子式为C3H6有机物最多存在4个C-C单键,与C5H12的碳碳单键数相同
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质中,既能因发生化学反应而使溴水褪色,又能使高锰酸钾酸性溶液褪色的是( )
①CH3CH2CH2CH3 ②CH3CH2CH===CH2

A.①②③④ B.②③④
C.②④ D.只有②
查看答案和解析>>
科目: 来源: 题型:
【题目】下列物质的分类正确的是
碱 | 酸 | 盐 | 碱性氧化物 | 酸性氧化物 | |
A | Na2CO3 | H2SO4 | NaOH | SO2 | CO2 |
B | NaOH | HCl | NaCl | Na2O | CO |
C | NaOH | CH3COOH | CaF2 | CO | SO2 |
D | KOH | HNO3 | CaCO3 | CaO | SO2 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)取3.7g某有机物A在足量氧气中充分燃烧,只生成8.8 gCO2和4.5g H2O,则A中含有的元素为_________________(填元素符号),其实验式为____________。
(2)下图是A的质谱图,则其相对分子质量为 ________ ;分子式为 _________;
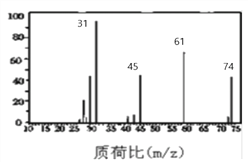
(3)经测定,A在核磁共振氢谱中出现四个峰,吸收峰面积之比为6:1:2:1;A与金属钠反应产生氢气;则A的结构简式为 ____________________________。
(4)A有多种同分异构体,写出与A具有相同官能团的同分异构体的结构简式(任写两种):_________________________,_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】姜黄素有抗氧化、保肝护肝、抑制肿瘤生长等功能。它的结构简式如图所示
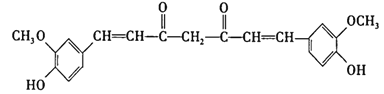
已知: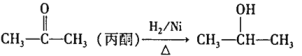
下列有关姜黄素的说法正确的是
A. 姜黄素在一定条件下能发生水解、加成、氧化反应
B. 1个姜黄素分子一定有15个原子共平面
C. 1mol姜黄素在镍(Ni)、加热条件下最多10molH2发生加成反应
D. 姜黄素的分子式为C21H18O6
查看答案和解析>>
科目: 来源: 题型:
【题目】观察下列实验装置图,试回答下列问题:
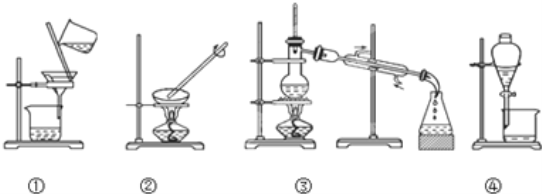
⑴写出图中实验操作对应的名称 ①:_______________ 、 ③:______________ 。
⑵下列实验需要在哪套装置中进行(填序号): a、分离植物油和水: ____________ ; b、从海水中提取蒸馏水: __________ ;
⑶装置①中玻璃棒的作用是__________________________________;
⑷ 实验室需要490mL 0.5molL-1 NaOH溶液,请回答下列问题:
①需称取 ___________g的烧碱固体.
②配制的玻璃仪器除烧杯和玻璃棒、胶头滴管,还需要___________________________。
③下列各项中,可能导致实际浓度偏高的是 _________(填标号).
A.定容时,仰视容量瓶的刻度线
B.NaOH溶解时放出大量的热,未冷却立即配制溶液
C.溶解NaOH固体之后的烧杯未洗涤
D.向容量瓶中转移溶液时不慎洒出
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(主要成分为:Na2Cr2O7·2H2O),其主要工艺流程如下:

查阅相关资料得知:
i.常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下能将Cr3+转化为CrO42-,自身被还原为Bi(OH)3固体。
ii.
物质 | 开始沉淀的pH | 完全沉淀的pH |
Fe(OH)3 | 2.7 | 3.7 |
Al(OH)3 | 3.4 | 4.4 |
Cr(OH)3 | 4.6 | 5.9 |
Fe(OH)2 | 7.5 | 9.7 |
Bi(OH)3 | 0.7 | 4.5 |
回答下列问题:
(1)将铬铁矿矿石粉碎的目的是________________________________________。
(2)操作I、III、IV用到的主要玻璃仪器有玻璃棒和___________(填仪器名称)。
(3)写出④反应的化学方程式_____________________________________________。
(4)⑤中酸化是使CrO42-转化为Cr2O72-![]() 写出该反应的离子方程式______。
写出该反应的离子方程式______。
(5)将溶液H经下列操作:蒸发浓缩,__________,过滤,洗涤,干燥即得红矾钠。
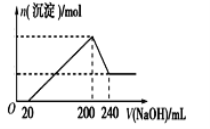
(6)取一定质量的固体D溶解于200 mL的稀硫酸中,向所得溶液中加入5.0 mol/L的NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)关系如图所示,则稀硫酸的浓度为_________,固体D中含Fe化合物的物质的量为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(题文)亚氯酸钠(NaClO2)是重要漂白剂。探究小组开展如下实验,回答下列问题:
实验Ⅰ:制取NaClO2晶体按右图装置进行制取。
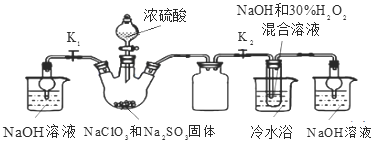
A B C D E
已知:NaClO2饱和溶液在低于38℃时析出NaClO23H2O,38-60℃时析出NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。
(1)用50%双氧水配制30%的H2O2溶液,需要的玻璃仪器除玻璃棒、胶头滴管、烧杯外,还需要_____(填仪器名称);装置C的作用是_____________________。
(2)B中产生ClO2的化学方程式______________________________________。
(3)装置D中反应生成NaClO2的化学方程式为____________________________ 。反应后的溶液中阴离子除了ClO2-、ClO3-、Cl-、ClO-、OH—外还可能含有的一种阴离子是_________,检验该离子的方法是___________________________。
(4)请补充从装置D反应后的溶液中获得NaClO2晶体的操作步骤。
①减压,55℃蒸发结晶;②______________;③______________;④______________;得到成品。
(5)如果撤去D中的冷水浴,可能导致产品中混有的杂质是______________;
实验Ⅱ:样品杂质分析与纯度测定
(6)测定样品中NaClO2的纯度。测定时进行如下实验:
准确称一定质量的样品,加入适量蒸馏水和过量的KI晶体,在酸性条件下发生如下反应:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl-,将所得混合液稀释成100mL待测溶液。
取25.00mL待测溶液,加入淀粉溶液做指示剂,用c mol·L-1 Na2S2O3标准液滴定至终点,测得消耗标准溶液体积的平均值为V mL(已知:I2 +2S2O32-=2I-+S4O62-)。
①确认滴定终点的现象是__________________________________________________。
②所称取的样品中NaClO2的物质的量为______________mol(用含c、V的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图中A为278g/mol。B、D、E、F、G是氧化物且B为红棕色固体,F、K是氢化物,C、H是日常生活中最常见的金属单质,J是黄绿色气体。O是白色沉淀(图中部分反应物和生成物没有列出)。

(1)写出A、G、L的化学式A______________:G: _______________,L:______________。
(2)反应②的化学方程式 ________________________________________________。
(3)写出反应M→L的离子方程式为________________________________________。
(4)若将O敞口久置,变质过程中的现象为___________________________________,发生的化学方程式为__________________________________________________。
(5)向M溶液中投入与M等物质的量的Na2O2,反应的离子方程式是____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】雄黄(As4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
(1)As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体.若As2S3和SnCl2正好完全反应,As2S3和HCl的物质的量之比为________。写出化学方程式并用双线桥法标出电子转移_______________________________________________。
(2)上述反应中的氧化剂是________,反应产生的气体可用________吸收。
(3)As2S3和HNO3有如下反应:As2S3+10H++10NO3-=2H3AsO4+3S+10NO2↑+2H2O
若生成2 mol H3AsO4,则反应中转移电子的物质的量为________。若将该反应设计成一原电池,则NO2应该在________(填“正极”或“负极”)附近逸出。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com