
科目: 来源: 题型:
【题目】按反应特征与产物的结构关系,有机反应大致可分为:取代反应、消去反应、加成反应三种,下列反应中属于加成反应的是
A. C6H5CH2Cl+NaCN ![]() C6H5CH2CN+NaCl
C6H5CH2CN+NaCl
B. 2C2H5OH ![]() C2H5OC2H5+H2O
C2H5OC2H5+H2O
C. CH3CH2CHO+HCN ![]() CH3CH2CH(CN)OH
CH3CH2CH(CN)OH
D. CH3COOH+C2H5OH ![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
查看答案和解析>>
科目: 来源: 题型:
【题目】Fe与水蒸气反应实验装置如图所示。
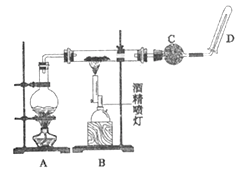
(1)装置A的作用是_________。
(2)B中反应的化学方程式为_____。
(3)C的作用是除杂,使用的试剂是_________。
(4)在D处玻璃管口点燃生成的气体前,必须对该气体进行_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】利用下图所示实验装置能验证热稳定性Na2CO3强于NaHCO3。请回答:
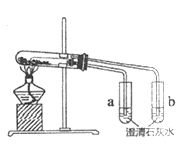
(1) NaHCO3受热分解的化学方程式是_________。
(2)证明热稳定性Na2CO3强于NaHCO3的实验现象是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组制备高铁酸钾(K2FeO4) 并探究其性质。
资料: K2FeO4 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4 (夹持装置略)

①A为氯气发生装置。A中化学反应的还原剂是_______。
②装置B的作用是除杂,所用试剂为___________。
③C中得到紫色固体和溶液。C中的反应有:3Cl2 + 2Fe(OH)3+ 10KOH=== 2K2FeO4 + 6KCl+ 8H2O
此反应表明:氧化性Cl2______FeO42-(填“>”或“<”)。
④C中除了发生③中的反应,还发生化学反应:__________。
(2)探究K2FeO4的性质
用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液a。取少量a,滴加盐酸,有Cl2产生。
①此实验可证明氧化Cl-的物质只能是FeO42-。用KOH溶液洗涤的目的是__________。
②此实验得出Cl2和FeO42-的氧化性强弱关系与制备实验时得出的结论相反,原因是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A是生产某新型工程塑料的基础原料之一,结构简式为 。
。
(1)写出A的分子式___________。
(2)拟从芳香烃![]() 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下:

已知:A在酸性条件下水解生成有机物B和甲醇。
(a)写出反应⑤的类型__________。
(b)写出H的结构简式____________________。
(c)G中所含官能团的名称是_________、__________;
(d)已知F分子中含有“—CH2OH”,通过F不能有效、顺利地获得B,其原因是______________________。
(e)写出反应⑦的方程式(注明必要的条件)___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某一定量的苯的同系物A完全燃烧,生成的气体通过浓硫酸后,浓硫酸增重5.4克,再通过KOH溶液后,KOH溶液增重19.8克,(设浓硫酸和KOH溶液的吸收率为100%)。
(1)通过计算确定A的分子式。(写出计算过程)_________________
(2)若0.1molA的氧化产物(被酸性高锰酸钾氧化)恰好被2mol/L100mL的NaOH溶液完全中和。写出A可能的的结构简式。_________________________
(3)若A的核磁共振氢谱中只有2种峰,则写出A的结构简式。_____________________
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两组同学用不同的方法制备SO2并探究其性质。(夹持装置已略去)
I.甲组同学设计的实验装置如图所示,回答下列问题:

(1)试管①中反应的化学方程式是__________。
(2)试管②中的品红溶液褪色。欲证明品红褪色的原因是SO2,需要补充的实验操作及应出现的实验现象是__________。
(3)试管③中的试剂是NaOH溶液,反应的离子方程式是___________。
II.乙组同学设计的实验装置如下图所示,回答下列问题:

已知: BaSO3是白色难溶于水的物质,但可溶解于盐酸。
(4)④中反应的化学方程式是__________。
(5)⑤中产生了不溶于盐酸的白色沉淀,该沉淀是___________。
(6)经过分析,乙组同学认为装置中的空气是出现白色沉淀的原因。他们在不改变实验装置的情况下加入了某操作过程,证实了这种猜测是正确的。他们的操作及实验现象是__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2。某同学在实验室中对NH3与NO2反应进行了探究。回答下列问题:
(1)用消石灰和氯化铵固体制备NH3

①NH3的发生装置应选择上图中的_______(填序号),制备NH3的化学方程式为______。
②欲收集一瓶干燥的NH3,选择上图中的装置,其连接顺序为:发生装置→_________(按气流方向,用小写字母表示)。
(2)研究NH3与NO2的反应
将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。

操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢充入Y管中 | ①Y管中__________ | ②反应的化学方程式 _______________ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝聚 |
打开K2 | 溶液倒吸入Y管 | ③________________ |
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组离子能够在碱性溶液中大量共存,且溶液呈无色透明的是( )
A.K+、Cu2+、Cl-、SO42-B.Na+、CO32-、SO42-、Cl-
C.NO3-、Na+、CO32-、Ba2+D.Na+、NO3-、H+、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com