
科目: 来源: 题型:
【题目】X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
(1)L的元素符号为________;M在元素周期表中的位置为___________;五种元素的原子半径从大到小的顺序是_______________(用元素符号表示)。
(2)Z、X两元素按原子数目比l∶3和2∶4构成分子A和B,A的电子式为______,B的化学式为____________,Z、X两种元素形成的一种既含离子键又含共价键的物质名称为:____________;
(3)硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为_______,其最高价氧化物对应的水化物与足量烧碱溶液反应的化学方程式为____________。1mol铁跟足量的硒单质化合时,转移的电子数为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A. 化学合成和分离技术是人类生存所必须的,是其他各项技术的基础
B. 氨基酸是指分子中含有﹣COOH和﹣NH2,且连在同一个碳原子上
C. 根据纤维在火焰上燃烧产生的气味,确定该纤维是否为蛋白质纤维
D. Na2SiO3的水溶液俗称水玻璃,用水玻璃浸泡的木材、纺织品耐火耐腐蚀
查看答案和解析>>
科目: 来源: 题型:
【题目】A+、B+、C-、D、E5种微粒(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①A++C-=D+E;②B++C-=2D。据此,回答下列问题:
(1)上述含10电子的四核阳离子为___________,含10电子的阴离子为_______。
(2)A+和B+的电子式A+____________、B+____________。
(3)C-、D、E3种粒子结合质子H+的能力由强到弱的顺序是(用粒子的化学式表示)____________________;这一顺序可用以下离子方程式加以说明:
①_____________________________________________;
②_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有机物中
①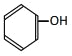 ②
② 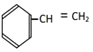 ③
③![]() ④
④![]() ⑤
⑤ 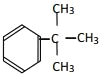 ⑥
⑥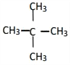
(1)属于芳香族化合物的是______;
(2)属于芳香烃的是______;
(3)属于苯的同系物的是______;
(4)属于脂环烃的是______;
(5)属于烃的衍生物的是______(填序号)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 | |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在这些元素中,最易失电子的元素是________,非金属性最强的元素是______;
(2)化学性质最不活泼的元素是_____,其原子的原子结构示意图为________;
(3)元素的最高价氧化物对应的水化物中酸性最强的是____,碱性最强的是___,呈两性的氢氧化物是_______________;(填写化学式)
(4)在③~⑦元素中,简单离子半径最小的是_________;
(5在⑦与⑩的单质中,氧化性较强的是_______________,用反应化学方程式证明:_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学为了验证碳和硅两种元素非金属性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。
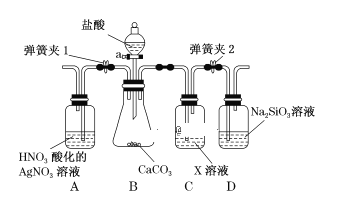
实验操作步骤:
Ⅰ.打开弹簧夹1,关闭弹簧夹2,并打开活塞a,滴加盐酸。
Ⅱ.A中看到白色沉淀时,…,关闭活塞a。请回答:
(1)B中反应的离子方程式是_________________________________________。
(2)通过步骤 Ⅰ、 Ⅱ 得知盐酸具有的性质是________(填字母)。
A.挥发性 B.还原性 C.氧化性 D.酸性
(3)C装置的作用是______________,X是____________________(写化学式)。
(4)为了验证碳的非金属性强于硅,步骤Ⅱ中未写的操作和现象是_______________,D中反应的化学方程式是__________________________________。
(5)碳、硅的非金属性逐渐减弱的原因是_____________________(从原子结构角度加以解释)。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求填空:
(1)已知R2-离子的核内有n个中子,R的质量数为M,则mg R2-离子里含有电子的物质的量为 ____________mol。
(2)X元素最高价氧化物对应的水化物为H3XO4,则它对应的气态氢化物为_____ 。
(3)已知同周期X、Y、Z三种元素的最高价氧化物对应水化物酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则元素非金属性由强到弱顺序为:____________ ;气态氢化物的稳定性由强到弱顺序为:______________ 。
(4).甲、乙两种非元素:①甲比乙容易与H2化合;②甲原子能与乙的阴离子发生置换反应;③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强;④与某金属反应时,甲原子得电子数目比乙的多;⑤甲的单质熔、沸点比乙的低。
能说明甲的非金属性比乙的非金属性强的有________________
(5)下表是某兴趣小组通过实验获得的相同体积足量稀硫酸与铁反应的实验数据:
实验序号 | 金属质量/g | 金属状态 | c(H2SO4) mol/L | 实验温度/℃ | 金属消失的时间/s |
1 | 0.10 | 丝 | 0.7 | 25 | 240 |
2 | 0.10 | 丝 | 1.0 | 25 | 190 |
3 | 0.10 | 粉末 | 1.0 | 25 | 120 |
4 | 0.10 | 粉末 | 1.0 | 40 | 40 |
分析上述数据,回答下列问题:
①实验1、
②实验2、3可得出的结论是_________________________。
③实验3、4可得出的结论是______________________。
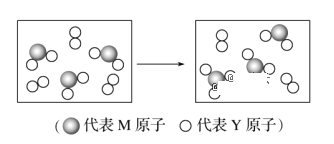
(6)下图表示由M、Y两元素组成的两种气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求回答下列问题:
(1)键线式![]() 表示的分子式______;结构简式是______。
表示的分子式______;结构简式是______。
(2)![]() 中含有的官能团的名称为____________。
中含有的官能团的名称为____________。
(3)![]() 命名:_____________。
命名:_____________。
(4)写出乙醇在铜做催化剂的情况下被氧化成乙醛的化学方程式:________
(5)![]() 的分子式为______;
的分子式为______;
查看答案和解析>>
科目: 来源: 题型:
【题目】用右图所示装置进行下列实验,实验结果与预测的现象不一致的是
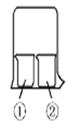
①中的物质 | ②中的物质 | 预测①中现象 | |
A | 淀粉碘化钾溶液 | 浓硝酸 | 无明显现象 |
B | 酚酞溶液 | 浓盐酸 | 无明显现象 |
C | 氯化铝溶液 | 浓氨水 | 有白色沉淀 |
D | 湿润红纸条 | 饱和氯水 | 红纸条褪色 |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】用价层电子对互斥理论预测H2S和BCl3的立体结构,两个结论都正确的是
A. 直线形;三角锥形B. V形;三角锥形
C. 直线形;平面三角形D. V形;平面三角形
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com