
科目: 来源: 题型:
【题目】冬青油又叫水杨酸甲酯,是一种重要的有机合成原料。某化学小组用水杨酸(![]() )和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
)和甲醇在酸性催化剂催化下合成水杨酸甲酯并计算其产率。
实验步骤:
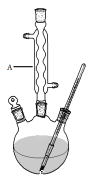
Ⅰ.如图,在三颈烧瓶中加入13.8g (0.1mol)水杨酸和24 g(30 mL,0.75 mol)甲醇,向混合物中加入约10 mL甲苯(甲苯与水形成的共沸物,沸点为85℃,该实验中加入甲苯,易将水蒸出),再小心地加入5 mL浓硫酸,摇动混匀,加入1~2粒沸石,组装好实验装置,在85~95℃下恒温加热反应1.5小时:
Ⅱ.待装置冷却后,分离出甲醇,然后转移至分液漏斗,依次用少量水、5%NaHCO3溶液和水洗涤;分出的产物加入少量无水MgSO4固体,过滤得到粗酯;
Ⅲ.将粗酯进行蒸馏,收集221℃~224℃的馏分,得水杨酸甲酯9.12g。
常用物理常数:
名称 | 分子量 | 颜色状态 | 相对密度 | 熔点(℃) | 沸点(℃) |
水杨酸甲酯 | 152 | 无色液体 | 1.18 | -8.6 | 224 |
水杨酸 | 138 | 白色晶体 | 1.44 | 158 | 210 |
甲醇 | 32 | 无色液体 | 0.792 | -97 | 64.7 |
请根据以上信息回答下列问题:
(1)仪器A的名称是 ,加入沸石的作用是 。若加热后发现未加沸石,应采取的正确方法是 。
(2)制备水杨酸甲酯时,最合适的加热方法是 。
(3)实验中加入甲苯对合成水杨酸甲酯的作用是 。
(4)反应结束后,分离出甲醇采用的方法是 。
(5)实验中加入无水硫酸镁的作用是 。
本实验的产率为 (保留两位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上常以烃的含氧衍生物X为主要原料生产可降解塑料PCL{HO(CH2)5COOH}及阻燃剂四溴双酚A。合成线路如下图所示:
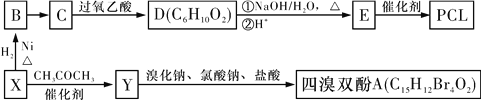
已知:①X的蒸气密度是相同条件下H2的47倍,遇FeCl3溶液显紫色;C为O。
②ROH![]() RBrOHBr。
RBrOHBr。
③RCOCH2R′![]() RCOOCH2R′。
RCOOCH2R′。
(1)X的分子式为____________;B的名称是__________。
(2)B→C还需要的反应试剂及条件是________________________。C→D的反应类型是______________。
(3)写出X→Y的化学方程式: _______________________________________。
(4)0.5 mol四溴双酚A在常温下与足量的Na2CO3溶液反应,最多消耗________mol Na2CO3。
(5)符合以下条件的C的同分异构体有__________种(不考虑立体异构)。
①含有两个甲基 ②含有一个碳碳双键 ③能发生银镜反应
(6)已知由烯烃直接制备不饱和酯的新方法为:2CH3CHCH2+2ROH+2CO+O2![]() 2CH3CHCHCOOR+2H2O,利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料CHCH2COOCH2CH3,写出合成该涂料的反应流程图。_________________
2CH3CHCHCOOR+2H2O,利用乙烯为有机原料(无机物和反应条件自选)合成聚合物涂料CHCH2COOCH2CH3,写出合成该涂料的反应流程图。_________________
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)①Na2CO3俗称纯碱,其水溶液呈碱性,原因是________________________(用离子方程式解释);
②常温下,0.050 0 mol/L硫酸溶液的pH=__________;
③用0.010 0 mol/L氢氧化钠溶液滴定未知浓度的盐酸,酚酞作指示剂,滴定终点时,溶液的颜色由无色变为__________(填“蓝色”或“浅红色”),且半分钟内保持不变。
(2)①已知H2与O2反应生成1 mol H2O(g)时放出241.8 kJ的热量,请完成该反应的热化学方程式:2H2(g)+O2(g)===2H2O(g) ΔH=__________kJ/mol;
②已知:C(石墨,s)===C(金刚石,s) ΔH>0,则稳定性石墨比金刚石________(填“强”或“弱”)。
(3)在某恒容密闭容器中进行可逆反应FeO(s)+CO(g)=Fe(s)+CO2(g) ΔH>0,平衡常数表达式为K=![]() 。
。
①反应达到平衡后,向容器中通入CO,化学平衡向__________(填“正反应”或“逆反应”)方向移动;
②若降低温度,平衡常数K__________(填“增大”“减小”或“不变”);
③查阅资料得知1 100 ℃时K=0.263。某时刻测得容器中c(CO2)=0.025 mol/L,c(CO)=0.10 mol/L,此时刻反应__________(填“达到”或“未达到”)平衡状态。
(4)电化学是研究化学能与电能相互转化的装置、过程和效率的科学。
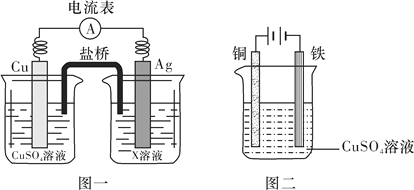
①根据氧化还原反应2Ag+(aq)+Cu(s)===2Ag(s)+Cu2+(aq),设计的原电池如图一所示,X溶液是__________(填“CuSO4”或“AgNO3”)溶液;
②图二装置在铁件上镀铜,铁作阴极,则阴极上的电极反应式是__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)关注营养平衡,合理使用药物,有利于身心健康。现有下列四种物质:
A.维生素C B.油脂 C.青霉素 D.碘酸钾
请根据题意,选择恰当的选项用字母代号填空。
①在人体内起供能和储能作用的物质是______________________;
②为预防甲状腺肿大,常在食盐中加入的物质是______________________;
③能阻止多种细菌生长的重要抗生素是__________________________;
④存在于蔬菜、水果中,具有还原性的物质是______________________。
(2)随着工业的发展和社会的进步,人们日益关注环境污染问题。
①垃圾处理遵循无害化、减量化和资源化的原则,垃圾分类收集是实现上述原则的措施之一,贴有如图所示标志的垃圾箱收集的是________(填字母代号);

A.可回收物 B.有害物质 C.其他垃圾
②我国城市发布的“空气质量日报”中,下列物质不列入首要污染物的是______(填字母代号);
A.二氧化硫 B.二氧化碳 C.二氧化氮 D.可吸入颗粒
③使用Pb2+含量超标的水,会严重危害人体健康,某冶炼厂产生了Pb2+含量超标的废水,处理此废水的方法是加入适量Na2S,使Pb2+沉淀而除去。请写出该反应的离子方程式:______________________________________________。
(3)材料是人类生存和发展的物质基础,合理使用材料可以节约资源。
①下列生活中的常见物质,属于合金的是________(填字母代号);
A.汽车轮胎 B.不锈钢 C.水泥
②我国航天员穿的航天服主要是由具有密度小、强度高、耐腐蚀、柔软等优良性能的特殊材料制成的,这些材料属于__________(填字母代号)。
A.镁铝合金 B.合成纤维 C.天然纤维
(4)某同学取一颗光亮的铁钉按如图装置做吸氧腐蚀实验。几天后观察到试管内铁钉生锈,液面上升。此过程中,负极的反应式为Fe-2e-===Fe2+,则正极的反应式为__________________________________________。

查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关胶体的叙述正确的是( )
A. 直径介于1-100nm之间的微粒称为胶体
B. 有色玻璃、雾都不是胶体
C. 涂料、颜料、墨水的制造,明矾净水和胶体有关
D. 硅酸胶体加入过量的氢氧化钠溶液由于胶体聚沉而形成硅酸沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组对铝热反应实验展开研究。现行高中化学教材中对“铝热反应”的现象有这样的描述:“反应放出大量的热,并发出耀眼的光芒”“纸漏斗的下部被烧穿,有熔融物落入沙中”。查阅《化学手册》知,Al、Al2O3、Fe、Fe2O3的熔点、沸点数据如下:
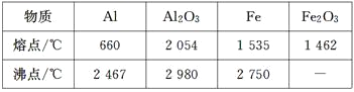
Ⅰ.(1)某同学推测,铝热反应所得到的熔融物应是铁铝合金。理由是:该反应放出的热量使铁熔化,而铝的熔点比铁低,此时液态的铁和铝熔合形成铁铝合金。你认为他的解释是否合理?________(填“合理”或“不合理”)。
(2)设计一个简单的实验方案,证明上述所得的块状熔融物中含有金属铝。该实验所用试剂是________,反应的离子方程式为__________________________________________________。
(3)实验室溶解该熔融物,在下列试剂中最适宜的试剂是________(填序号)。
A.浓硫酸 B.稀硫酸 C.稀硝酸 D.氢氧化钠溶液
Ⅱ.实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。某同学取一定量上述的熔融物与一定量很稀的硝酸充分反应,反应过程中无气体放出。在反应结束后的溶液中,逐滴加入4 mol·L-1的氢氧化钠溶液,所加氢氧化钠溶液的体积(mL)与产生的沉淀的物质的量(mol)的关系如图所示。试回答下列问题:
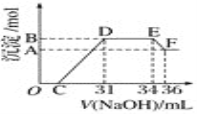
(1)图中OC段没有沉淀生成,此阶段发生反应的离子方程式为_________________________。
(2)在DE段,沉淀的物质的量没有变化,则此阶段发生反应的离子方程式为___________;上述现象说明溶液中________结合OH-的能力比________强(填离子符号)。
(3)B与A的差值为________mol。
(4)B点对应的沉淀的物质的量为________mol,C点对应的氢氧化钠溶液的体积为________mL。
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,请参照元素①~⑦在表中的位置,回答下列问题:
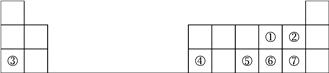
(1)①~⑦元素中原子半径最大的是__________(用元素符号表示);
(2)②⑦两种元素所形成的气态氢化物中最稳定的是__________(用化学式表示);
(3)⑤⑥两种元素最高价氧化物对应的水化物的酸性较强的是__________(用化学式表示);
(4)写出③④两种元素的最高价氧化物对应的水化物发生反应的离子方程式:_____________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,按下列物质的量关系进行反应,其对应的离子方程式或化学方程式书写正确的是( )
A. n(Cl2)∶n(Fe)=5∶45Cl2+4Fe![]() 2FeCl2+2FeCl3
2FeCl2+2FeCl3
B. n(Cl2)∶n(FeBr2)=1∶1Fe2++2Br-+Cl2=Fe3++Br2+2Cl-
C. n(MnO4—)∶n(H2O2)=2∶32MnO4—+3H2O2+6H+=2Mn2++4O2↑+6H2O
D. n(Fe)∶n[HNO3(稀)]=1∶34Fe+12H++3NO3—=3Fe2++Fe3++3NO↑+6H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com