
科目: 来源: 题型:
【题目】ClO2是新一代饮用水的消毒剂,我国许多自来水厂采用ClO2代替Cl2来进行自来水消毒。请回答下列有关问题:
(1)ClO2读作____________,它属于________(选填“单质”“氧化物”或“混合物”)。
(2)ClO2中氯元素的化合价为__________。
(3)我国最近成功研制出制取ClO2的新方法,其反应的微观过程如图所示:

该反应的化学方程式为__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组按下列路线合成镇痛药哌替啶:
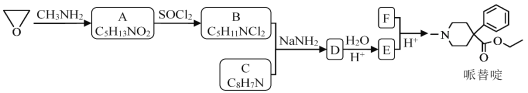
已知: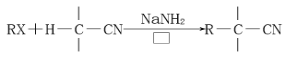
请回答:
(1)A→B的反应类型是________。
(2)下列说法不正确的是________(填字母)。
A.化合物A的官能团是硝基 B.化合物B可发生消去反应
C.化合物E能发生加成反应 D.哌替啶的分子式是C15H21NO2
(3)写出B+C→D的化学反应方程式________。
(4)设计以甲苯为原料制备C的合成路线__________________(用流程图表示,无机试剂任选)。
(5)写出同时符合下列条件的C的所有同分异构体的结构简式________。
①分子中有苯环而且是苯环的邻位二取代物;
②1HNMR谱表明分子中有6种氢原子;IR谱显示存在碳氮双键(C=N)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学课外小组所做实验的示意图如图所示:图中“→”表示气体流向, M是一种纯净而干燥的气体,Y为另一种气体,E内有红棕色气体产生,实验所用物质只能由下列物质中选取:Na2CO3、Na2O2、NaCl、Na2O、CaCl2、(NH4)2CO3、碱石灰等固体及蒸馏水。据此实验,完成下列填空:
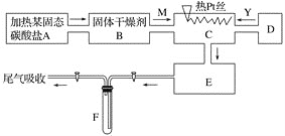
(1)A中所用装置的主要仪器和药品是______________________。
(2)B中所选的干燥剂是________,其作用是______________________________。
(3)C中发生的主要反应的化学方程式:________________________________。
(4)制取Y气体的D装置所用的主要仪器是__________________________。
制取Y气体的化学方程式是________________________。
(5)F中发生反应的化学方程式为__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】聚乙炔能够导电,下列关于聚乙炔![]() 和聚合物A
和聚合物A![]() 的说法中正确的是
的说法中正确的是
A. 聚合物A和聚乙炔均能使溴水褪色
B. 两种聚合物的单体互为同系物
C. 聚合物A的相对分子质量是聚乙炔的两倍
D. 1mol 两种聚合物的单体分别与Br2发生反应,最多消耗Br2的物质的量之比为2:1
查看答案和解析>>
科目: 来源: 题型:
【题目】FeSO4受热分解的化学方程式为2FeSO4![]() Fe2O3+SO2↑+SO3↑
Fe2O3+SO2↑+SO3↑
请回答:
(1)将FeSO4受热产生的气体按图示装置进行实验,证实含有SO3和SO2。能说明SO2存在的实验现象是______________________;为测定BaSO4沉淀的质量,后续的操作步骤依次为________、洗涤、干燥、称量。

(2)设计一个实验方案,用化学方法验证FeSO4受热后固体的成分(不考虑其他反应)
________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以苯为基础原料,可以合成多种有机物。

已知:I.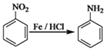
II.![]()
回答下列问题:
(1)由苯合成有机物A用到的无机试剂为______________。
(2)B分子中的官能团的名称为_________,B→C的反应类型为_______________。
(3)生成PF树脂的化学方程式为_____________。
(4)试剂D是___________________(填代号)。
a.溴水 b.高锰酸钾溶液 c.Ag(NH3)2OH溶液 d.新制Cu(OH)2悬浊液
(5)写出同时满足下列条件的肉桂酸乙酯的一种同分异构体________________。
①苯环上仅有2个取代基且处于对位
②能发生水解反应和银镜反应,其中一种水解产物遇FeCl3溶液显紫色
③为顺式异构
(6)以乙醇为原料合成CH3-CH=CH-COOCH2CH3,其他试剂任选,写出合成路线________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学小组采用如图所示装置,对浓硝酸与木炭的反应进行探究(已知:4HNO34NO2↑+O2↑+2H2O)。

请回答下列问题:
(1)检查装置气密性后,将燃烧匙中的木炭在酒精灯上加热至红热状态,伸入三口烧瓶中,并塞紧瓶塞,滴加浓硝酸,可观察到三口烧瓶中气体的颜色为________,产生该气体的化学方程式是____________。
(2)装置C中盛有足量Ba(OH)2溶液,炽热的木炭与浓硝酸反应后可观察到C中出现白色沉淀,该白色沉淀为____________(填化学式)。
(3)装置B的作用是__________________________。
(4)装置D中收集到了无色气体,部分同学认为是NO,还有部分同学认为是O2。
①下列对该气体的检验方法合适的是________。
A.敞口观察装置D中集气瓶内气体的颜色变化
B.将湿润的蓝色石蕊试纸伸入集气瓶内,观察蓝色石蕊试纸是否变红
C.将带火星的木条伸入集气瓶中,观察木条是否复燃
②如果D中集气瓶中收集的无色气体是氧气,则氧气的来源是________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】卤素单质及其化合物是物质世界不可缺少的组成部分。请利用所学物质结构与性质的相关知识回答下列问题:
(1)At原子的核外价电子排布式为______________________;I3+中心原子杂化方式为_______;ClO2-的空间构型为__________。基态氟原子核外电子有________种空间运动状态。
(2)已知高碘酸有两种结构,化学式分别为H5IO6(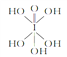 )和HIO4;前者为五元酸,后者为一元酸,请比较二者的酸性强弱:H5IO6 ______HIO4(填“>”、“=”或“<”).
)和HIO4;前者为五元酸,后者为一元酸,请比较二者的酸性强弱:H5IO6 ______HIO4(填“>”、“=”或“<”).
(3)TiCl4熔点为-24℃,沸点为136.4℃。可溶于甲苯,固态TiCl4属于_________晶体。
(4)用锌还原TiCl4的盐酸溶液,可制得绿色配合物[TiCl(H2O)5]Cl2·H2O。1mol该配合物中含有σ键数目为__________。
(5)CaF2晶胞结构如下图
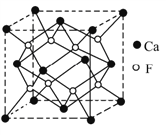
①晶体中距离最近的2个Ca2+(X)与一个F-(Y)形成的夹角(∠XYX)为___________。
②CaF2的摩尔质量为78g/mol,晶胞密度为ρg/cm3,阿伏加德罗常数为NA,则晶体中两个最近的Ca2+间中心距离为____________cm
查看答案和解析>>
科目: 来源: 题型:
【题目】由硫铁矿烧渣(主要成分:Fe3O4、Fe2O3、和FeO)得到绿矾(FeSO4·7H2O),在通过绿矾制备铁黄[FeO(OH)]的流程如下:
![]()
已知:FeS2和铁黄均难溶于水
下列说法不正确的是
A. 步骤①,最好用硫酸来溶解烧渣
B. 步骤②,涉及的离子方程式为FeS2+14Fe3++8H2O=15Fe2++2SO42-+16H+
C. 步骤③,将溶液加热到有较多固体析出,再用余热将液体蒸干,可得纯净绿矾
D. 步骤④,反应条件控制不当会使铁黄中混有Fe(OH)3
查看答案和解析>>
科目: 来源: 题型:
【题目】利用钛白粉厂废酸(主要含硫酸、Fe3+、Fe2+、TiO2+、Al3+)制备过二硫酸铵[(NH4)2S2O8],同时回收TiO(OH)2的简要流程如下:
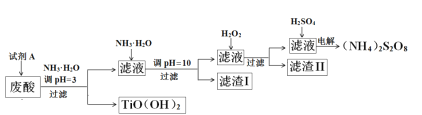
已知:i.部分离子完全生成氢氧化物沉淀的pH
金属离子 | TiO2+ | Fe3+ | Fe2+ | Al3+ |
开始沉淀的PH | 1.2 | 1.9 | 7.0 | 3.2 |
沉淀完全的pH | 2.8 | 3.1 | 9.4 | 4.7 |
ii.pH>7时,Fe2+部分生成Fe(II)氨络离子[Fe(NH3)2]2+。
请回答下列问题:
(1)为保证产物TiO(OH)2的纯度,加入试剂A要适量。试剂A为___________。
(2)煅烧回收的TiO(OH)2,获得的TiO2会发黄,发黄的杂质可能是_______(填化学式)。
(3)滤渣I的主要成分除Fe(OH)2、Al(OH)3外,还含有______________。
(4)加入H2O2的目的是氧化除掉Fe(II)氨络离子[Fe(NH3)2]2+,配平下列离子方程式:2[Fe(NH3)2]2+ +________+4H2O +H2O2 =_______ + 4NH3·H2O
(5)电解制备过二硫酸铵的装置如下图所示。
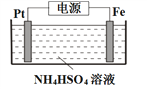
①S2O82-中S元素的化合价为+6,其中过氧键的数目为___________。
②电解时,铁电极连接电源的___________极。
③常温下,电解液中含硫微粒主要存在形式与 pH 的关系如下图所示。
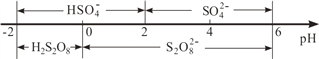
在阳极放电的离子主要为HSO4-,阳极区电解质溶液的 pH 范围为______,阳极的电极反应式为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com