
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是
A. 32 g O2和O3的混合气体所含原子数为NA
B. 5NH4NO3![]() 2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA
2HNO3+4N2↑+9H2O反应中,生成28g N2时,转移的电子数目为3.75NA
C. 高温下,0.2mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
D. 在25℃、101kPa下,2 mol氧气和氢气的混合气体的体积约为44.8 L
查看答案和解析>>
科目: 来源: 题型:
【题目】按要求完成下列反应方程式:
①CH3-CH2-Br与氢氧化钠溶液在加热条件下的反应方程式 ___________________________________。
②乙醛与银氨溶液水浴加热条件下的反应方程式___________________________________。
③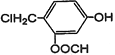 与NaOH溶液在加热条件下的化学反应方程式___________________________________。
与NaOH溶液在加热条件下的化学反应方程式___________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列与含氯化合物有关的说法正确的是
A. HClO是弱酸,所以NaClO是弱电解质
B. 向沸水中逐滴加入少量饱和FeCl3溶液,可制得Fe(OH)3胶体
C. 六水合氯化钙可用作食品干燥剂
D. 氯化铵、漂白粉都属于强电解质
查看答案和解析>>
科目: 来源: 题型:
【题目】有一无色溶液,其中可能含有 Fe3+、Al2+ 、Fe2+、Mg2+、Cu2+、NH4+、K+、CO32-、SO42-等离子的几种,为分析其成分,取此溶液分别进行了四个实验,其探作和有关现象如下图所示:
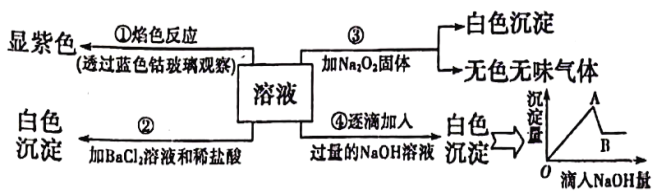
请你根据上图推断:
(1)原溶液中一定存在的阴离子有(写化学式):_________________________。
(2)写出实验④中产生的沉淀有:______________________。
写出由A→B过程中所发生反应的离子方程式: ______________________。
(3)实验③中产生无色无味气体所发生的化学方程式为:______________________。
(4)实验②中加入稀盐酸的目的是______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法中正确的是
A. 阿伏加德罗常数就是指6.02×1023
B. 1 mol 任何物质都约含有6.02×1023个分子
C. 3.01×1023个Na+的物质的量是0.5 mol
D. 2 mol SO42-约含有1.204×1023个SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】砷化镓是继硅之后研究最深入、应用最广泛的半导体材料。回答下列问题:
(1)Ga 基态原子核外电子排布式为 ____,As 基态原子核外有_________个未成对电子。
(2)Ga、As、Se 的第一电离能中大到小的顺序是 __________,Ga、As、Se 的电负性由大到小的顺序是 ____。
(3)比较下列镓的卤化物的熔点和沸点,分析其变化规律及原因:_____。
镓的卤化物 | GaCl3 | GaBr3 | GaI3 |
熔点/℃ | 77.75 | 122.3 | 211.5 |
沸点/℃ | 201.2 | 279 | 346 |
GaF3 的熔点超过 1000 ℃,可能的原因是 _____________。
(4)二水合草酸镓的结构如图 1 所示,其中镓原子的配位数为_____,草酸根中碳原子的杂化轨道类型为 ____。
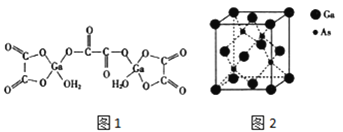
(5)砷化镓的立方晶胞结构如图 2 所示,晶胞参数为 a=0.565nm,砷化镓晶体的密度为_____g/ cm3(设 NA为阿伏加德罗常数的值,列出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气的制取与储存是氢能源利用领域的研究热点。回答下列问题:
(1)直接热分解法制氢
某温度下2H2O(g) ![]() 2H2(g) +O2(g),该反应的平衡常数表达式为 K= ________。
2H2(g) +O2(g),该反应的平衡常数表达式为 K= ________。
(2)乙醇水蒸气重整制氢
反应过程和反应的平衡常数(K)随温度(T)的变化曲线如图 1 所示。某温度下,图 1 所示反应每生成1mol H2(g),热量变化是 62 kJ,则该反应的热化学方程式为________________
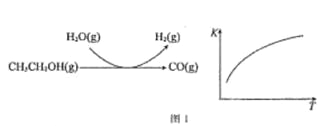
(3)水煤气法制氢
CO(g)+ H2O(g) ![]() CO2(g) +H2(g) △H<0,在进气比[n(CO):n(H2O)]不同时,测得相应的 CO 的平衡转化率见图 2(图中各点对应的反应温度可能相同,也可能不同)。
CO2(g) +H2(g) △H<0,在进气比[n(CO):n(H2O)]不同时,测得相应的 CO 的平衡转化率见图 2(图中各点对应的反应温度可能相同,也可能不同)。
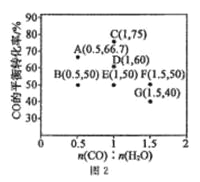
①向 2 L 恒温恒容密闭容器中加入一定量的 CO 和 0.1mol H2O(g),在图中 G 点对应温度下,反应经5 min 达到平衡,则平均反应速率 v(CO)=___________。
②图中 B、E 两点对应的反应温度分别为 TB 和 TE,则 TB ___________TE (填“>”“ <”或“=”)。
③经分析,A、E、G 三点对应的反应温度都相同(均为 T℃),其原因是 A、E、G 三点对应的 _______相同。
④当 T℃时,若向一容积可变的密闭容器中同时充入 3.0 mol CO、1.0 mol H2O(g)、1.0 molCO2 和xmol H2,使上述反应开始时向正反应方向进行,则x应满足的条件是_________。
(4)光电化学分解制氢

反应原理如图3,钛酸锶光电极的电极反应式为 4OH--4e-=O2↑+2H2O,则铂电极的电极反应式为 ________。
(5)Mg,Cu 是一种储氢合金
350℃时,Mg、Cu 与 H2 反应,生成 MgCu2 和仅含一种金属元素的氢化物(其中氢的质量分数约为 7.7%)。该反应的化学方程式为_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】二甲醚又称甲醚,简称DME,熔点为-141.5℃,沸点为-24.9℃。二甲醚与液化石油气(LPG)相似,被誉为“21世纪的清洁燃料”。由合成气(CO、H2)制备二甲醚的反应原理如下:
①CO(g)+2H2(g)![]() CH3OH(g) △H1= -90.0 kJ·mol-1
CH3OH(g) △H1= -90.0 kJ·mol-1
②2CH3OH(g)![]() CH3OCH3(g)+H2O(g) △H2=-20.0kJ·mol-l
CH3OCH3(g)+H2O(g) △H2=-20.0kJ·mol-l
回答下列问题:
(1)反应①为熵___________(填“增加”或“减少”)的反应,__________ (填“低温”或“高温”)下易自发进行。
(2)写出由合成气(CO、H2) 直接制备二甲醚的热化学方程式:__________________________________。
(3)温度为500K时,在2L的密闭容器中充入2 mol CO和6 molH2发生反应①、②,5 min时达到平衡,平衡时CO的转化率为60%,c(CH3OCH3)=0.2 mol·L-1,用H2表示反应①的速率是______________,反应②的平衡常数K=________________。
若在500K时,测得容器中n(CH3OCH3)=2n (CH3OH),此时反应②的v正__ v逆(填“>”、 “< ”或“=”)。
(4)研究发现,在体积相同的容器中加入物质的量相同的CO和H2发生反应①、②,在不同温度和有无催化剂组合下经过相同反应时间测得如下实验数据:
T(K) | 催化剂 | CO转化率(%) | CH3OCH3选择性(%) |
473 | 无 | 10 | 36 |
500 | 无 | 12 | 39 |
500 | Cu/ZnO | 20 | 81 |
[备注]二甲醚选择性:转化的CO中生成CH3OCH3的百分比
①相同温度下,选用Cu/ZnO作催化剂,该催化剂能____________ (填标号)。
A.促进平衡正向移动 B.提高反应速率 C.降低反应的活化能
D.改变反应的焓变 E.提高CO的平衡转化率
②表中实验数据表明,在500K时,催化剂Cu/ZnO对CO转化成CH3OCH3的选择性有显著的影响,其原因是_________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com