
科目: 来源: 题型:
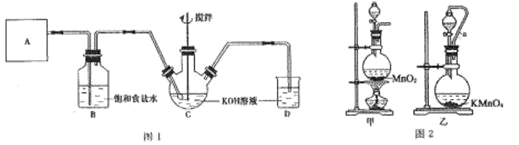
【题目】实验室用图 1 所示装置制备 KClO 溶液,并通过 KClO 溶液与 FeCl3 溶液的反应制备高效水处理剂K2FeO4。已知 K2FeO4 具有下列性质: ①可溶于水,微溶于饱和 KOH 溶液;②在 0~5 ℃的强碱性溶液中比较稳定;③在 Fe3+和 Fe(OH)3 催化作用下发生分解;④在酸性至弱碱性条件下,能与水反应生成 Fe(OH)3 和 O2。
回答下列问题:
(1)装置A 用于产生氯气,若选用图 2 中的甲装置,反应的离子方程式是_____,若选用装置乙,其中的导管 a 的作用是_____。
(2)Cl2 与 KOH 在较高温度下反应生成 KClO3。在不改变 KOH 溶液的浓度和体积的条件下,控制反应在0--5℃进行。实验中可采取的措施是_____;在通入氯气的过程中,不断搅拌的目的是_____。
(3)制备 K2FeO4 时,KClO 饱和溶液与 FeCl3 饱和溶液的混合方式为_____,反应的离子方程式是_____。
(4)提纯 K2FeO4 粗产品[ 含有 Fe(OH)3、KCl 等杂质]的实验方案为:将 K2FeO4 粗产品溶于冷的3 mol/LKOH 溶液中__________(填操作名称),将滤液置于冰水浴中,再加入_________,搅拌、静置、再过滤,晶体用适量乙醇洗涤 2--3 次后,在真空干燥箱中干燥。
查看答案和解析>>
科目: 来源: 题型:
【题目】以下实验能获得成功的是( )
A.用稀硫酸与乙醇混合液共热控制在170℃制乙烯气体
B.将铁屑、溴水、苯混合制溴苯
C.在苯酚溶液中滴入少量稀溴水出现白色沉淀
D.将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A.蔗糖和葡萄糖互为同分异构体
B.淀粉、纤维素都是天然高分子化合物
C.蔗糖与稀硫酸共热后的溶液中加入新制的氢氧化铜,加热有红色沉淀
D.在常温下,淀粉遇碘离子变蓝
查看答案和解析>>
科目: 来源: 题型:
【题目】某工业废料中含有 Cr(OH)3、Al2O3、CuO、NiO 等物质,工业上通过下列流程回收其中有用的金属和制取 Na2Cr2O7。
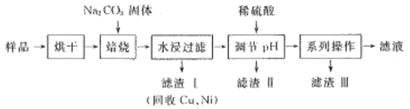
已知:①“水浸过滤”后的溶液中存在 Na2CrO4、NaAlO2 等物质
②除去滤渣 II 后,溶液中存在反应 2CrO42-+2H+![]() Cr2O72-+H2O
Cr2O72-+H2O
③Na2Cr2O7、Na2CrO4 在不同温度下的溶解度(g/100 g H2O)如下表:
20℃ | 60℃ | 100℃ | |
Na2Cr2O7 | 183 | 269 | 415 |
Na2CrO4 | 84 | 115 | 126 |
(1)“焙烧”过程中生成 NaAlO2 的化学方程式为_____。
(2)生成滤渣时,需加入适量稀硫酸调节溶液的 pH 除去 AlO2 -,若稀硫酸过量,则因过量引起反应的离子方程式为_______________________。
(3)“系列操作”为:继续加入稀硫酸、_____、冷却结晶、过滤。继续加入稀硫酸的目的是_________;滤渣 III 中除含有少量硫酸钠晶体外,主要成分是 _________________(写化学式)。
(4)工业上还可以在“水浸过滤”后的溶液中加入适量稀硫酸,用石墨作电极电解生产金属铬,阴极的电极反应式为 ____。
(5)流程图最后的“滤液”中仍然有残留的 Na2Cr2O7。Cr 为重金属元素,若含量过高就排入河流中, 会对河水造成重金属污染。为测定“滤液”中的 c(Na2Cr2O7),某实验小组取“滤液”20 mL,加水稀释至 250 mL,再取稀释后的溶液 25 mL 于锥形瓶中,用 c mol/L的 FeSO4 溶液进行氧化还原滴定,到终点 时清耗 FeSO4 溶液体积为 V mL[已知发生的反应为Na2Cr2O7+FeSO4+H2SO4→Na2SO4+Cr2(SO4)3+ Fe2(SO4)3+ H2O(未配平)],则“滤液”中的c(Na2Cr2O7)=_________mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列是六种环状的烃类物质:
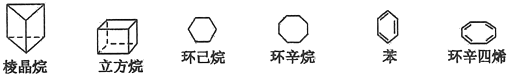
(1)互为同系物的有__________和____________(填名称)。互为同分异构体的有__________和____________、__________和____________(填写名称,可以不填满,也可以再补充)。
(2)立方烷的分子式为_________________,其一氯取代产物有________种,其二氯取代产物有___________种。
(3)写出两种与苯互为同系物且一氯代物只有两种的物质的结构简式,并命名:
结构________________________,名称_________________________;
结构________________________,名称_________________________;
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与生产、生活息息相关,下列叙述错误的是
A. 二氧化硫可广泛用于食品的增白
B. 小苏打是面包发酵粉的主要成分之一
C. 燃烧化石燃料是造成雾霾天气的一种重要因素
D. 硅胶可用作食品干燥剂
查看答案和解析>>
科目: 来源: 题型:
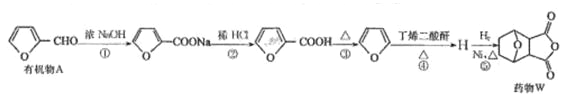
【题目】药物 W 对肝癌的治疗具有很好的效果,一种合成药物 W 的路线如下:
已知以下信息:
①2HCHO +NaOH→CH3OH+ HCOONa
②![]()
③丁烯二酸酐的结构筒式为![]()
回答下列问题:
(1)有机物 A 中含有的官能团有碳碳双键、_____(填名称)。
(2)第①步反应中除生成![]() 外,还生成另一产物,此产物的结构简式为_____。
外,还生成另一产物,此产物的结构简式为_____。
(3)H 的结构简式为_____。
(4)第⑤步的反应类型是_____。
(5)L 是药物 W 的同分异构体,同时满足下列条件的 L 有 _____种(不考虑立体异构);
①分子中含有苯环,苯环上,有 4 个取代基
②既能与 FeCl3,溶液发生显色反应,又能与 NaHCO3,溶液反应生成气体
③1mol能与 3 mol NaOH 完全反应,其中核磁共振氢谱为四组峰,峰面积比为 1:2:2:3 的结构简式为 ____。
(6)写出由![]() 制备丁烯二酸酐
制备丁烯二酸酐![]() 的合成路线:_____其他试剂任选)。
的合成路线:_____其他试剂任选)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化碘(ICl)跟水发生反应:ICl+H2O=HIO+HCl,这个过程可以称为ICl的水解。预计PCl3水解的产物是
A.PH3和HClOB.HCl和H3PO4C.HCl和H3PO3D.HCl和HPO3
查看答案和解析>>
科目: 来源: 题型:
【题目】在两份相同的Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示,下列分析正确的是
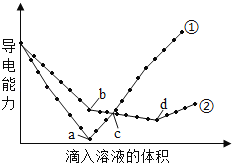
A. ②代表滴加H2SO4溶液的变化曲线
B. b点,两反应物物质的量之比为1: 2
C. a、d两点对应的溶液均显中性
D. c点,两溶液中含有相同物质的量浓度的OH﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com