
科目: 来源: 题型:
【题目】下列说法中正确的是( )
A. 加水稀释0.01 mol·L-1的CH3COOH溶液,溶液中c(OH-)减小
B. 室温时,0.1 mol·L-1的某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4
C. 氨水加水稀释后,溶液中![]() 的值增大
的值增大
D. 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
查看答案和解析>>
科目: 来源: 题型:
【题目】有一种香料X的相对分子质量为88,只含有C,H、O三种元素,其原子个数比为2:4:1,含有碳氧双键,与其有关的反应如下:
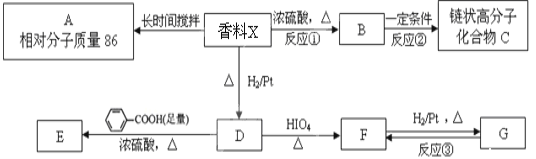
已知:![]()
(1)香料X的分子式为___________;
(2)Y是香料X的同分异构体,属于酯类,其同分异构体的总数为_____;
(3)写出反应①、③的反应类型:①_______、③________;
(4)写出下列物质的结构简式:X________、C________;
(5)写出D→E反应的化学方程式_______________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B是两种有刺激气味的气体。试根据下列实验事实填空。

(1)写出A~F各物质的化学式:
A__________、B__________、C__________、D__________、E__________、F__________。
(2)写出A、B跟水反应的离子方程式:______________________。
查看答案和解析>>
科目: 来源: 题型:
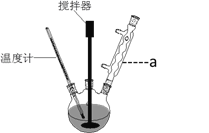
【题目】阿斯匹林的制备装置和反应原理如下:
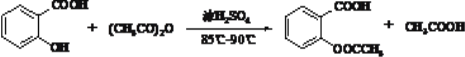
已知乙酸酐(CH3C0)2O在水中会发生水解反应生成乙酸。
实验步骤:
①开启水浴恒温槽的电源,使水浴温度控制在85℃-90℃。
②在三口瓶中加入5g水杨酸,14ml(15g)乙酸酐(CH3C0)2O,1.8ml浓硫酸。
③在水浴中,搅拌反应15min,冷却至室温,在瓶中加入70ml水,继续搅拌5min,再放在冷水浴中静置5—10min,加入冰块,在冰水浴中静置10—20min,冷却结晶,抽滤,用少量冰水洗涤2次。
④将晶体放在250ml烧杯中,并加入70ml饱和碳酸氢钠溶液,搅拌到无二氧化碳放出为止。抽滤除去聚合物固体。
⑤将滤液放在250ml烧杯中,边搅拌边慢慢滴入18%盐酸,直至PH值为1.5。烧杯放入冰水浴中冷却,直至结晶完全。真空抽滤,用少量冰水洗涤二次,得粗产品。
⑥粗产品放入150ml烧杯中,加入20ml无水乙醇,搅拌,缓慢加热,直至晶体溶解,再加入40ml水,在室温中静置,再放入冰水浴中冷却,直至结晶完全。真空抽滤,用少量无水乙醇-水(1:2,v/v)溶液洗涤,烘干,得产品。称量,计算产率。
回答以下问题:
(1)仪器a的名称为_________________
(2)反应容器干燥无水的原因是__________________________________。加入浓硫酸的目的是______________________________________。水浴加热的目的是__________________________
(3)本实验含有两个六元环和一个八元环的副产物的结构简式为__________________。
(4)加入70ml饱和碳酸氢钠溶液的目的是__________________________________。把碳酸氢钠换为氢氧化钠将使产品因________________________而损失。
(5)将滤液边搅拌边慢慢滴入18%盐酸利用了______________________________的原理。
(6)水杨酸可以在各步纯化过程和产物的重结晶过程中被除去,检验水杨酸除尽的方法是____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的有几个
①质子数相同的微粒一定属于同一种元素
②同一元素的核素种数由中子数决定
③Cl2中35C1与37Cl两种核素的个数之比与HCl中35Cl与37C1的个数之比相等
④18 g H2O中含有的中子数为10NA
⑤标准状况下,等体积CH4和HF所含的分子数相同
⑥只有活泼金属元素与活泼非金属元素之间才能形成离子键
⑦等物质的量的CN-和N2含有的共用电子对数相等
⑧通过化学变化可以实现16O与18O之间的相互转化
A. 2个 B. 3个 C. 4个 D. 5个
查看答案和解析>>
科目: 来源: 题型:
【题目】霉酚酸酯(MMF)是器官移植中抑制细胞增殖最常用的药物,它在酸性溶液中能发生如下反应:

下列说法中正确的是( )
A. 1molMMF与足量NaOH 溶液共热,最多可消耗3molNaOH
B. 可以用FeCl3溶液区别MMF与化合物Ⅰ
C. 化合物R 的分子式为C6H12NO2
D. MMF分子中含有三种官能团
查看答案和解析>>
科目: 来源: 题型:
【题目】有人设想合成具有以下结构的四种烃分子,下列有关说法不正确的是( )
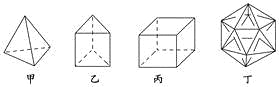
A. 1 mol甲分子内含有10 mol共价键
B. 由乙分子构成的物质不能发生氧化反应
C. 丙分子的二氯取代产物只有三种
D. 分子丁是不可能合成的
查看答案和解析>>
科目: 来源: 题型:
【题目】为了保护环境,充分利用资源,可将工业废弃物转变成重要的化工原料。回答下列问题:
(1)可用NaClO3氧化酸性FeCl2废液得到FeCl3,FeCl3具有净水作用,但腐蚀设备。
①写出NaClO3氧化酸性FeCl2的离子方程式:__________________________。
②若酸性FeCl2废液中:c(Fe2+)=2.0×10-2 mol∕L,c(Fe3+)=1.0×10-3 mol∕L,c(Cl-)=5.3×10-2 mol∕L,则该溶液的pH约为_________。
③FeCl3净水的原理是:___________________________(用离子方程式及适当文字回答);
(2)可用废铁屑为原料,按下图的工艺流程制备聚合硫酸铁(PFS),PFS是一种新型的
絮凝剂,处理污水比FeCl3高效,且腐蚀性小。

①酸浸时最合适的酸是______________。
②反应釜中加入的氧化剂,下列试剂中最合适的是____________(填标号)。
a.HNO3 b.KMnO4 c.Cl2 d.H2O2
检验其中Fe2+是否完全被氧化,应选择__________(填标号)。
a.K3[Fe(CN)6]溶液 b.Na2SO3溶液 c.KSCN溶液
③生成PFS的离子方程式为:xFe3++yH2O Fex(OH)y(3x-y)++yH+欲使平衡正向移动可采用的方法是____________(填标号)。
加入NaHCO3 b.降温 c.加水稀释 d.加入NH4Cl
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化铝(Al2O3) 和氮化硅(Si3N4)是优良的高温结构陶瓷,在工业生产和科技领域有重要用途。
(1)Al与NaOH溶液反应的离子方程式为_____________________________________。
(2)下列实验能比较镁和铝的金属性强弱的是____________(填序号)。
a.测定镁和铝的导电性强弱
b.测定等物质的量浓度的Al2(SO4)3和MgSO4溶液的pH
c.向0.1 mol/L AlCl3和0.1 mol/L MgCl2中加过量NaOH溶液
(3)铝热法是常用的金属冶炼方法之一。
已知:4Al (s)+3O2(g) =2Al2O3(s) ΔH1 = -3352 kJ/mol
Mn(s)+ O2(g) =MnO2 (s) ΔH2 = -521 kJ/mol
Al与MnO2反应冶炼金属Mn的热化学方程式是_____________________________。
(4)工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g) + 2N2(g) + 6H2(g) ![]() Si3N4(s) + 12HCl(g) △H<0
Si3N4(s) + 12HCl(g) △H<0
某温度和压强条件下,分别将0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2L密闭容器内,进行上述反应,5min达到平衡状态,所得Si3N4(s)的质量是5.60g。
①H2的平均反应速率是_________ mol/(L·min)。
②若按n(SiCl4) : n(N2) : n(H2) = 3 : 2 : 6的投料配比,向上述容器不断扩大加料,SiCl4(g)的转化率应______(填“增大”、“减小”或“不变”)。
(5)298K时,Ksp[Ce(OH)4]=1×10—29。Ce(OH)4的溶度积表达式为Ksp=_______________。
为了使溶液中Ce4+沉淀完全,即残留在溶液中的c(Ce4+)小于1×10-5mol·L-1,需调节pH为______以上。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com