
科目: 来源: 题型:
【题目】CaCO3是一种化工原料,可以通过反应生成一系列物质,如下图所示。
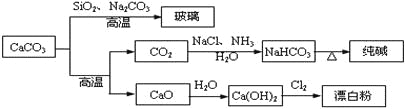
下列说法正确的是( )
A. Cl2和SO2均可以漂白有色物质,且漂白的原理相同
B. 由SiO2+ Na2CO3![]() Na2SiO3+ CO2↑可知H2CO3的酸性强于H2SiO3
Na2SiO3+ CO2↑可知H2CO3的酸性强于H2SiO3
C. 工业上,可先向饱和食盐水中通入NH3后再通入CO2制NaHCO3
D. 制取玻璃、纯碱和漂白粉所涉及的反应都是非氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】将铁的化合物溶于盐酸,滴加KSCN溶液不发生颜色变化,再加入适量氯水,溶液立即呈红色的是( )
A. FeO B. FeCl3 C. Fe2(SO4)3 D. Fe2O3
查看答案和解析>>
科目: 来源: 题型:
【题目】硼氢化钠(NaBH4)在有机合成、化工生产方面有广泛应用。制备硼氢化钠的化学方程式为NaBO2+2SiO2+4Na+2H2![]() NaBH4+2Na2SiO3。下列有关上述反应的说法错误的是( )
NaBH4+2Na2SiO3。下列有关上述反应的说法错误的是( )
A. 氧化产物和还原产物的物质的量之比为2:1
B. 转移4 mol电子时,只需向装置中通入44.8 L H2(标准状况)
C. 装药品之前加热装置至100℃并持续一会儿
D. 制备硼氢化钠的副产物可能有NaH
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA代表阿伏加德罗常数的值,下列有关叙述正确的是
A. 标准状况下,2.24LCl2与足量的NaOH溶液反应,转移的电子数目为0.2NA
B. 标准状况下,44.8 L NO与22.4 L O2混合后气体中分子总数等于2NA
C. NO2和H2O反应每生成2 mol HNO3时转移的电子数目为2NA
D. 1 mol Fe在氧气中充分燃烧失去3NA个电子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列指定反应的离子方程式正确的是
A. 向FeCl3溶液中滴加HI溶液:Fe3++2I-===Fe2++I2
B. 用铜电极电解氯化钠溶液:2Cl-+2H2O![]() Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
C. 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH4+
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2 Na+
查看答案和解析>>
科目: 来源: 题型:
【题目】目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2 (g)+4H2(g) ![]() CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升至400℃,重新达到平衡,下列表格中各物理量的变化判断正确的是
CH4(g)+2H2O(g)。已知H2的体积分数随温度的升高而增加。若温度从300℃升至400℃,重新达到平衡,下列表格中各物理量的变化判断正确的是
A. 正反应速率减小 B. 逆反应速率增大
C. 平均相对分子质量不变 D. 转化率增大
查看答案和解析>>
科目: 来源: 题型:
【题目】已知 A、B、C、D、E 是化学中常见的物质。常温下,E 是一种无色无味的液体,它们之间有如下反应关系。

(1)若 A 是一种具有磁性的黑色金属氧化物,B 是一种常见的非氧化性酸,A 和 B 反应的离子方程式为________;若在生成物 C 中继续滴加氢氧化钠溶液,会观察到生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色,写出白色沉淀发生化学反应的方程式________________________________。A 与 CO 高温下反应可得到金属单质,写出该金属单质与水蒸气反应的化学方程式________________________________。
(2)若实验室中利用固体 A 和 B 的反应制备气体 C,C 是一种无色、刺激性气味、密度比空气小、碱性的气体,试写出此反应的化学方程式________________________________;实验室检验 C 的方法为________________________________。
(3)若 B 是黄绿色有毒气体,上述关系经常用于实验室尾气处理,则反应的离子方程式为
________________________________。若用湿润的淀粉碘化钾试纸靠近盛满 B 的试管口,看到的现象为________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组欲探究SO2的化学性质,设计了如下实验方案。
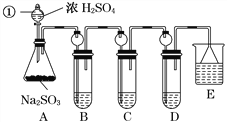
(1)指出仪器①的名称:______________。
(2)检查A装置的气密性的方法是______________________________________________。
(3)装置B检验SO2的氧化性,则B中所盛试剂可以为________。
(4)装置C中盛装溴水用以检验SO2的________性,则C中反应的离子方程式为
________________________________________________________________________。
(5)装置D中盛装新制漂白粉浓溶液,通入SO2一段时间后,D中出现了大量白色沉淀。同学们对白色沉淀成分提出三种假设:
①假设一:该白色沉淀为CaSO3;
假设二:该白色沉淀为__________________________________________________;
假设三:该白色沉淀为上述两种物质的混合物。
②基于假设一,同学们对白色沉淀成分进行了探究。设计如下方案:
限选的仪器和试剂:过滤装置、试管、滴管、带导管的单孔塞、蒸馏水、0.5 mol·L-1HCl、0.5 mol·L-1H2SO4、0.5 mol·L-1BaCl2、1 mol·L-1NaOH、品红溶液。
第1步,将D中沉淀过滤、洗涤干净,备用。
请回答洗涤沉淀的方法:____________________________________________________。
第2步,用另一只干净试管取少量沉淀样品,加入________(试剂),塞上带导管的单孔塞,将导管的另一端插入盛有________(试剂)的试管中。若出现__________________现象,则假设一成立。
③若假设二成立,试写出生成该白色沉淀的化学方程式:_________________________________。
(6)装置E中盛放的试剂是________,作用是__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com