
科目: 来源: 题型:
【题目】下列指定微粒的数目相等的是
A. 等质量的乙烯和丙烯中含有的共用电子对数
B. 等物质的量的水与重水含有的中子数
C. 同温、同压、同体积的CO和NO含有的质子数
D. 等物质的量的铁和铝分别与足量盐酸完全反应时转移的电子数
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A. 乙烯使溴水或酸性高锰酸钾褪色均属于加成反应
B. 利用溴水能鉴别苯、乙醇和乙酸三种溶液
C. 用重铬酸钾溶液检验司机是否酒驾所发生的反应属于乙醇的氧化反应
D. 石油的分馏、煤的干馏都是物理变化,而裂化、裂解是化学变化
查看答案和解析>>
科目: 来源: 题型:
【题目】某地煤矸石经预处理后含SiO2(63%)、Al2O3(25%)、Fe2O3(5%)等,一种综合利用工艺设计如下:
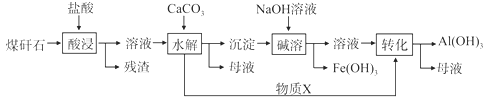
(1)物质X的化学式为__________________
(2)“酸浸”过程中主要反应的离子方程式为:________________,________________
(3)“碱溶”的目的是___________________
(4)从流程中分离出来的Fe(OH)3沉淀可在碱性条件下用KClO溶液处理,制备新型水处理剂高铁酸钾(K2FeO4),该反应的离子方程式为:_________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是
A. 有能量变化的过程均为化学变化
B. 氢氧化钡晶体与氯化铵晶体的反应为放热反应
C. 反应物的总能量高于生成物的总能量时发生放热反应
D. 旧化学键断裂所放出的能量低于新化学键形成所吸收的能量时发生吸热反应
查看答案和解析>>
科目: 来源: 题型:
【题目】锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]________,有________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是_______________________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_____________________。
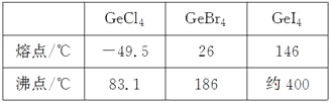
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是________________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为____________,微粒之间存在的作用力是________________。
(6)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置,下图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(1/2,0,1/2);C为(1/2,1/2,0)。则D原子的坐标参数为________。
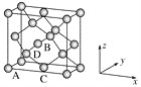
②晶胞参数,描述晶胞的大小和形状,已知Ge单晶的晶胞参数a=565.76 pm,其密度为________g·cm-3(列出计算式即可)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6 LH2(标准状况下)。
①合金中镁的物质的量_________。
②写出该合金溶于足量NaOH溶液的化学方程式_________________。同时产生H2的体积(标准状况下)为____________ 。
(2)相同条件下,某Cl2与O2混合气体100 mL恰好与150 mL H2化合生成HCl和H2O,则混合气体中Cl2与O2的体积比为__________,混合气体的平均相对分子质量为____________。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为____________。
(4)在同温、同压下,实验测得CO、N2和O2三种气体的混合气体的密度是H2的14.5倍,其中O2的质量分数为____________ (计算结果保留1位小数) 。若其中CO和N2的物质的量之比为1∶1,则混合气体中氧元素的质量分数为_______________ (计算结果保留1位小数)。
查看答案和解析>>
科目: 来源: 题型:
【题目】已知五种元素的原子序数的大小顺序为C>A>B>D>E,A,C同周期,B,C同主族。A与B形成的离子化合物A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子的分子。试回答下列问题:
(1)写出五种元素的元素符号:A:________、B:________、C:________、D:________、E:________。
(2)用电子式表示离子化合物A2B的形成过程:______________________。
(3)写出下列物质的电子式:
①D元素形成的单质:_______________________________________________。
②E与B形成的化合物:_____________________________________________。
③A,B,E形成的化合物:___________________________________________。
④D与E形成的化合物:______________________________________________。
⑤C,D,E形成的离子化合物:________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】微型化学实验可以有效实现化学实验绿色化的要求。如下图所示在一块衬白纸的玻璃片的不同位置分别滴加浓度为0.1mol/L的KI(含淀粉溶液)、NaOH的酚酞(C20H14O4)试液、FeCl2(含KSCN)溶液各一滴,在圆心处放置一粒芝麻大小的KMnO4的晶体,向KMnO4的晶体上滴加一滴浓盐酸,再立即用表面皿盖好根据上述描述涉及到的元素,回答下列问题:
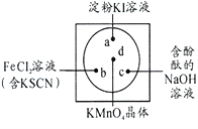
(1)a中反应的化学反应方程式为________________________________________证明KI中含有钾元素的方法是:____________________________。
(2)c中反应的离子反应方程式为_______________________________________b中的现象是________________________________________________。
(3)短周期原子半径最大的原子共有______种不同能量的电子。它与同周期原子半径最小元素形成晶体,该晶体中每个阳离子周围距离最近有_______个阴离子。
(4)把少许 KMnO4撒入盛水烧杯中溶解,包含物理过程(即__________过程和化学过程(即_____________过程。所以,溶液中的有色离子应该是__________________(写名称)
(5)NH3与H2O分别能与H+结合成NH4+与H3O+。与NH4+具有相同空间构型的微粒是_______;
a.H3O+b.CH4c.P4d.NH3
(6)加碘盐中含碘量为20mg~50mg/kg。制取加碘盐(含KIO3的食盐)1000kg,若用KI与 Cl2反应制KIO3,至少需要消耗Cl2___________________L(标准状况,保留2位小数)
查看答案和解析>>
科目: 来源: 题型:
【题目】俄罗斯科学家用含20个质子的钙的一种原子轰击含95个质子的镅原子,结果4次成功合成4个第115号元素的原子。这4个原子生成数微秒后衰变成第113号元素。下列有关叙述正确的是
A. 115号元素在第六周期
B. 113号元素在第七周期ⅢA族
C. 115号和113号元素都是非金属元素
D. 镅元素和115号元素不在同一周期
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com