
科目: 来源: 题型:
【题目】对乙烯基苯甲酸是重要的医药中间体,广泛应用于合成感光材料。对乙烯基苯甲酸可通过如下反应合成。
反应①: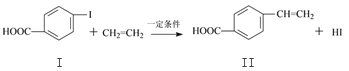
(1)下列关于化合物I和化合物Ⅱ的说法,正确的是______________。
a.化合物I能与新制的Cu(OH)2反应 b.均可发生酯化反应和银镜反应
c.化合物Ⅱ能使KMnO4溶液褪色 d.1 mol化合物Ⅱ最多能与5 mol H2反应
(2)化合物Ⅱ在催化剂条件下生成高分子化合物的反应方程式为_____________。
(3)化合物Ⅱ可由芳香族化合物Ⅲ通过消去反应获得,Ⅲ和Cu共热的产物能发生银镜反应,写出化合物Ⅲ的结构简式__________________________。
(4)化合物Ⅳ是化合物Ⅱ的同分异构体,且化合物Ⅳ遇FeCl3溶液显紫色,苯环上的一氯代物只有2种,写出化合物Ⅳ的结构简式________________________(写一种)。
查看答案和解析>>
科目: 来源: 题型:
【题目】完成下列空白。
(1)“辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,下图是异辛烷的球棍模型,则异辛烷的系统命名为_________________。
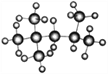
(2)写出下列反应的化学方程式和反应类型
①2—溴丙烷与NaOH溶液:________________________。
②苯酚和饱和溴水:____________________________。
(3)有机物A可以通过不同的反应得到B和C:
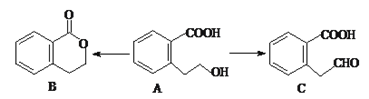
①A的分子式为___________________,C的含氧官能团名称为___________________。
②A制取B的有机反应类型为________________。
③A制取C的化学方程式为:_____________________________________________。
④A发生消去反应后产物的结构简式为___________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】计算后填空:
(1)在标准状况下,448 mL某气体的质量为0.64 g,这种气体的相对分子质量为________。
(2)某氯化铁与氯化钠的混合液,已知c(Fe3+)=0.2 mol·L-1,c(Cl-)=1 mol·L-1。则c(Na+)为________。
(3)19 g某二价金属的氯化物RCl2中含有0.4 mol的Cl-,则R的相对原子质量为__________。
(4)500mL Fe2(SO4)3溶液中含Fe3+ 28 g,则溶液中SO42-的物质的量浓度为________mol·L-1。
(5)在无土栽培中,配制1 L含5 mol NH4Cl、1.6 mol KCl、2.4 mol K2SO4的某营养液,若用KCl、NH4Cl、(NH4)2SO4配制,则需KCl、NH4Cl的物质的量分别为________、________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一种瑞香素的衍生物的结构简式如图,下列有关该有机物性质的说法正确的是

A. 不能与FeCl3溶液发生显色反应
B. 1 mol该有机物最多可与3 mol H2加成
C. 1 mol该有机物最多可与含5 mol NaOH溶液反应
D. 1 mol该有机物与足量NaHCO3溶液反应可放出3 mol CO2
查看答案和解析>>
科目: 来源: 题型:
【题目】制得的碳酸钠样品中往往含有少量NaCl,现欲测定样品中Na2CO3的质量分数,某探究性学习小组分别设计了如下实验方案。请回答下列有关问题:
方案一:把一定质量的样品溶解后加入过量的CaCl2溶液,将所得沉淀____________(填操作名称)、洗涤、烘干、称量、计算。洗涤沉淀的具体操作是_____________________________。
方案二:把一定量的样品与足量硫酸反应后,用下图所示装置测定产生CO2的体积,为了确保测定结果的准确性,B中的溶液最好采用_________________。下图装置中实验仪器a的名是_________________。

方案三:利用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去)。实验步骤如下:
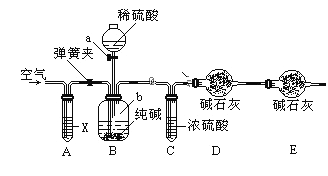
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰的干燥管D的质量为33.4g;
③准确称得6g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为35.6g。
(1)若④⑤两步的实验操作太快,则会导致测定结果__________(填“偏大”或“偏小”)。
(2)装置A中试剂X应选用________________________。
(3)E装置的作用是_______________________________。
(4)根据实验中测得的有关数据,计算纯碱样品Na2CO3的质量分数为___________(结果保留小数点后一位)。
查看答案和解析>>
科目: 来源: 题型:
【题目】高锰酸钾溶液在酸性条件下可以与硫酸亚铁反应,化学方程式如下(未配平):KMnO4+FeSO4+H2SO4―→K2SO4+MnSO4+Fe2(SO4)3+H2O。下列说法正确的是
A. Fe2+的还原性强于Mn2+
B. MnO4-是氧化剂,Fe3+是还原产物
C. 生成1 mol水时,转移1.25 mol电子
D. 取反应后的溶液加KSCN溶液,可观察到有血红色沉淀生成
查看答案和解析>>
科目: 来源: 题型:
【题目】能正确表达下列反应的离子方程式为( )
A. 用稀盐酸除去水垢:2H++CaCO3===Ca2++CO2↑+H2O
B. 硫化亚铁与浓硫酸混合加热:2H++FeS===H2S↑+Fe2+
C. 向硫酸铝溶液中滴加碳酸钠溶液:2Al3++3CO32-===Al2(CO3)3↓
D. Na2O2溶于水产生O2∶Na2O2+H2O===2Na++2OH-+O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】海水是巨大的资源宝库。下图是从海水中提取食盐和溴的主要流程。

(1)粗盐除含 NaCl 外,还含有少量 MgCl2、 CaCl2、 Na2SO4以及泥沙等杂质。以下是粗盐提纯的
操作流程。

提供的试剂:
Na2CO3溶液、 K2CO3溶液、 NaOH 溶液、 BaCl2溶液、 Ba(NO3)2溶液、饱和 NaCl 溶液。
①除去溶液 I 中的 MgCl2、 CaCl2、 Na2SO4,从提供的试剂中选出 a 所代表的试剂,按滴加顺序依次为: 过量的NaOH 溶液、_______、_______;
②如何证明操作①中 NaOH 溶液已经过量?_______。
③蒸发过程所用的主要仪器有:铁架台、酒精灯、_______;
(2)某同学在实验室中用四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
①分离出四氯化碳层的操作是:_______。
②分离溴的四氯化碳溶液的操作方法是:_______。
(3)工业上将较高浓度的溴水经进一步处理得到工业溴。某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料, Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性。水的沸点为 100℃。他们参观生产过程后,设计了如下装置简图:

①图中仪器 B 的名称:_______。
②用热水浴加热的优点是:_______。
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为:_______℃。
查看答案和解析>>
科目: 来源: 题型:
【题目】某课外小组对金属钠进行了研究。已知C、D都是单质,F的水溶液是一种常见的强酸。
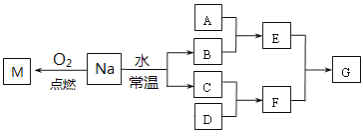
(1)F的名称是:______________
(2)金属Na在空气中放置足够长时间,最终的生成物是:________________
(3)该小组同学应该如何取用金属钠:_________________________________________
(4)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是_________________________。
(5)若A是一种不稳定的盐,A溶液与B溶液混合将产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,请写出该过程的离子方程式:___________________

(6)若A是一种溶液,只可能含有H+、NH4+、Mg2+、Fe3+、Al3+、CO32-、SO42-中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如右图所示,由此可知,该溶液中肯定含有的离子及其物质的量浓度之比为__________________________。
(7)将NaHCO3与M的混合物在密闭容器中充分加热后排出气体,经测定,所得固体为纯净物,则NaHCO3与M的质量比为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com