
科目: 来源: 题型:
【题目】Fe(OH)3胶体的制备方法:________________________化学方程式为_____________________。FeCl3净水的原理__________(离子方程式解释)
查看答案和解析>>
科目: 来源: 题型:
【题目】镭是周期表中第7周期第ⅡA主族元素,下列关于镭的性质描述中不正确的是
A. 在化合物中呈+2价 B. 镭比钙的金属性强
C. 氢氧化物呈两性 D. 碳酸盐难溶于水
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于化学平衡常数K的说法中,正确的是( )
A. 对于某一反应来说,K是定值,不随外界条件的改变而改变
B. K越大,化学反应速率越快
C. K越大,反应进行得越彻底
D. 使用合适的催化剂,既可以改变反应速率,也可以改变平衡常数K
查看答案和解析>>
科目: 来源: 题型:
【题目】科学史上每一次重大发现都极大地推进了科学的发展。俄国科学家门捷列夫对化学的突出贡献在于( )
A.发现了元素周期律B.提出了原子分子学说
C.揭示了燃烧的本质D.提取了治疟药物青蒿素
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法错误的是( )
A. 从CH4、NH4+、SO42-为正四面体结构,可推测PH4+、PO43-也为正四面体结构
B. 1mol碳化硅晶体中,平均含有4mol C—Si共价键
C. 水的沸点比硫化氢的高,是因为H2O分子间存在氢键,H2S分子间不能形成氢键
D. 某气态团簇分子结构如图所示,该气态团簇分子的分子式为EF或FE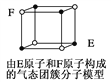
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)在标准状况下3.2g CO与CO2的混合气体,体积为2.24L。则:混合气体的平均摩尔质量是________ CO2和CO的体积之比是________ CO2和CO的质量之比是_______,混合气体中所含氧原子的物质的量是_______
(2)若10 g密度为ρ g·cm-3的Ca(NO3)2溶液中含有4 g Ca2+,则溶液中NO3-的物质的量浓度为____________
(3)在标准状况下,将V L A气体(摩尔质量为M g·mol-1)溶于0.1 L水中,所得溶液的密度为ρ g·cm-3,则此溶液的物质的量浓度(mol·L-1)为 ____________________
(4)在反应3BrF3+5H2O===9HF+Br2+HBrO3+O2↑中,若有2molH2O参加反应,有_____mol水作还原剂,被水还原的溴元素____________mol;
(5)把V L含MgSO4和K2SO4的混合溶液分成五等份,一份加入含a mol NaOH的溶液恰好使镁离子完全沉淀;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为_______
(6)3.04g铜镁合金完全溶解于50mL密度为1.40g·mL-1、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体2240mL(标准状况),向反应后的溶液中加入1.0mol·L-1NaOH溶液,当金属离子全部沉淀时,得到5.08g沉淀,则该浓硝酸中HNO3的物质的量浓度是 ___mol·L-1,镁的质量为______g,NO2和N2O4的混合气体中,NO2的体积分数是___,得到5.08g沉淀时,加入NaOH溶液的体积是____mL。
(7)在100mL FeBr2溶液中通入2.24L Cl2(标准状况),溶液中有1/3的溴元素被氧化成单质Br2,则原FeBr2溶液中FeBr2的物质的量浓度为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】将一定量的氯气通入30 mL浓度为10.00 mol·L-1的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系。下列判断正确的是
A. 与NaOH反应的氯气一定为0.3 mol
B. n(Na+)∶n(Cl-)可能为7∶3
C. 若反应中转移的电子为n mol,则0.15<n<0.25
D. n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列示意图与对应的反应情况符合的是
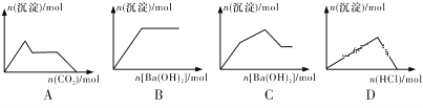
A. 向含0.01mol KOH和0.01mol Ca(OH)2的混合溶液中缓慢通入CO2至过量
B. 向NaHSO4溶液中逐滴加入Ba(OH)2溶液至过量
C. 向KAl(SO4)2溶液中逐滴加入Ba(OH)2溶液至过量
D. 向NaAlO2溶液中逐滴加入盐酸至过量
查看答案和解析>>
科目: 来源: 题型:
【题目】我们在学习和生活过程中所观察的以下现象与电化腐蚀有关的是
A. 光亮的自行车钢圈不易生锈
B. 炒过菜的铁锅未及时洗净出现红褐色锈斑
C. 光亮的铜丝在火焰上灼烧后变黑
D. 实验室镁带拆封放置一段时间后表面变灰暗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com