
科目: 来源: 题型:
【题目】将30 mL 0.5 mol·L-1 NaOH溶液加水稀释到500 mL,关于稀释后的溶液叙述不正确的是( )
A. 浓度为0.03 mol·L-1 B. 从中取出10 mL溶液,其浓度为0.03 mol·L-1
C. 含NaOH 0.6 g D. 从中取出10 mL溶液,含NaOH 0.015 mol
查看答案和解析>>
科目: 来源: 题型:
【题目】Ⅰ.已知有机物A是最简单的烷烃,有机物B含有与A相同数目的氢原子,B分子中碳、氢的质量分数分别是40%、6.6%,其余为氧。请通过计算回答:
(1)该有机物B的分子式是_____________。
(2)若有机物B在核磁共振氢谱图(1H—NMR)上有三个峰,其结构简式为_______________。
Ⅱ.只含C、H、O三种元素的有机化合物R的相对分子质量大于110,小于150。经分析得知,其中碳和氢的质量分数之和为52.24%。请通过计算回答:
(1)该有机物R的分子式是_______________。
(2)该有机物R分子中最多含________个碳氧双键。
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组设计用50 mL1.0mol/L盐酸和50 mL1mol/L氢氧化钠溶液在如图装置中进行中和反应。通过测定反应过程中所放出的热量计算中和热。试回答下列问题:

(1)本实验中在大小烧杯中填充泡沫塑料的作用是______
(2)使盐酸与NaOH溶液混合均匀的正确操作是______(填字母)。
a.用温度计小心搅拌 b.揭开硬纸片用玻璃棒搅拌
c.轻轻地振荡烧杯 d.用套在温度计上的环形玻璃棒轻轻地搅动
(3)该实验小组做了四次实验,每次取溶液各50mL,记录如下原始数据。
实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差平均值(t2-t1)/℃ | ||
盐酸 | NaOH溶液 | 平均值 | |||
1 | 25.1 | 24.9 | 25.0 | 31.6 | |
2 | 25.1 | 25.1 | 25.1 | 28.5 | |
3 | 25.1 | 25.1 | 25.1 | 31.9 | |
4 | 25.1 | 25.1 | 25.1 | 31.8 | |
①结合上表数据,计算时应采用温度差的平均值为______℃。
②已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混合液的比热容c=4.18×103kJ/(g·℃),则中和热ΔH=_____(保留到小数点后1位)。
(4)若因反应放热,而造成少量盐酸在反应过程中挥发,则测得的中和热_______(填“偏大”“偏小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与![]() ===
===![]() 相比较,水的作用不相同的是( )
相比较,水的作用不相同的是( )
A. ![]() ===
===![]() ↑
↑
B. ![]() ===
===![]()
C. ![]() ===
===![]()
D. ![]() ===
===![]() ↑
↑
查看答案和解析>>
科目: 来源: 题型:
【题目】氢化钠(NaH)是一种白色的离子化合物,其中钠显+1 价,NaH 与水反应放出氢气。下列叙述正确的是( )
A. NaH 在水中显酸性 B. 钠与其他碱金属都必须保存在煤油中
C. NaH 中氢离子半径比锂离子半径大 D. NaH 中氢离子被还原为氢气
查看答案和解析>>
科目: 来源: 题型:
【题目】香料甲和G都在生活中有很多用途,其合成路线如下:

已知:①R1—CHO+R2—CH2—CHO![]()
![]() (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)
②D与A互为同系物;在相同条件下,D蒸气相对于氢气的密度为39。
请回答下列问题:
(1)G中含氧官能团的名称是_______________,写出一种能鉴别A和D的试剂:________________。
(2)②的反应类型是____________,B和F的结构简式分别为______________、___________________。
(3)写出反应①的化学方程式_________________________________________________。
(4)C有多种同分异构体,其中属于芳香族化合物的还有_______种。
(5)G的同分异构体 是一种重要的药物中间体,其合成路线与G相似,请以
是一种重要的药物中间体,其合成路线与G相似,请以![]() 为原料设计它的合成路线(其他所需原料自选),写出其反应流程图:_____________________________________________________________________。
为原料设计它的合成路线(其他所需原料自选),写出其反应流程图:_____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有A、B、C、D、E、F六种元素,试按下述所给的条件推断:①A、B、C是同一周期的金属元素,已知原子核外有3个电子层,A的原子半径在所属周期中最大且原子半径A>B>C;②D、E是周期表中位置相邻的非金属元素,它们跟氢化合可生成气态氢化物HD和HE,在室温时,D的单质是液体,E的单质是固体;③F是除氢外原子半径最小的主族元素。
(1)A元素的名称___,B元素在周期表中的位置为___,C元素的离子结构示意图_____。
(2)E元素的单质颜色_____。
(3)在上述六种元素最高价氧化物对应的水化物中,碱性最强的化学式______,酸性最强的化学式____,气态氢化物最稳定的化学式______。
(4)A、C元素最高价氧化物对应的水化物反应的离子方程式_______。
(5)用电子式表示A元素与D元素形成化合物的过程___________。
(6)F元素的单质与水反应的化学方程式__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列有关化学用语表示正确的是( )
A. 乙醇的结构简式:C2H6O
B. 氨基的电子式: ![]()
C. 镁离子的结构示意图:![]()
D. 制备Fe(OH)3胶体的离子方程式:Fe3++3H2O![]() Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
查看答案和解析>>
科目: 来源: 题型:
【题目】一种重要的有机化工原料有机物X,如图是以它为初始原料设计出的转化关系图(部分产物、合成路线、反应条件略去)。Y是一种功能高分子材料。
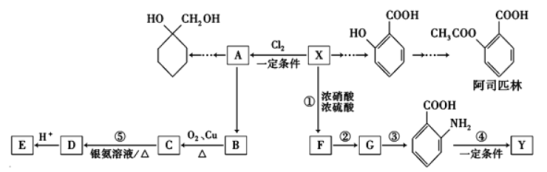
已知:①X为芳香烃,其相对分子质量为92
②烷基苯在高锰酸钾的作用下,侧链被氧化成羧基:![]()
③ ![]() (苯胺,易被氧化)
(苯胺,易被氧化)
请根据本题所给信息与所学知识回答下列问题:
(1)X的分子式为_____________;
(2)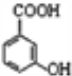 中官能团的名称为___________________;
中官能团的名称为___________________;
(3)反应③的反应类型是_____________;已知A为一氯代物,则E的结构简式为_______________;
(4)反应④的化学方程式为_______________________________________;
(5)阿司匹林有多种同分异构体,满足下列条件的同分异构体有_______种:
①含有苯环;
②既不能发生水解反应,也不能发生银镜反应;
③1mol该有机物能与2molNaHCO3完全反应.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com