
科目: 来源: 题型:
【题目】实验室模拟工业漂白液(有效成分为NaClO)脱除废水中氨氮(NH3)的流程如下:
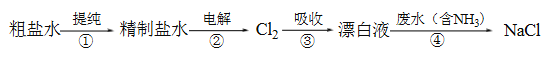
下列分析正确的是
A. ①中采用蒸馏的方法精制粗盐水
B. ②中阳极的主要电极反应:4OH- - 4e- = 2H2O + O2↑
C. ③中制备漂白液的反应:Cl2 + OH- = Cl- + HClO
D. ②、③、④中均发生了氧化还原反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在反应3NO2+H2O=2HNO3+NO中,若NA为阿伏加德罗常数,下列说法正确的是
A.NO2只是氧化剂B.H2O既不是氧化剂,也不是还原剂
C.NO2只是还原剂D.每生成1mol NO,转移1 NA电子
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各种关于酸的使用,其中正确的是
A. 为了抑制Fe2+的水解,用稀硝酸酸化 B. 检验溶液中是否含有SO42—时,先用盐酸酸化
C. 检验氯乙烷中的氯元素,水解后再用硫酸酸化 D. 为了增强KMnO4溶液的氧化能力,用浓盐酸酸化
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物I(分子式为C19H20O4)属于芳香酯类物质,是一种调香剂,其合成路线如下:

已知:①A属于脂肪烃,核磁共振氢谱显示有2组峰,面积比为3:1,其蒸汽在标准状况下密度为2.5g·L-1;D分子式为C4H8O3;E分子式为C4H6O2,能使溴水褪色。
② 其中R为烃基
其中R为烃基
③ 其中R1和R2均为烃基
其中R1和R2均为烃基
回答下列问题:
(1)A的结构简式为________________________________;
(2)反应④的化学方程式为_________________________________;
(3)E的同系物K比E多一个碳原子,K有多种链状同分异构体,其中能发生银镜反应且能水解的有______________种;
(4)反应①~⑦属于取代反应的是________________________(填序号);
(5)反应⑦的化学方程式为________________________________;
(6)参照上述合成路线,以  为原料(无机试剂任选),经4步反应制备可降解塑料
为原料(无机试剂任选),经4步反应制备可降解塑料 ________________________。
________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列热化学方程式书写正确的是
A. 2SO2 + O2=2SO3 △H=-196.6 kJ/mol
B. H2(g)+1/2O2(g)==H2O (g) △H=-241.8 kJ
C. 2H2(g)+O2(g)== 2H2O(l) △H=-571.6 kJ/mol
D. C(s) + O2(g)== CO2(g) △H= + 393.5 kJ/mol
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与社会、生活密切相关,下列说法不正确的是
A. 天然气是高效清洁燃料和重要的化工原料
B. 人造放射性同位素,在工农业、医疗等方面有重要用途
C. 氢键在生命现象中也起着重要作用
D. 芳香族化合物都有芳香性气味
查看答案和解析>>
科目: 来源: 题型:
【题目】硫代硫酸钠又名大苏打、海波,可以用于治疗氰化物中毒等,某化学兴趣小组通过查阅资料,设计了如下的装置(略去部分夹持仪器)来制取Na2S2O3·5H2O晶体并探究其性质。

已知烧瓶C中发生如下三个反应:
Na2S(aq)+H2O(l)+SO2(g) = Na2SO3(aq)+H2S(aq)
2H2S(aq)+SO2(g) =3S(s)+2H2O(l) ;S(s)+Na2SO3(aq) ![]() Na2S2O3(aq)
Na2S2O3(aq)
(1)装置B的作用之一是观察SO2的生成速率。控制SO2生成速率可以采取的措施有_________________________(写一条)
(2)常温下,用pH试纸测定0.1 mol·L-1 Na2S2O3溶液pH值约为8,测定时的具体操作是_______________________________。
(3)向新制氯水中滴加少量Na2S2O3溶液,氯水颜色变浅,有硫酸根离子生成,写出该反应的离子方程式_____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学设计实验制备2-羟基-4-苯基丁酸乙酯,反应原理、装置和数据如下:


相对分子质量 | 密度(g/cm3) | 沸点(℃) | 水溶性 | |
2-羟基-4-苯基丁酸 | 180 | 1.219 | 357 | 微溶 |
乙醇 | 46 | 0.789 | 78.4 | 易溶 |
2-羟基-4-苯基丁酸乙酯 | 208 | 1.075 | 212 | 难溶 |
实验步骤:
①如图1,在干燥的圆底烧瓶中加入20mL2-羟基-4-苯基丁酸、20mL无水乙醇和适量浓硫酸,再加入几粒沸石;
②加热至70℃左右保持恒温半小时;
③分离、提纯三颈瓶中的粗产品,得到有机粗产品;
④精制产品。
请回答下列问题:
(1)油水分离器的作用为____________________。实验过程中发现忘记加沸石该如何操作_______________________。
(2)本实验采用____________加热方式(填“水浴”、“油浴”或“酒精灯加热”)。
(3)取三颈烧瓶中的混合物分别用水、饱和碳酸氢钠溶液和水洗涤。第二次水洗的目的是___________________。
(4)在精制产品时,加入无水MgSO4的作用为___________________;然后过滤,再利用如图2装置进行蒸馏纯化,图2装置中的错误有__________________________。
(5)若按纠正后的操作进行蒸馏纯化,并收集212℃的馏分,得2-羟基-4-苯基丁酸乙酯约9.0g。则该实验的产率为__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列反应的方程式:①2Fe3++2I-=2Fe2++I2;②Br2+2Fe2+=2Br-+2Fe3+,可判断各物质的氧化性由强到弱的顺序是
A.Fe3+、Br2、I2B.Fe3+、I2、Br2
C.Br2、Fe3+、I2D.Br2、I2、Fe3+
查看答案和解析>>
科目: 来源: 题型:
【题目】下列溶液中,溶质的物质的量浓度为1mol/L的是( )
A. 含Na+为2mol的Na2SO4溶液
B. 将80g SO3溶于水并配成1L的溶液
C. 将0.5mol/L的某饱和溶液100mL,加热蒸发掉50g水后的溶液
D. 将58.5gNaCl溶于1L水所得的溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com