
科目: 来源: 题型:
【题目】用下列实验装置完成对应的实验(部分仪器略去),能达到实验目的是( )
A.  制取乙酸乙酯
制取乙酸乙酯
B.  吸收NH3
吸收NH3
C.  石油的分馏
石油的分馏
D.  比较盐酸、碳酸、苯酚的酸性强弱
比较盐酸、碳酸、苯酚的酸性强弱
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室用密度为1.18g/ml,质量分数为36.5%浓盐酸配制250ml0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250ml0.1mol/L的盐酸溶液.应量取盐酸体积_________ml,应选用容量瓶的规格__________________ml。
(2)配制时,其正确的操作顺序是________。
A.用30ml水洗涤烧杯 2﹣3次,洗涤液均注入容量瓶,振荡
B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30ml),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入250ml的容量瓶中
D.将容量瓶盖紧、振荡、摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1﹣2cm处
a.BCAFED b.BCFED c.BCAED
(3)操作B中,使用量筒量取液体时视线俯视会造成配制液体浓度__________(偏高、偏低或无影响)。操作E中加水超过刻度线该如何处理?____________
(4)若出现如下情况,对所配溶液浓度将有何影响(偏高、偏低或无影响)?
a.没有进行A操作____________;
b.加蒸馏水时不慎超过了刻度___________;
c.定容时俯视_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有关溴乙烷的下列叙述中,正确的是( )
A. 在溴乙烷中滴入AgNO3溶液,立即有淡黄色沉淀生成
B. 溴乙烷不溶于水,能溶于大多数有机溶剂
C. 溴乙烷与NaOH的醇溶液反应,可生成乙醇
D. 溴乙烷通常用溴水与乙烷直接反应来制取
查看答案和解析>>
科目: 来源: 题型:
【题目】保龄球与竹签可以用来制作有机分子球棍模型,保龄球代表有机分子中的原子,且保龄球个数和大小分别代表有机分子中的原子个数和类型;竹签代表有机分子中原子间结合的化学键,并以竹签的数目和类型代表化学键的数目和类型,下列关于用保龄球和竹签制作分子球棍模型的判断,正确的是( )
A. 甲烷的球棍模型需要用五个保龄球和五根竹签制作
B. 甲烷球棍模型中,较大的保龄球代表甲烷分子中的氢原子
C. 甲烷的球棍模型中,五个保龄球的球心不在同一平面上
D. 制作乙烯的模型时,需要用到六根完全相同的竹签
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中产生气泡速率最快的是( )
选项 | 温度 | 浓度 | 外加物质 |
A | 25℃ | 2 mL5%H2O2 | 2滴0.1mol·L-1FeCl3 |
B | 35℃ | 2mL8%H2O2 | 无 |
C | 35℃ | 2mL8%H2O2 | MnO2粉末 |
D | 25℃ | 2mL8%H2O2 | MnO2粉末 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】下面关于硅及其化合物的叙述中,不正确的是
A.普通玻璃是以纯碱、石灰石和石英为原料在玻璃窑中熔融制成
B.玻璃、陶瓷、水泥、碳化硅都属于传统的硅酸盐产品
C.硅胶可用作食品干燥剂及催化剂的载体
D.硅元素是一种亲氧元素,其中[SiO4]四面体结构存在于二氧化硅和硅酸盐矿中
查看答案和解析>>
科目: 来源: 题型:
【题目】有机物H是一种重要的高分子化合物,其合成路线如下:

已知:
请回答下列问题:
(1)A的名称是_______________,C中含氧官能团名称是______________。
(2)写出反应类型:A→B______________,C→D__________________。
(3)B→C的反应试剂和反应条件是______________________。
(4)D+E→F的反应方程式是_________________。
(5)G的分子式是____________________。
(6)满足下列条件的F的同分异构体共有__________种(不考虑立体异构)。
a.苯环上有两个取代基,无其他环状结构;b.含碳碳三键,无-C≡COH结构。
(7)多环化合物是有机研究的重要方向,请设计由![]() 、.CH3CHO、
、.CH3CHO、![]() -CHO合成多环化合物
-CHO合成多环化合物 的路线(无机试剂任选)______________
的路线(无机试剂任选)______________
查看答案和解析>>
科目: 来源: 题型:
【题目】能够充分说明在恒温下的密闭容器中,反应H2(g)+I2(g)![]() 2HI(g)已达到平衡状态的标志是
2HI(g)已达到平衡状态的标志是
A. 容器中H2、I2、HI的物质的量之比为1:1:2
B. H2、I2、HI在密闭容器中共存
C. 单位时间内生成2molHI 时,即消耗1molH2
D. 2 v正(H2)=v逆(HI)
查看答案和解析>>
科目: 来源: 题型:
【题目】已知酸性高锰酸钾溶液可以将FeSO4氧化,方程式为:2KMnO4+10FeSO4+8H2SO4=K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示.则下列有关说法错误的是( )
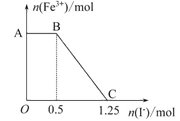
A. 图中AB段主要是高锰酸钾和碘化钾溶液反应
B. 图中BC段发生的反应为2Fe3++2I-=2Fe2++I2
C. 根据OC段的数据可知开始加入的硫酸亚铁的物质的量为1.25mol
D. 根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com