
科目: 来源: 题型:
【题目】如图所示(B中冷却装置未画出),将氯气和空气(不参与反应)以体积比约1∶3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O制备次氯酸溶液。
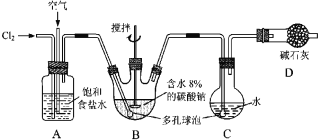
已知:Cl2O极易溶于水并与水反应生成HClO;Cl2O的沸点为3.8 ℃,42 ℃以上分解为Cl2和O2。
(1)①实验中控制氯气与空气体积比的方法是________________________________。
②为使反应充分进行,实验中采取的措施有______________________________。
③装置D的作用是____________________________________。
(2)①装置B中产生Cl2O的化学方程式为:____________________________________。
②若B无冷却装置,则进入C中的Cl2O会大量减少。其原因是_____________________。
(3)装置C中采用棕色圆底烧瓶是因为______________________________________。
(4)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定C中次氯酸溶液的物质的量浓度的实验方案为:用_____取20.00 mL次氯酸溶液,加入足量的_________________,再加入足量的_______________,过滤,洗涤沉淀,在真空干燥箱中干燥,用电子天平称量沉淀质量。 (可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液)。
查看答案和解析>>
科目: 来源: 题型:
【题目】X、Y、Z、L、M为原子序数依次增大的短周期元素,周期表中X原子半径最小,Y元素形成化合物种类最多,Z元素的氢化物水溶液呈碱性,常温下L可以形成两种液态氢化物,M的最高价氧化物对应的水化物呈两性。回答下列问题:
(1)L元素形成单质的名称为______;M在元素周期表中的位置为____;五种元素的原子半径从大到小的顺序是______(用元素符号表示)。
(2)硒(Se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则Se的原子序数为______。
(3)写出由X、Z、L三种元素组成的离子化合物与稀的NaOH溶液加热反应的离子方程式为______。
查看答案和解析>>
科目: 来源: 题型:
【题目】浓硫酸分别和三种钠盐反应,下列分析正确的是

A. 对比①和②可以说明还原性Br->Cl-
B. ①和③相比可说明氧化性Br2>SO2
C. ②中试管口白雾是HCl遇水蒸气所致,说明酸性H2SO4>HCl
D. ③中浓H2SO4被还原成SO2
查看答案和解析>>
科目: 来源: 题型:
【题目】向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系不正确的是
A. ![]() B.
B. ![]() C. n=m+17Vc D.
C. n=m+17Vc D. ![]() m<p<
m<p<![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备MgCO3·3H2O。实验过程如下:
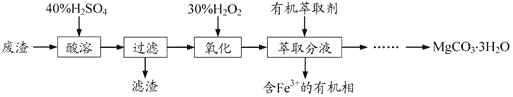
(1)酸溶过程中主要反应的热化学方程式为
MgCO3(s)+2H+(aq)===Mg2+(aq)+CO2(g)+H2O(l) ΔH=-50.4 kJ·mol–1
Mg2SiO4(s)+4H+(aq)="==2" Mg2+(aq)+H2SiO3(s)+H2O(l) ΔH=-225.4 kJ·mol–1
酸溶需加热的目的是_____ _;所加H2SO4不宜过量太多的原因是____ __。
(2)加入H2O2氧化时发生发应的离子方程式为__________
(3)用如图所示的实验装置进行萃取分液,以除去溶液中的Fe3+。
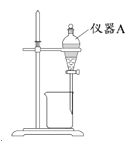
①实验装置图中仪器A的名称为__________。
②为使Fe3+尽可能多地从水相转移至有机相,采取的操作:向装有水溶液的仪器A中加入一定量的有机萃取剂, 、静置、分液,并重复多次。
(4)请补充完整由萃取后得到的水溶液制备MgCO3·3H2O的实验方案:边搅拌边向溶液中滴加氨水, ,过滤、用水洗涤固体2~3次,在50℃下干燥,得到MgCO3·3H2O。
[已知该溶液中pH=8.5时Mg(OH)2开始沉淀;pH=5.0时Al(OH)3沉淀完全]。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
Ⅰ.(1)将钠、钾、镁、铝各1mol分别投入到足量的同浓度的盐酸中,试预测实验结果:____与盐酸反应最剧烈;_________与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明Cl的非金属性比S强,反应的离子方程式为____。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律

(3)仪器B的名称为_____,干燥管D的作用为_______。
(4)若要证明非金属性:Cl>I,则A中加浓盐酸,B中加KMnO4(KMnO4与浓盐酸常温下反应生成氯气),C中加淀粉碘化钾混合溶液,观察到C______的现象,即可证明,从环境保护的观点考虑,此装置缺少尾气处理装置,可用_____溶液吸收尾气。
(5)若要证明非金属性:N>C>Si,则在A中加硝酸、B中加碳酸钙,并在两装置间加一个除去挥发出来的HNO3的装置,C中加_____溶液观察到C中溶液白色沉淀,即可证明。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列乙醇的化学性质中不是由羟基所决定的是( )
A.跟活泼金属Na等发生反应
B.在足量O2中完全燃烧生成CO2和水
C.当Ag或Cu存在时跟O2发生反应生成乙醛和H2O
D.乙醇被酸性高锰酸钾氧化为乙酸
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述正确的是( )
A. 标准状况下,11.2LSO2气体中含氧原子数等于18g水中含有的氧原子数
B. 5.6 g铁与足量稀硫酸反应失去的电子的物质的最为0.3 mol
C. 100g98%的浓硫酸所含的氧原子个数为4mol
D. 20gNaOH溶于1L水,所得溶液中c(Na+)=0.5mol·L-1
查看答案和解析>>
科目: 来源: 题型:
【题目】叠氮化钠(NaN3)可用于汽车安全气囊的添加剂,与酸反应生成N2和H2。某学习小组在实验室用亚硝酸钠和氨在无氧环境中制备NaN3,设计如下实验(夹持装置略去):
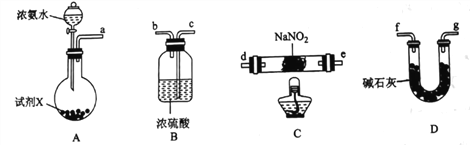
(1)按气流从左到右的方向,上述装置合理的连接顺序为_________________(填仪器接口字母)。
(2)试剂X可选用________________(填试剂名称)。
(3)装置C中发生反应的化学方程式为_________________________________________,该反应需要在无氧环境中进行的原因为_______________________________________________。
(4)装置B的作用为___________________________________________。
(5)加热条件下,NaNH2和N2O反应也可制备NaN3,同时生成能使湿响的红色石蕊试纸变蓝的气体,该反应的化学方程式为_____________________________________________。
(6)HNO2是一元弱酸,不稳定,容易分解为两种氮的氧化物。现用如下试剂:NaNO2、pH试纸、水、稀硫酸、NaOH溶液、碱石灰、CuSO4、CuO,计实验证明((可加热);
①HNO2为弱酸:____________________________________________________。
②装置C中反应进行一段时间后,有NaN3生成:______________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com