
科目: 来源: 题型:
【题目】氮氧化合物是目前造成大气污染的主要气体,而汽车尾气中就含有NO 等多种污染气体。汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致。请结合所学知识回答下列问题:
(1) 已知:N2(g)+2O2(g)![]() 2NO2(g) △H1=+67.8 kJ/mol
2NO2(g) △H1=+67.8 kJ/mol
2NO2(g)![]() O2(g)+2NO(g) △H2=+116.2 kJ/mol
O2(g)+2NO(g) △H2=+116.2 kJ/mol
则N2(g)+O2(g)![]() 2NO(g) △H=_________kJ/mol;汽车启动后,气缸温度越高,单位时间内NO 的排放量越大,分析其原因为_____________
2NO(g) △H=_________kJ/mol;汽车启动后,气缸温度越高,单位时间内NO 的排放量越大,分析其原因为_____________
(2) 若反应N2(g)+O2(g)![]() 2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是________
2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是________
a.2υ正(N2)= υ逆(NO) b.混合气体密度不变
c.生成1molO2的同时生成2molNO d.混合气体平均相对分子质量不变
(3) 汽车尾气净化反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:

①该反应能自发进行的条件为_____ (填“高温”、“低温”或“任意温度”);
②在6~9 min 内,以CO 表示的平均反应速率 υ(CO)=________mol·L-l·min-1;
③第12min时改变的反应条件为_________ (填“升高温度”或“降低温度”);
④反应在第24min时的平衡常数K=____________(只列出计算式,无需计算结果),若保持温度不变,再向容器中充入CO、N2 各0.060mol,平衡将_________移动(填“正向”、“逆向”或“不”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】很多鲜花和水果的香味都来自酯的混合物。下图是乙烯等为原料制取乙酸乙酯的过程(部分产物和反应条件已略去)。

请回答下列问题:
(1)B的结构简式为______________。
(2)乙烯与水反应生成A的反应类型为______________。
(3)A与C反应生成乙酸乙酯的化学方程式为__________,其反应类型为__________。
(4)实验室可用如图装置制取乙酸乙酯。
①在试管a中加好相关试剂后,还需要加入2—3块的碎瓷片,其作用是__________。
②试管b中盛有饱和碳酸钠溶液,生成的乙酸乙酯在该溶液的_______(填“上”或“下”)层,用分液的方法分离出该产品所需的主要仪器是________。试管b中的导管口应在液面上方而不伸入到液面以下,其原因是______________。

查看答案和解析>>
科目: 来源: 题型:
【题目】工业用氧化铝与焦炭在氮气流中加强热制备氮化铝(AlN),氮化铝样品中含少量Al4C3、C、Al2O3杂质。某实验小组拟测定ag氮化铝样品中Al4C3含量并探究甲烷与氧化铜反应的氧化产物为CO2。
已知:(Ⅰ)AlN、Al4C3都能与水反应,分别生成NH3、CH4。
(Ⅱ)CH4还原氧化铜:CH4+4CuO![]() 4Cu+CO2+2H2O。
4Cu+CO2+2H2O。
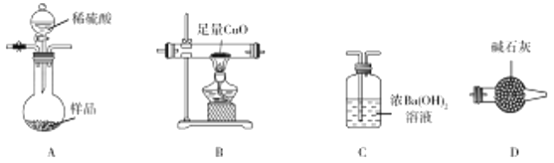
(1)装置连接顺序为 ________________________(按气流从左至右)。
(2)写出A中发生反应的化学方程式:AlN和稀硫酸反应:__________________________;Al4C3与
稀硫酸反应:_______________________________________________________________________。
(3)有下列操作步骤:
①缓缓向A中通入一定量的N2。
②称量B(酒精灯、木块和铁架台除外),按顺序组装仪器,检查装置的气密性,将样品放入烧瓶中;
③点燃B处酒精灯;
④再次称量B;
⑤从分液漏斗中缓慢滴入稀硫酸,直到不再产生气体为止;
⑥再次缓慢通入一定量的N2。
正确的操作顺序是_________________________;操作①的目的是_______________;若操作③与操作⑤顺序颠倒, 将导致测得的Al4C3的质量分数_________(填“偏大”“偏小”或“不变”)。
(4)设计实验证明A中有NH4+生成:__________________________________。
(5)实验结束后,测得B中固体质量减少bg,则样品中Al4C3的质量分数为________×100%。
(6)通过测定C中生成BaCO3的质量可以确定甲烷与氧化铜反应是否有CO生成。实验完毕后,测得B
中固体质量减少bg;对C中混合物进行过滤、洗涤、干燥、称重,当m(BaCO3)=________g时(用含b表达式表示),表明氧化产物只有CO2。
查看答案和解析>>
科目: 来源: 题型:
【题目】铜、硼、硅、砷等元素的化合物是制造新型激光武器和新型太阳能电池的重要材料。回答下列问题:
(1)基态硅原子电子占据的最高能层符号是_____,其中能量最高的电子所占据能级的原子轨道有_____个伸展方向,原子轨道呈_____形。
(2)在硫酸铜溶液中通入过量的氨气,小心蒸发,最终得到深蓝色的[Cu(NH3)4]SO4晶体,晶体中含有的化学键除普通共价键外,还有____________。
(3)硒为第四周期元素,相邻的元素有砷和溴,则三种元素的第一电离能从大到小的顺序为________(用元素符号表示)。H2SeO3的酸性_______H2SeO4(填“强于”或“弱于”),原因是___________(从分子结构的角度回答)。
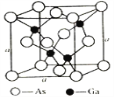
(4)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂。它的晶体结构如下左图所示。六方相氮化硼______π键(填“含有”或“不含”),其质地软的原因是_________。NaBH4是一种重要的储氢载体,阴离子的的立体结构为_______。
(5)砷化镓是优良的第三代半导体材料。如上图所示为GaAs的晶胞结构。
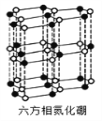
①与GaAs互为等电子体的一种原子晶体的化学式为________。
②已知晶胞的密度是ρ g·cm3,阿伏加德罗常数值为NA,棱长a=_____pm。
查看答案和解析>>
科目: 来源: 题型:
【题目】钛酸钡(BaTiO3)在工业上有重要用途,主要用于制作电子陶瓷、PTC热敏电阻、电容器等多种电子元件。以下是生产钛酸钡的一种工艺流程图:
![]()
已知:①草酸氧化钛钡晶体的化学式为BaTiO(C2O4)2·4H2O;
②25℃时,BaCO3的溶度积Ksp=2.58×10-9;
(1)BaTiO3中Ti元素的化合价为:__________。
(2)用盐酸酸浸时发生反应的离子方程式为: __________。
(3)流程中通过过滤得到草酸氧化钛钡晶体后,为提高产品质量需对晶体洗涤。
①过滤操作中使用的玻璃仪器有_____________________。
②如何证明晶体已洗净?_______________________。
(4)TiO2具有很好的散射性,是一种有重要用途的金属氧化物。工业上可用TiCl4水解来制备,制备时需加入大量的水,同时加热,其目的是:_______________。
(5)某兴趣小组取19.70gBaCO3模拟上述工艺流程制备BaTiO3,得产品13.98g,BaTiO3的产率为:________。
(6)流程中用盐酸酸浸,其实质是BaCO3溶解平衡的移动。若浸出液中c(Ba2+)=0.1mol/L,则c(CO32-)在浸出液中的最大浓度为__________ mol/L。
查看答案和解析>>
科目: 来源: 题型:
【题目】T℃时,在 2 L 的密闭容器中,气体 X、Y 和 Z 三种物质的物质的量随时间变化的曲线如图所示,下列描述正确的是

A. 容器中化学反应为 X(g)+Y(g)![]() Z(g)
Z(g)
B. 0~10 s,X 表示的平均化学反应速率为 0.04 mol/(L·s)
C. 使用催化剂只能加快 0~10 s 间的反应速率
D. 0~4 s 的平均反应速率小于 0~10 s 的平均反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】下列①~⑧中物质间的反应不能产生气体的是 ( )
①石灰石和盐酸 ②冷浓硫酸中投入铝片 ③石英与苏打混和加强热 ④石墨与高温水蒸气 ⑤过氧化钠与水 ⑥氟与水 ⑦钠与硫酸铜溶液 ⑧碳酸氢钠与氢氧化钠溶液
A.①和⑤B.④和⑦C.③和⑦D.②和⑧
查看答案和解析>>
科目: 来源: 题型:
【题目】将1 mol X、3 mol Y充入一个密闭容器中,在一定条件下发生如下反应并达到平衡:X(g) +3Y(g) ![]() 2Z(g);ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是 ( )
2Z(g);ΔH<0。当改变某个条件并达到新平衡后,下列叙述正确的是 ( )
A.升高温度,X的体积分数减小
B.缩小体积,Y的物质的量浓度不变
C.保持容器体积不变,充入1mol的稀有气体He,Z的浓度不变
D.保持容器体积不变,充入2mol的Z(g),X的体积分数增大
查看答案和解析>>
科目: 来源: 题型:
【题目】CO2是造成温室效应的废气,研究二氧化碳的利用具有十分重要的意义。CO2可用来合成低碳烯烃:2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g) ΔH=127.8 kJ/mol。请回答:
C2H4(g)+4H2O(g) ΔH=127.8 kJ/mol。请回答:
(1)已知:H2的燃烧热是285.8kJ/mol,且H2O(g)![]() H2O(l) ΔH=44.0 kJ/mol,则表示C2H4燃烧热的热化学方程式为__________________。
H2O(l) ΔH=44.0 kJ/mol,则表示C2H4燃烧热的热化学方程式为__________________。
(2)图l、图2分别是CO2的平衡转化率(α)随压强及温度的变化关系,已知Z为起始时的投料比,即Z=![]() 。
。

①图l中投料比相同,温度从低到高的顺序为________。
②图2中Z1、Z2、Z3投料比从大到小的顺序为________,理由是____________________。
③若要进一步提高CO2的平衡转化率,除了可以适当改变反应温度外,还可以采取的措施有________________。(任写一种)
(3)若图2中Z1=2.5,在温度为680 K、体积为2 L的恒容密闭容器中,充入1 mol H2和0.4 mol CO2,10 min后达到平衡状态。
①从反应开始到恰好达到平衡时,H2的平均反应速率v(H2)=________。
②680 K时,反应的平衡常数K=________。
(4)在催化剂M的作用下,CO2和H2同时发生下列两个反应:
①2CO2(g)+6H2(g)![]() C2H4(g)+4H2O(g)
C2H4(g)+4H2O(g)
②2CO2(g)+6H2(g)![]() CH3OCH3(g)+3H2O(g) ΔH<0
CH3OCH3(g)+3H2O(g) ΔH<0
下图是乙烯在相同时间内,不同温度下的产率,则高于T℃时乙烯产率降低的原因可能是______。
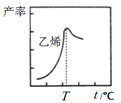
A.催化剂M的活性降低 B.①反应的平衡常数变大
C.②反应的活化能增大 D.生成甲醚的量增加
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com