
科目: 来源: 题型:
【题目】某一元醇的化学式为C6H14O,已知其分子中有二个—CH3、三个—CH2—、一个![]() ,此一元醇可能的结构有
,此一元醇可能的结构有
A. 4种 B. 5种 C. 6种 D. 7种
查看答案和解析>>
科目: 来源: 题型:
【题目】下列各组有机物不论以何种比例混合,只要物质的量之和不变,那么完全燃烧时消耗的氧气的物质的量相等,且所生成的水的物质的量也相等的是( )
A. 甲烷和甲酸甲酯 B. 乙烷和乙酸
C. 乙炔和苯乙烯 D. 苯和苯酚
查看答案和解析>>
科目: 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 标况下,11.2L戊烷分子数为0.5 NAB. 0.5molC3H8分子中C—H共价键个数为2NA
C. 11.2L一氯甲烷所含分子数为0.5NAD. 30g乙烷分子中含有的共用电子对为7NA
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下在一容积不变的密闭容器中发生可逆反应2X(g) ![]() Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
A. 混合气体的密度不再变化 B. 反应容器中Y的质量分数不变
C. X的分解速率与Y的消耗速率相等 D. 单位时间内生成1 mol Y的同时生成2 mol X
查看答案和解析>>
科目: 来源: 题型:
【题目】通常状况下,在体积一定的密闭容器中的NH3和Cl2恰好完全反应,若反应产物只有N2和NH4Cl,则反应前后容器中的压强比应接近于
A.1:11B.11:1C.7:11D.1:1
查看答案和解析>>
科目: 来源: 题型:
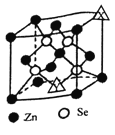
【题目】【选做-选修3:物质结构与性质】硒化锌是一种半导体材料,回答下列问题。
(1)锌在周期表中的位置_______;Se基态原子价电子排布图为______。元素锌、硫和硒第一电离能较大的是________(填元素符号)。
(2)Na2SeO3分子中Se原子的杂化类型为_______;H2SeO4的酸性比H2SeO3强,原因是_______。
(3)气态SeO3分子的立体构型为_______;下列与SeO3互为等电子体的有__(填序号)。
A.CO32- B.NO3- C.NCl3 D.SO32-
(4)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为______(填元素符号);该晶胞中硒原子所处空隙类型为_____(填“立方体”、“正四面体”或正八面体”);若该品晶胞密度为ρg/cm3,硒化锌的摩尔质量为Mg/mol。用NA代表阿伏加德罗常数的数值,则晶胞参数a为_______nm。
查看答案和解析>>
科目: 来源: 题型:
【题目】对尼古丁和苯并[a]芘的分子组成与结构描述正确的是 ( )
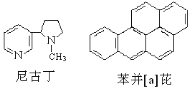
A. 尼古丁为芳香族化合物
B. 尼古丁的分子式为C10H14N2
C. 苯并[a]芘分子中含有苯环结构单元,是苯的同系物
D. 尼古丁分子中的所有碳原子一定不在同一平面上
查看答案和解析>>
科目: 来源: 题型:
【题目】杀虫剂“阿乐丹”的“键线式”表示为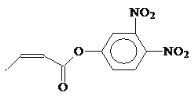 ,若它在稀酸作用下能发生水解反应,生成两种有机物,则此两种有机物具有的共同性质是( )
,若它在稀酸作用下能发生水解反应,生成两种有机物,则此两种有机物具有的共同性质是( )
A. 遇FeCl3溶液均成紫色 B. 均能发生银镜反应
C. 均能与溴水反应 D. 均能与NaOH溶液反应
查看答案和解析>>
科目: 来源: 题型:
【题目】氢气是一种清洁、高效新能源,也是重要的化工原料。
(1)工业上利用甲烷制备氢气的反应为:CH4(g)+H2O(g)![]() CO(g)+3H2(g)
CO(g)+3H2(g)
已知:
①H2(g)+1/2O2(g)![]() H2O(g) △H1=-198kJ/mol
H2O(g) △H1=-198kJ/mol
②CO(g)+1/2O2(g)![]() CO2(g) △H2=-283kJ/mol
CO2(g) △H2=-283kJ/mol
③CH4(g)+2O2(g)![]() CO2(g)+2H2O(g) △H3=-846.3kJ/mol
CO2(g)+2H2O(g) △H3=-846.3kJ/mol
则CH4(g)+H2O(g)![]() CO(g)+3H2(g) △H4=________。
CO(g)+3H2(g) △H4=________。
(2)工业上利用CO和H2合成清洁能源CH3OH,其反应为:CO(g)+2H2(g)![]() CH3OH(g) △H=-116kJ/mo1
CH3OH(g) △H=-116kJ/mo1
①如图表示CO的平衡转化率(α)随温度和压强变化的示意图。X表示的是_______,理由_________;Y1_____Y2(填“<”“=”或“>”)。

②在2L恒容密闭容器中充入2 mol CO和4 mol H2,在一定条件下经过10 min达到平衡状态c点处。则在该条件下,从开始至达到平衡状态v(CH3OH)=_______________,平衡常数Ka、Kb、Kc 的大小关系:___________。
③下列措施既能增大反应速率又能提高反应物的转化率的是_______。
A.使用催化剂 B.及时分离CH3OH C.升高温度 D.增大压强
(3)已知燃料电池的比能量与单位质量燃料物质失去的电子数成正比。理论上H2、CH4、CH3OH的碱性电池的比能量由大到小的顺序为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】铍铜是广泛应用于制造高级弹性元件的良好合金。某科研小组从某废旧铍铜元件(含BeO:25%、CuS:71%、少量FeS和SiO2)中回收铍和铜两种金属的工艺流程如下:
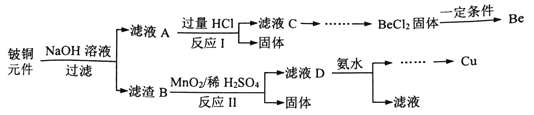
已知:I.铍、铝元素化学性质相似
II.常温下:Ksp[Cu(OH)2]=2.2×10-20、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Mn(OH)2]=-2.1×10-13
(1)滤液A的主要成分除NaOH外,还有_____ (填化学式),写出反应I中含铍化合物与过量盐酸反应的离子方程式_____________。
(2)①溶液C中含NaCl、BeCl2和少量HCl,为提纯BeCl2,选择最合理步骤顺序______。
a.加入过量的NaOH b.通入过量的CO2 c.加入过量的氨水
d.加入适量的HC1 e.过滤 f.洗涤
②从BeCl2溶液中得到BeCl2固体的操作是________________。
(3)①MnO2能将金属硫化物中的硫元素氧化为硫单质,写出反应II中CuS 发生反应的化学方程式______________。
②若用浓HNO3溶解金属硫化物,缺点是____________(任写一条)。
(4)溶液D中含c(Cu2+)=2.2mol/L、c(Fe3+)=0.008mol/L c(Mn2+)=0.01mol/L,逐滴加入稀氨水调节pH可依次分离,首先沉淀的是___ (填离子符号),为使铜离子开始沉淀,常温下应调节溶液的pH值大于____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com