
科目: 来源: 题型:
【题目】肼(N2H4,无色液体)是一种用途广泛的化工原料。实验室中先制备次氯酸钠,再用次氯酸钠溶液和氨反应制备肼并验证肼的性质。实验装置如图所示。
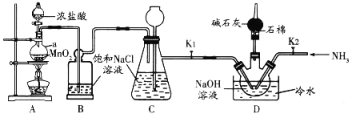
已知:Cl2(g)+2NaOH(aq)=NaC1O(aq)+NaC1(aq)+H2O(g) △H<0。当温度超过40℃时,Cl2与NaOH溶液反应生成NaClO3。回答下列问题:
(1)仪器a的名称是________________,装置B的作用是____________________________。
(2)为控制D装置中的反应温度,除用冷水浴外,还需采取的实验操作是________________。
(3)当三颈烧瓶中出现黄绿色气体时立即关闭分液漏斗活塞、移去酒精灯、关闭K1。此时装置C的作用是________________________________。
(4)将D装置水槽中的冷水换为热水,把三颈烧瓶中黄绿色气体赶走后,打开K2,通入NH3,使其与NaC1O溶液反应制取肼。理论上通入三颈烧瓶的Cl2和NH3的最佳物质的量之比为______________。
(5)请从提供的下列试剂中选择合适试剂,设计合理的实验方案验证肼的还原性____________(说明操作、现象和结论)。
①淀粉-KI溶液 ②稀硫酸(酚酞) ③NaHCO3 ④AgC1
查看答案和解析>>
科目: 来源: 题型:
【题目】砷(As)及其化合物与生产、生活密切相关,广泛应用在杀虫剂以及药物中。回答下列问题:
(1)砷是第四周期VA族元素。下列关于第VA族元素及其化合物的说法不正确的是_______(填序号)。
a.沸点:PH3<NH3
b.酸性:HNO3>H3AsO4
c.As的氧化物的水化物是强碱
d.形成的简单离子半径随着原子序数递增而增大
(2)工业生产中常用“古氏试砷法”检验微量砷,其反应原理为:
①将含砷化合物转化为具有极强还原性的AsH3;
②AsH3与AgNO3溶液反应产生As2O3与另一种固体,该反应的离子方程式为_____________。
(3)砷及其化合物几乎都有毒,通常+3价砷化合物毒性强于+5价砷化合物。海产品中含有微量+5价砷化合物,食用海鲜后不能马上进食水果的原因是________________________________。
(4)砷酸(H3AsO4)可用于制造杀虫剂、药物。As2O3溶于稀硝酸中可得砷酸,此反应的化学方程式为________________________________。
(5)利用单质铁处理水体砷污染的原理为:单质铁在水体中被氧化腐蚀得到水合氧化铁[Fe(OH)3和FeOOH],吸附沉降砷的化合物。在其它条件一定时,调节水样的pH,得到除砷效率曲线如图所示。
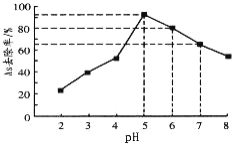
①请解释水样酸性较强时,除砷效率较低的原因是_____________________。
②国家饮用水标准规定水中砷的含量应低于0.05mg·L-1(1mg=1000μg)。某水样中含砷总浓度为100μg·L-1,若控制水样的pH=6,出水后的砷浓度_________________(填“能”或“否”)达到饮用水标准。
查看答案和解析>>
科目: 来源: 题型:
【题目】⑴现有分子式为CllH16的一烷基取代苯,已知它可以被酸性KMnO4溶液氧化成为![]() ,它的异构体共有7种,其中的3种是
,它的异构体共有7种,其中的3种是![]() 、
、![]() 、
、![]()
请写出其他4种的结构简式:____________________、______________________ 、
_____________________、__________________________。
(2)化合物甲:![]() 能使Br2的CCl4溶液褪色,写出甲与Br2发生等物质的量加成反应时可能产物的结构简式_________ ,_____________,_____________。
能使Br2的CCl4溶液褪色,写出甲与Br2发生等物质的量加成反应时可能产物的结构简式_________ ,_____________,_____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】钛被称为继铁、铝之后的第三金属。工业上常用硫酸酸解钛铁矿(主要成分为FeTiO3,还含有部分Fe2O3)的方法制取金红石(TiO2),再还原TiO2制取金属钛。工业制取TiO2的工艺流程图如下:
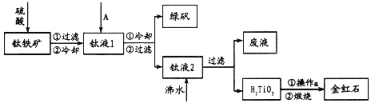
回答下列问题:
(1)钛酸亚铁(FeTiO3)中Ti的化合价为________________________。
(2)钛液1中钛以TiO2+的形式存在,则FeTiO3与硫酸反应的离子方程式为________。
(3)为提高钛铁矿的酸解率,可添加适量氧化剂,依据右图判断,添加的最佳氧化剂为_____________(填化学式)。

(4)钛液1中加入的A物质是____________,流程中的操作a是____________。
(5)制取金红石过程中,需要测定TiO2+的含量。取100mL钛液1,加铝粉,使其发生反应3TiO2++Al+6H+=3Ti3++Al3++3H2O,反应消耗铝1.35g,则钛液1中TiO2+的物质的量浓度为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列选项中的物质所属类别正确的是
选项 | 物质 | 类别 |
A | 空气、石油、干冰 | 混合物 |
B | 水银、金刚石、水晶 | 单质 |
C | 胆矾、硝酸、水 | 电解质 |
D | 硫酸、盐酸、过氧化钠 | 化合物 |
A.AB.BC.CD.D
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C为三种链烃,其碳原子数有如下组合:
组 别 | 碳原子数 | ||
A | B | C | |
① | 3 | 3 | 6 |
② | 3 | 3 | 4 |
③ | 1 | 4 | 5 |
④ | 2 | 4 | 4 |
⑤ | 5 | 2 | 7 |
⑥ | 2 | 2 | 4 |
试回答下列问题:
(1)若B、C为烷烃,且在一定条件下C可分解(裂化)为A和B,则满足此条件的可能组别是(填组别序号)______________________________________________。
(2)若组别⑥中A为烷烃,B为炔烃,C为烯烃,且A、B、C三种物质按物质的量1:1:2混合,取标准状况下该混合物和过量O2组成的混合气体840mL,电火花点燃,将燃烧后的产物用过量碱石灰吸收,碱石灰增重0.93g。求:碱石灰吸收后所剩气体在标准状况下的体积 _______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】一定温度下,在一容器内进行某一反应,M、N的物质的量随反应时间变化的曲线如下图所示,则下列叙述中,正确的是( )
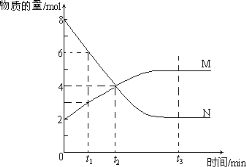
A. 反应的化学方程式一定为2M![]() N
N
B. ![]() 时,逆反应速率一定大于正反应速率
时,逆反应速率一定大于正反应速率
C. ![]() 时,反应达到了化学平衡状态
时,反应达到了化学平衡状态
D. ![]() 时,正反应速率等于逆反应速率
时,正反应速率等于逆反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应中,水既不是氧化剂、也不是还原剂的氧化还原反应是
A. Mg+2H2O===Mg(OH)2+H2↑ B. 2F2+2H2O===4HF+O2
C. Na2O+H2O===2NaOH D. 2Na2O2+2H2O===4NaOH+O2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】某学生用锌片、铜片、发光二极管、滤纸、导线等在玻璃片制成如图所示的原电池,当滤纸用醋酸溶液润湿时,二极管发光.下列有关该电池的说法正确的是( )
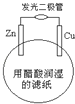
A. 铜片上的电极反应:Cu — 2e﹣ = Cu2+
B. 锌片为电池的负极
C. 外电路中电子由铜片经导线流向锌片
D. 电池工作时电能直接转化为化学能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com