
科目: 来源: 题型:
【题目】A、B、C、D、E四种短周期元素,它们的原子序数依次增大。其中A与C、B与E分别是同主族元素。已知B、E两元素间可形成EB2和EB3两种化合物,两者相对分子质量相差16。又知A、C两元素原子序数之和是B、E两元素原子序数之和的![]() , D的单质是一种常见的半导体材料。请回答下列问题:
, D的单质是一种常见的半导体材料。请回答下列问题:
(1)D位于元素周期表的位置是___________________。
(2)写出由B、C两种元素形成的原子个数比为1:1的化合物的电子式:________,该化合物中所含化学键的类型有_________________。
(3)A2B与A2E的沸点:A2B______A2E(填“高于”或“低于”),其原因是:___________________________。
(4)由A、B、C、E四种元素形成的物质X,与盐酸反应能够生成具有刺激性气味的气体。写出X与盐酸反应的离子方程式:___________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】锌溴液流电池是一种新型电化学储能装置(如下图所示),电解液为溴化锌水溶液,电解液在电解质储罐和电池间不断循环。下列说法正确的是( )
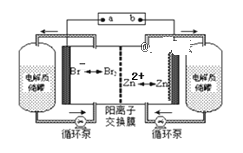
A. 充电时阴极的电极反应式为:Br2+2e-=2Br-
B. 放电时每转移2mol电子,负极区质量减少65克
C. 放电时左侧电解质储罐中的离子总浓度增大
D. 充电是b接电源的正极,Zn2+通过阳离子交换膜由左侧流向右侧
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验:
(1)若要比较镁、铝的金属性强弱,下列方案可行的是:____________(填序号)。
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将等量的这两种元素的单质粉末分别与同浓度的盐酸反应
c.将这两种元素的单质粉末分别与热水作用,并滴入酚酞溶液
d.比较这两种元素的气态氢化物的稳定性
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?_________;说明理由:______________________________________________。
(3)利用如图装置(夹持装置省略)可以验证部分元素的非金属性强弱。
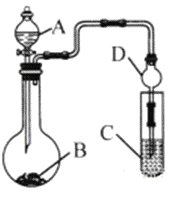
①实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请在其中选择合适药品设计实验验证氯的非金属性大于硫,烧瓶中发生反应的化学方程式为:_____________________________________________。装置C中的实验现象为有淡黄色沉淀生成,离子方程式为:_____________________________。
②若要自选药品证明非金属性:C>Si,则A中加__________、B中加Na2CO3粉末、C中加_____________,观察到C中溶液的现象为_________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】请按要求回答下列问题:
(1)下列物质:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥MgCl2 ⑦CaO ⑧CO2,其中只存在离子键的是:_________(用序号回答,下同。);既存在离子键又存在共价键的是:_________;试写出⑧的电子式:__________。
(2)在下列物质中,互为同分异构体的是_________(填序号,下同。);互为同素异形体的是_________;互为同系物的是_________;互为同位素的是_________;为同一物质的是_________。
①液氨和氨气 ②NH4CNO和CO(NH2)2 ③4019K和4020Ca ④白磷和红磷 ⑤35Cl和37Cl ⑥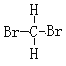 和
和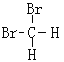 ⑦CH3CH3 和
⑦CH3CH3 和![]() ⑧CH4和 CH2=CH-CH3 ⑨CH2=CH-CH3 和
⑧CH4和 CH2=CH-CH3 ⑨CH2=CH-CH3 和![]()
查看答案和解析>>
科目: 来源: 题型:
【题目】人工光合作用能够借助太阳能,用CO2和H2O制备化学原料。下图是通过人工光合作用制备HCOOH的原理示意图,下列说法不正确的是
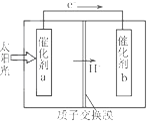
A. 该过程是将太阳能转化为化学能的过程
B. 催化剂a表面发生氧化反应,有O2产生
C. 催化剂a附近酸性减弱,催化剂b附近酸性增强
D. 催化剂b表面的反应是CO2+2H++2e一=HCOOH
查看答案和解析>>
科目: 来源: 题型:
【题目】下列哪一事实能说明生物界与非生物界具有统一性
A. 生物与非生物都具有化学变化
B. 生物与非生物都由元素构成
C. 组成生物体的化学元素在无机自然界中都可以找到
D. 生物与非生物都含有碳元素
查看答案和解析>>
科目: 来源: 题型:
【题目】常温下,用0.1000mol/L NaOH溶液滴定20.00mL 0.1000mol/L HCl溶液,滴定曲线如图所示,下列说法不正确的是
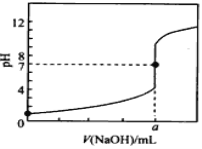
A. a=20.00
B. 滴定过程中,可能存在:c(Cl-)>c(H+)>c(Na+)>c(OH-)
C. 若将盐酸换成相同浓度的醋酸,则滴定到pH=7时,a<20.00
D. 若用酚酞作指示剂,当滴定到溶液明显由无色变为浅红色时立即停止滴定
查看答案和解析>>
科目: 来源: 题型:
【题目】请按要求回答下列问题:
(1)在2L密闭容器内,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
①如图中,表示NO2变化曲线的是_______ 。用O2表示从0s ~2s内该反应的平均速率V=__________。
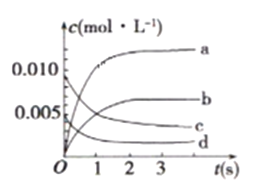
②能说明该反应已达到平衡状态的是___________
A.v(NO2)=2v(O2) B.容器内压强保持不变
C.容器中氧气体积分数不变 D.容器内密度保持不变
(2)为了探究铝电极在原电池中的作用,设计并进行了以下一系列实验,试完成有关问题:
实验编号 | 电极材料 | 电解质溶液 |
1 | Al、Mg | 稀盐酸 |
2 | Al、Cu | 稀盐酸 |
3 | Al、C(石墨) | 稀盐酸 |
4 | Al、 | 氢氧化钠溶液 |
5 | Al、Zn | 浓硝酸 |
①实验1中Al所作的电极是______(填“正极”或“负极”)。
②实验2中H+移向______(填“Al”或“Cu”),Cu极发生_____反应(填“氧化”或“还原”)。
③实验3中石墨的电极反应式: _________________。
④实验4中铝作______极,写出总反应的化学方程式:_______________________。
⑤实验5中负极的电极反应式为:__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列离子方程式书写正确的是( )
A. 澄清石灰水与过量的小苏打溶液反应:Ca2++OH-+HCO3-===CaCO3↓+H2O
B. 酸性高锰酸钾溶液与稀草酸反应:5C2O42-+2MnO4-+16H+===2Mn2++10CO2+8H2O
C. AgCl的悬浊液中滴加Na2S溶液:2AgCl+S2-===Ag2S+2Cl-
D. NH4HCO3溶液加入过量NaOH溶液加热:NH4++OH-===NH3H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com