
科目: 来源: 题型:
【题目】如图甲是一种利用微生物将废水中的尿素(H2NCONH2)的化学能直接转化为电能并生成环境友好物质的装置,同时利用此装置的电能在铁上镀铜,下列说法中正确的是( )

A. 乙装置中溶液颜色会变浅
B. 铁电极应与 Y 相连接
C. M 电极反应式:H2NCONH2+H2O-6e-===CO2↑+N2↑+6H+
D. 当 N 电极消耗 0.25 mol 气体时,铜电极质量减少 16 g
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列判断正确的是

A. a为负极、b为正极
B. 电解过程中,c电极上发生氧化反应
C. d为阳极,电极反应为:2Cl―2e-=Cl2↑
D. 电解过程中,化学能转化为电能
查看答案和解析>>
科目: 来源: 题型:
【题目】气体的自动化检测中常应用根据原电池原理设计的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。

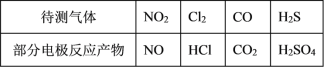
则下列说法中正确的是
A. 上述气体检测时,敏感电极均作电池负极
B. 检测 Cl2 气体时,敏感电极的电极反应式为 Cl2+2e-=2Cl-
C. 检测 H2S 气体时,对电极充入空气,对电极上的电极反应式为 O2+2H2O+4e-=4OH-
D. 检测 Cl2 和 CO 体积分数相同的两份空气样本时,传感器上电流大小、方向相同
查看答案和解析>>
科目: 来源: 题型:
【题目】某实验小组用下图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯):
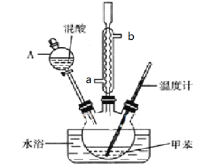
反应原理: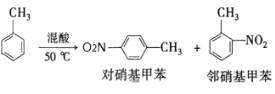
实验中可能用到的数据:
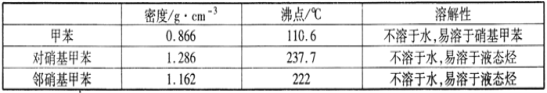
相对原子质量:H-1 C-12 N-14
实验步骤:①浓硫酸与浓硝酸按体积比1:3配制混合溶液(即混酸)共40mL;
②在三颈瓶中加入13g甲苯(易挥发),按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸;
④控制温度约为50℃,反应大约10 min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯,经提纯最终得到纯净的一硝基甲苯共15 g。
请回答下列问题:
(1)实验前需要在三颈瓶中加入少许________,目的是____________________。
(2)冷凝管的作用是______________;冷却水从冷凝管的_______(填“a”或“b”)端进入。
(3)仪器A的名称是________ ,使用该仪器前必须进行的操作是_________________。
(4)分离反应后产物的方案如下:

其中,操作1的名称为________,操作2必需的玻璃仪器有酒精灯、温度计、锥形瓶、牛角管(尾接管)和________________、_________________。
(5)本实验中甲苯的转化率为________(结果保留3位有效数字)。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+3/2O2(g)===CO2(g)+2H2O(g)ΔH=-a kJ/mol,则 a___238.6(填“>”、“<”或“=”)。
(2)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:_________________________________。
(3)反应mA(g)+nB(g)![]() pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
pC(g) +qD(g)过程中的能量变化如图所示,回答下列问题。
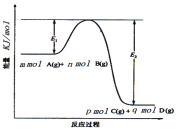
该反应△H =____(用含E1、E2式子表示);在反应体系中加入催化剂,E1___,E2___,(填增大、减小、不变)。
(4)已知:CO (g) +H2O (g)![]() H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
H2 (g) +CO2 (g)平衡常数K随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
回答下列问题:
①该反应的ΔH=__________填“>”、“=”或“<”)。
②已知在一定温度下,C(s) +CO2 (g)![]() 2CO(g)平衡常数K1;C (s) +H2O (g)
2CO(g)平衡常数K1;C (s) +H2O (g)![]() CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是__________________________。
CO(g) +H2 (g)平衡常数K2。则K、K1 、K2之间的关系是__________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】有关热化学方程式书写与对应表述均正确的是
A. 稀硫酸与0.1 mol/L NaOH 溶液反应:H+(aq)+OH-(aq)= H2O(l) △H = +57.3 kJ·mol1
B. 已知 2C(s)+O2(g)=2CO(g)△H= -221 kJ·mol-1, 则可知 C 的热值为 110.5 kJ·mol1
C. 0℃、30MPa 下,将 0.5mol N2 和 1.5molH2 置于密闭的容器中充分反应生成 NH3(g),放热 19.3kJ, 其热化学方程式为:N2(g) + 3H2(g) ![]() 2NH3(g) △H= -38.6kJ·mol1
2NH3(g) △H= -38.6kJ·mol1
D. 密闭容器中,0.3mol 硫粉与 0.2mol 铁粉混合加热生成硫化亚铁 0.2mol 时,放出 19.12 kJ 热量, 则 Fe(s)+S(s)=FeS(s)△H= - 95.6 kJ·mol1
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.离子化合物中可能含有共价键
B.分子晶体中的分子内不含有共价键
C.分子晶体中一定有非极性共价键
D.分子晶体中分子一定紧密堆积
查看答案和解析>>
科目: 来源: 题型:
【题目】易混易错题组
(1)在一定温度下的定容容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的浓度之比等于化学计量数之比,⑦某种气体的百分含量
①能说明2SO2(g)+O2(g) ![]() 2SO3(g)达到平衡状态的是________。
2SO3(g)达到平衡状态的是________。
②能说明I2(g)+H2(g) ![]() 2HI(g)达到平衡状态的是________。
2HI(g)达到平衡状态的是________。
③能说明C(s)+CO2(g) ![]() 2CO(g)达到平衡状态的是________。
2CO(g)达到平衡状态的是________。
④能说明NH2COONH4(s) ![]() 2NH3(g)+CO2(g)达到平衡状态的是________。
2NH3(g)+CO2(g)达到平衡状态的是________。
(2)对于以下三个反应,从正反开始进行达到平衡后,保持温度、体积不变,按要求回答下列问题。
①PCl5(g) ![]() PCl3(g)+Cl2(g),再充入PCl5(g)平衡向________方向移动,达到平衡后,PCl5(g)的转化率_____,PCl5(g)的百分含量______。
PCl3(g)+Cl2(g),再充入PCl5(g)平衡向________方向移动,达到平衡后,PCl5(g)的转化率_____,PCl5(g)的百分含量______。
②2HI(g) ![]() I2(g)+H2(g),再充入HI(g)平衡向________方向移动,达到平衡后,HI的分解率________,HI的百分含量________。
I2(g)+H2(g),再充入HI(g)平衡向________方向移动,达到平衡后,HI的分解率________,HI的百分含量________。
③2NO2(g) ![]() N2O4(g),再充入NO2(g),平衡向________方向移动,达到平衡后,NO2(g)的转化率________,NO2(g)的百分含量________。
N2O4(g),再充入NO2(g),平衡向________方向移动,达到平衡后,NO2(g)的转化率________,NO2(g)的百分含量________。
(3)一定的条件下,合成氨反应为:N2(g)+3H2(g)![]() 2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量的变化,图2表示在2L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
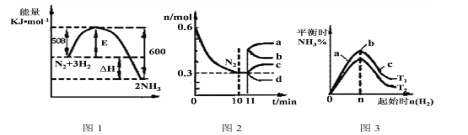
①该反应的平衡常数表达式为_______,升高温度,平衡常数______(填“增大”或“减小”或“不变”)。
②由图2分析,从11min起其它条件不变,压缩容器的体积为1L,则n(N2)的变化曲线为______(填“a”或“b”或“c”或“d”)。
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是___点,温度T1____T2(填“>”或“=”或“<”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】a、b、c、d 四种物质之间的转化关系如图所示(部分产物略去),下列说法正确的是

A. 若 a 为 Cl2,b 可能为 NH3,实验室可用加热固体 c 的方法制取 NH3
B. 若 a 为 Fe,b 可能为稀 HNO3,反应②的离子方程式为3Fe+8H++2NO3-===3Fe2++2NO2↑+4H2O
C. 若 a 为 AlCl3 溶液,b 可能为氨水,反应①的离子方程式为Al3++4NH3 ·H2O===AlO2-+4NH4++2H2O
D. 若 a 为 NaOH 溶液,b 可能为 CO2,可用 Ca(OH)2 溶液鉴定 c、d 溶液中的阴离子
查看答案和解析>>
科目: 来源: 题型:
【题目】(一)有下列各组物质:① 126C和136C;②石墨和足球烯;③漂白粉和漂白液主要成分 ④正丁烷和异庚烷;⑤乙烯和聚乙烯;⑥![]() 和
和 ;⑦丙烷和环丙烷 ⑧CH3-CH2-CH2-CH3 和CH3-CH(CH3)CH3。用序号填空:
;⑦丙烷和环丙烷 ⑧CH3-CH2-CH2-CH3 和CH3-CH(CH3)CH3。用序号填空:
(1)____________组两者互为同系物。
(2)____________组两者互为同分异构体
(3)____________组两者属于同位素。
(4)____________组两者互为同素异形体。
(5)____________组两者是同一物质。
(二)乙烯在化工生产领域应用广泛。
(1)乙烯能合成很多有实用价值的有机物。
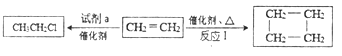
①试剂a是_____________。
②反应Ⅰ的反应类型是_____________。
(2)以原油为起始原料合成聚乙烯的路线如下图所示。
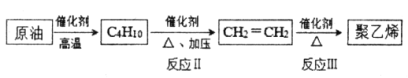
①反应Ⅲ的化学方程式是_____________。
②写出分子式符合C4H10的有机物的结构简式_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com