
科目: 来源: 题型:
【题目】对于放热反应Zn+H2SO4=ZnSO4+H2↑,下列叙述正确的是( )

A. 反应过程中的能量关系可用上图表示
B. 1 mol Zn的能量大于1 mol H2的能量
C. 若将其设计为原电池,则其能量转化形式为电能转化为化学能
D. 若将其设计为原电池,当有32.5gZn溶解时,正极放出的气体一定为11.2L.
查看答案和解析>>
科目: 来源: 题型:
【题目】在同一温度下,某强电解质溶液a,弱电解质溶液b,金属导体c的导电能力相同,则升高温度后它们的导电能力:( )
A.a>b>cB.a=b=cC.c>a>bD.b>a>c
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下,将3 mol A和1 mol B两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() xC(g)+2D(s)。2 min时该反应达到平衡,生成了0.8 mol D,并测得C的浓度为0.2 mol·L-1。下列判断错误的是( )
xC(g)+2D(s)。2 min时该反应达到平衡,生成了0.8 mol D,并测得C的浓度为0.2 mol·L-1。下列判断错误的是( )
A. x=1
B. 平衡时B与C的浓度之比为3∶2
C. 平衡时A与B的转化率相等,均为40%
D. 平衡时加入少量D可提高该反应的反应速率
查看答案和解析>>
科目: 来源: 题型:
【题目】已知A、B、C、D、E五种元素为周期表前20号元素且原子序数依次增大,其中只有A、D为非金属元素。A的气态氢化物溶于水得到的溶液能使酚酞溶液变红。B、C、D的最高价氧化物对应水化物相互之间能够两两反应,且D原子最外层电子数是C原子最外层电子数的2倍。B、E元素同主族。
(1)E在元素周期表中的位置:____________,写出E的最高价氧化物对应水化物与C的单质反应的化学方程式:___________________________________。
(2)A的气态氢化物溶于水后的电离方程式为________________________________。
(3)B单质在空气中燃烧后的产物的电子式为____________,产物中存在的化学键类型有_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】A元素的原子最外层电子数是a,次外层电子数是b;B元素的原子M层电子数是(a-b),L层电子数是(a+b),则A、B两元素形成化合物的化学式最可能表示为( )
A.B3A2B.BA2
C.A3B2D.AB2
查看答案和解析>>
科目: 来源: 题型:
【题目】根据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示,其中盐桥为琼脂-饱和硝酸钾盐桥。请回答下列问题:

(1)电极X的材料是______;电解质溶液Y是_____;
(2)银电极为电池的______极,写出电极反应式:银电极________;X电极:________。
(3)外电路中的电子是从______电极流向______电极。
(4)盐桥中向CuSO4溶液中迁移的离子是______(填序号)。
A.K+ B.NO3- C.Ag+ D.SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)H2O的沸点高于H2S是因为________________;H2O分子比H2S分子稳定是因为__________________。
(2)Al和铁红发生铝热反应的化学方程式_________________,该反应的用途是_________________(任写一条)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列化学反应,其中①②③属于同种反应类型。根据如图回答下列问题:
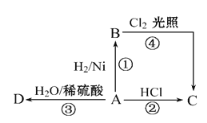
(1)写出A、B、C、D的结构简式:A__,B__,C__,D__。
(2)写出②、④两步反应的化学方程式,并注明反应类型。
②_________________,反应类型________。
④_________________,反应类型________。
查看答案和解析>>
科目: 来源: 题型:
【题目】图中甲池的总反应式为2CH3OH+3O2+4KOH=2K2CO3+6H2O,下列说法正确的是 ( )
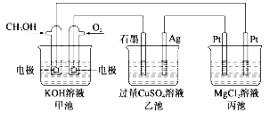
A.甲池电能转化为化学能,乙、丙池化学能转化为电能
B.甲池中通入CH3OH的电极反应式为: CH3OH-6e-+2H2O= CO+8H+
C.甲中消耗280 mL(标准状况下)O2时,丙池理论上最多产生1.45 g固体
D. 反应一段时间后,向乙池中加入一定量Cu(OH)2固体能使CuSO4溶液恢复到原浓度
查看答案和解析>>
科目: 来源: 题型:
【题目】工业合成氨反应:N2+3H2![]() 2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1 mol H-H键、1 mol N-H键、1 mol N≡N键放出能量分别为436 kJ、391 kJ、946 kJ。则:
2NH3是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1 mol H-H键、1 mol N-H键、1 mol N≡N键放出能量分别为436 kJ、391 kJ、946 kJ。则:
(1)若1 mol N2完全反应生成NH3可________(填“吸收”或“放出”)热量________kJ。
(2)如果将1 mol N2和3 mol H2混合,使其充分反应,放出的热量总小于上述数值,其原因是________________________。
(3)实验室模拟工业合成氨时,在容积为2 L的密闭容器内,反应经过10 min后,生成10 mol NH3,则用N2表示的化学反应速率为________mol·L-1·min-1。
(4)一定条件下,当合成氨的反应达到化学平衡时,下列说法正确的是________。
a.正反应速率和逆反应速率相等
b.正反应速率最大,逆反应速率为0
c.N2的转化率达到最大值
d.N2和H2的浓度相等
e.N2、H2和NH3的体积分数相等
f.反应达到最大限度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com