
科目: 来源: 题型:
【题目】H2S与CO2高温下发生反应:H2S(g)+CO2(g) ![]() COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 molH2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g)。在610 K时,将0.10 mol CO2与0.40 molH2S充入2.5 L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
(1)H2S的平衡转化率α1=________%,反应平衡常数K=___________________。
(2)在620K重复实验,平衡后水的物质的量分数为0.03,H2S的转化率α2________α1,该反应的ΔH____0(填“>”“<”或“=”)。
(3)向反应器中再分别充入下列气体,能使H2S转化率增大的是______(填标号)。
A.H2S B.CO2 C.COS D.N2
查看答案和解析>>
科目: 来源: 题型:
【题目】已知:pCu=-1gc(Cu+),pX=-lgc(X-)。298K时,Ksp(CuCl)=a×10-6,Ksp(CuBr)=b×10-9,Ksp(CuI)=c×10-12。在CuCl、CuBr、CuI的饱和溶液中阳离子和阴离子浓度关系如图所示。下列说法正确的是

A. 298K时,在CuCl的饱和溶液中加入少量NaCl,c(Cu+)和c(Cl-)都减小
B. 图中x代表CuI曲线,且P点c(Cu+)=c(I-)
C. 298K时增大M点的阴离子浓度,则y上的点向N点移动
D. 298K时CuBr(s)+I-(aq) ![]() CuI(s)+Br-(aq)的平衡常数K的数量级为103或102
CuI(s)+Br-(aq)的平衡常数K的数量级为103或102
查看答案和解析>>
科目: 来源: 题型:
【题目】配制一定物质的量浓度的Na2CO3溶液,下列操作正确的是
A. 称量时,将Na2CO3固体直接放在托盘天平的右盘上
B. 将Na2CO3固体在烧杯中溶解,所得溶液冷却到室温,再转移至容量瓶中
C. 定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分
D. 定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线
查看答案和解析>>
科目: 来源: 题型:
【题目】短周期主族元素X、Y、Z、W、R、Q原子序数依次增大。由这些元素组成的化合物甲、乙、丙、丁的0.1mol/L水溶液pH如下表,丙、丁为二元化合物。甲溶液逐滴滴入丙溶液中,先产生白色沉淀,后沉淀消失;乙的水溶液可除油污。下列说法一定正确的是

A. W和Q形成的化合物只含有离子键
B. Y和Z的氢化物沸点:Y<Z
C. 离子半径:r(Q>r(R)>r(Z)
D. Y和Q氧化物的水化物酸性:Q>Y
查看答案和解析>>
科目: 来源: 题型:
【题目】镁铝合金、铁合金、硅酸盐都是广泛的建筑材料。回答下列问题
(1)铝的原子结构示意图为___________;在周期表中第___周期,第____族;铝是一种活泼的金属,但在空气中不易被腐蚀,原因是________________________________(用化学方程式表示);写出铝与烧碱反应的离子方程式___________________。
(2)钢是用途最广、用量最多的铁合金,某种钢由铁和另一种元素组成,将少量的钢样品与足量热的浓硫酸充分反应生成两种气体,写出生成两种气体的化学方程式________________________;用长滴管向硫酸亚铁溶液中滴加煮沸过的氢氧化钠溶液,观察到的现象是______________;反应的化学方程式为_________________________;______________。
(3)滑石粉的主要成分是Mg3[Si4O10](OH)2,用氧化物表示其组成:______;二氧化硅能与一种酸反应,可根据此反应原理制雕花玻璃,这种酸是_______;常用的硅酸盐产品有_____、 _______、______。
查看答案和解析>>
科目: 来源: 题型:
【题目】用1L1.0mol/L的NaOH溶液吸收0.8molSO2,所得溶液中的SO32-和HSO3-的物质的量之比为( )
A.1:3B.1:2C.2:3D.3:2
查看答案和解析>>
科目: 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(用元素符号或化学式回答下列问题)
(1)在这些元素中,化学性质最不活泼的是_______,其原子结构示意图是_________。
(2)用电子式表示元素④与⑦组成的化合物的形成过程:________,该化合物属于_______(填“共价”或“离子”)化合物。
(3)常温下呈液态的非金属单质是_______。
(4)表中能形成两性氢氧化物的元素是_________,该元素的单质与⑨的最高价氧化物的水化物反应的化学方程式是___________。
(5)①、⑥、⑦三种元素的最高价氧化物对应的水化物中,按酸性增强的顺序排列为_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】对于反应CO(g)+H2O(g)![]() CO 2(g)+ H 2(g) △H﹤0,在其他条件不变的情况下
CO 2(g)+ H 2(g) △H﹤0,在其他条件不变的情况下
A. 加入催化剂,改变了反应的途径,反应的△H也随之改变
B. 改变压强,平衡不发生移动,反应放出的热量不变
C. 升高温度,反应速率加快,反应放出的热量不变
D. 若在原电池中进行,反应放出的热量不变
查看答案和解析>>
科目: 来源: 题型:
【题目】A是石油裂解气的主要产物之一,其产量是衡量一个国家石油化工发展水平的标志。下列是有机物A~G之间的转化关系:

请回答下列问题:
(1)D中所含官能团的名称是_____________。
(2)反应③的化学方程式是_________________________________。
(3)G是一种高分子化合物,可以用来制造农用薄膜材料等,其结构简式是___________。
(4)在体育竞技比赛中,当运动员肌肉挫伤或扭伤时,随队医生立即对准其受伤部位喷射物质F(沸点12.27℃)进行应急处理。A制备F的化学方程式是_____________。
(5)B与D反应加入浓硫酸的作用是_________;为了得到较纯的E,需除去E中含有的D,最好的处理方法是_____________(用序号填写)。
a.蒸馏 b.用过量饱和碳酸钠溶液洗涤后分液 c.水洗后分液 d.用过量氯化钠溶液洗涤后分液
查看答案和解析>>
科目: 来源: 题型:
【题目】要求完成下列问题。
(1)请根据图示回答:
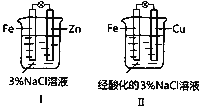
①在Ⅰ中,Zn为_____________极(填“正”或“负”)。
②在Ⅱ中,负极反应式为_____________;电子由________极移向_____________极(填“Fe”或“Cu”),溶液中Na+移向_____________极(填“Fe”或“Cu”)。
③在Ⅱ中,酸是足量的。若产生了标准状况下5.6 L的气体,则转移_________mol e-。
(2)铅蓄电池的总反应为:Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O。该电池的负极材料是_________。(填化学式)
2PbSO4+2H2O。该电池的负极材料是_________。(填化学式)
(3)用32 g Cu与300 mL 12 mol/L的浓硝酸反应,当铜全部溶解后,共收集到标准状况下的气体11.2 L(不考虑NO2转化为N2O4),反应消耗的硝酸的物质的量是_____mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com