
科目: 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值,下列说法中不正确的是( )
A. 一定条件下,将1g乙炔溶于12g苯,所得混合物中含有的碳原子数为NA
B. l04g苯乙烯中含有8NA个碳氢键和NA个碳碳双键
C. 在100g质量分数为46%的乙醇水溶液中,含有氢原子数为12NA
D. 14g分子式为CnH2n的烃中含有的碳碳双键数为NA/n
查看答案和解析>>
科目: 来源: 题型:
【题目】如图I所示,甲、乙之间的隔板K和活塞F都可以左右移动,F受压力恒定。甲中充入2mol A和1mol B,乙中充入2mol C和1mol He,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g)![]() 2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是( )
2C(g),反应达到平衡后,再恢复至原温度,则下列说法正确的是( )

A. 达到平衡时隔板K最终停留在0刻度左侧的2到4之间
B. 若达到平衡时隔板K最终停留在左侧1处,则乙中C的转化率小于50%
C. 如图II所示若x轴表示时间,则y轴可表示甲、乙两容器中气体的总物质的量或A的物质的量
D. 若达到平衡时隔板K最终停留在左侧靠近2处,则乙中F最终停留在右侧刻度大于4
查看答案和解析>>
科目: 来源: 题型:
【题目】I、下图是全钒液流电池的示意图
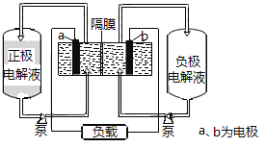
该电池充放电的总反应式为:![]()
请回答下列问题:
(1)充电时的阴极反应式为______________,阳极附近颜色变化是______。
(2)放电过程中,正极附近溶液的pH ________(选填“升高”“降低”或“不变”)。
II、回收利用废钒催化剂(主要成分为V2O5、VOSO4和二氧化硅)的工艺流程如下图所示。
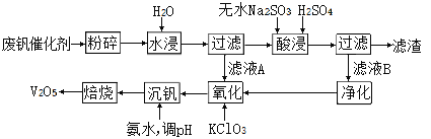
(3)滤渣可用于______________________(填一种用途)。
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间的关系如下表所示:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率(%) | 88.1 | 91.8 | 96.5 | 98 | 99.8 | 97.8 | 96.4 | 93.0 | 89.3 |
根据上表数据判断,加入氨水调节酸碱性,溶液的最佳pH为____;
(5)为了提高钒的浸出率,用酸浸使废钒催化剂中的V2O5转变成可溶于水的VOSO4,酸浸过程中,氧化产物和还原产物的物质的量之比为________。
(6)氧化过程中,VO2+变为VO2+,则该反应的离子方程式为____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列关于各图像的解释或结论正确的是
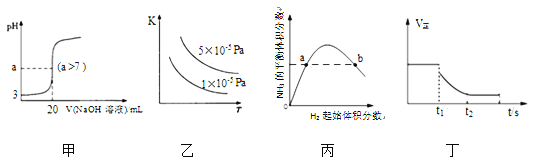
A. 图甲表示常温下向20mL pH=3的醋酸溶液中滴加pH=11的NaOH溶液,溶液的pH随NaOH溶液体积的变化关系
B. 图乙表示2SO2(g)+O2(g)![]() 2SO3(g) △H<0的平衡常数K与温度和压强的关系
2SO3(g) △H<0的平衡常数K与温度和压强的关系
C. 图丙表示一定条件下的合成氨反应,N2的起始量恒定时,NH3的平衡体积分数随H2起始体积分数的变化,图中a点N2的转化率等于b点
D. 图丁表示反应 2SO2+O2 ![]() 2SO3,t1 时刻降低温度符合图示变化
2SO3,t1 时刻降低温度符合图示变化
查看答案和解析>>
科目: 来源: 题型:
【题目】肼(N2H4)和氧气的反应情况受温度影响。某同学设计方案探究温度对产物影响的结果如图所示。下列说法不正确的是
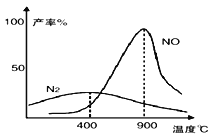
A. 温度较低时, 肼和氧气主要发生的反应N2H4+O2 = N2+2H2O
B. 900℃时,能发生 N2+O2 = 2NO
C. 900℃时, N2的产率与 NO 的产率之和可能小于 1
D. 该探究方案是将一定量的肼和氧气、在密闭容器中进行不断升温实验
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋中蕴含着丰富的资源。利用海水提取淡水、溴和镁的部分过程如图所示。
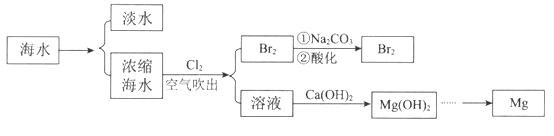
(1)海水淡化的方法有_________________、离子交换法和电渗析法等。
(2)用纯碱吸收浓缩海水吹出的Br2:
3Br2+ 6Na2CO3+3H2O= 5NaBr+ NaBrO3+6NaHCO3。当吸收3 mol Br2时,反应中转移的电子数是_____________。
(3)海水中部分离子的含量如下:
成分 | 含量( mg/L) | 成分 | 含量( mg/L) |
Na+ | 10560 | Cl- | 18980 |
Mg2+ | 1272 | Br- | 64 |
Ca2+ | 400 | SO42- | 2560 |
其中,Mg2+的物质的量浓度是____________。若要从100 L的海水中提取镁,理论上需要加入沉淀剂Ca(OH)2的质量是_______________。
(4)由Mg(OH)2制单质Mg,以下方法最合适的是________________(填序号)。
A.Mg(OH)2 ![]() MgO
MgO![]() Mg
Mg
B.Mg(OH)2![]() MgO
MgO![]() Mg
Mg
C.Mg(OH)2![]() 无水MgCl2
无水MgCl2![]() Mg
Mg
D.Mg(OH)2 ![]() MgCl2溶液
MgCl2溶液![]() Mg
Mg
查看答案和解析>>
科目: 来源: 题型:
【题目】前四周期元素X、Y、Z、R、Q核电荷数逐渐增加,其中X、Y、Z、R四种元素的核电荷数之和为58;Y 原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;R原子的L层电子数与最外层电子数之比为4∶1,其d轨道中的电子数与最外层电子数之比为5∶2;Q2+的价电子排布式为3d9。
回答下列问题:
(1)R基态原子核外电子的排布式为________。
(2)Z元素的最高价氧化物对应的水化物化学式是___________。
(3)Y、Z分别与X形成最简单共价化合物A、B,A与B相比,稳定性较差的是______(写分子式)。
(4)在Q的硫酸盐溶液中逐滴加入氨水至形成配合物[Q(NH3)4]SO4,现象是_________。不考虑空间结构,配离子[Q(NH3)4]2+的结构可用示意图表示为_____(配位键用→标出)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com