
科目: 来源: 题型:
【题目】某同学欲大量配制含有下列四种不同阴、阳离子的溶液,其中能配制成功的是
A. K+、H+、Cl-、CO32- B. Mg2+、Al3+、Cl-、SO42-
C. Na+、H+、NO3-、Fe2+ D. Na+、Ba2+、HCO3-、OH-
查看答案和解析>>
科目: 来源: 题型:
【题目】甲醇可作为燃料电池的原料。通过下列反应可以制备甲醇:CO ( g ) + 2H2 ( g ) ![]() CH3OH ( g ) △H =-90.8 kJ·mol-1 ,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO 的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A 时,容器的体积为20 L。
CH3OH ( g ) △H =-90.8 kJ·mol-1 ,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO 的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A 时,容器的体积为20 L。

(1)T1℃反应的平衡常数为_______________。
(2)图中P1 _______ P2(填“>”、“<”或“=”)。如反应开始时仍充入10 mol CO和20 mol H2,则在平衡状态B时容器的体积V(B)=__________L。
(3)关于反应CO(g)+2H2(g)![]() CH3OH(g)在化学平衡状态B时的描述正确的是________
CH3OH(g)在化学平衡状态B时的描述正确的是________
A.CO的含量保持不变 B.容器中CH3OH浓度与CO浓度相等
C.2v正(CH3OH)= v正(H2) D.容器中混合气体的平均相对分子质量保持不变
(4)已知CO2(g)+H2(g) ![]() CO(g) + H2O(g) △H = + 41.3 kJ·mol-1 ,试写出由CO2和H2制取甲醇的热化学方程式___________________________________。
CO(g) + H2O(g) △H = + 41.3 kJ·mol-1 ,试写出由CO2和H2制取甲醇的热化学方程式___________________________________。
(5)以CH3OH、O2、稀H2SO4组成燃料电池,写出该电池正极的电极反应式:_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引用了各界的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g),该反应的能量变化如图所示:
CH3OH(g)+H2O(g),该反应的能量变化如图所示:
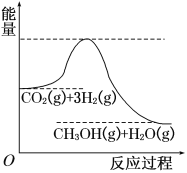
(1)上述反应平衡常数K的表达式为________________,温度降低,平衡常数K________(填“增大”、“不变”或“减小”)。
(2)在体积为2 L的密闭容器中,充入1 mol CO2和3 mol H2,测得CO2的物质的量随时间变化如下表所示。从反应开始到5 min末,用氢气浓度变化表示的平均反应速率v(H2)=________。从反应到平衡时CO2转化率=________
t/min | 0 | 2 | 5 | 10 | 15 |
n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
(3)下列条件能使上述反应的反应速率增大,且平衡向正反应方向移动的是________(填写序号字母)
a.及时分离出CH3OH气体
b.适当升高温度
c.保持容器的容积不变,再充入1 mol CO2和3 mol H2
d.选择高效催化剂
查看答案和解析>>
科目: 来源: 题型:
【题目】思维辨析:
(1)溴乙烷属于烷烃。(______)
(2)卤代烃属于有机化合物,都易燃烧。(______)
(3)卤代烃都可以发生水解反应和消去反应。(______)
查看答案和解析>>
科目: 来源: 题型:
【题目】合成氨工业对国民经济和社会发展具有重要的意义。对于密闭容器中的反应:N2(g)+3H2(g)![]() 2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )
2NH3(g),673 K、30 MPa下n(NH3)和n(H2)随时间变化的关系如下图所示。下列叙述正确的是( )

A. 升高温度,逆反应速率增大,正反应速率减小
B. 点c处反应达到平衡
C. 点d(t1时刻)和点e(t2时刻)处n(N2)不一样
D. 点a的正反应速率比点b的大
查看答案和解析>>
科目: 来源: 题型:
【题目】氧气是我们身边常见的物质,以下有关氧气的叙述正确的是( )
A.在空气中不能燃烧的物质,在氧气中也不能燃烧
B.鱼、虾等能在水中生存,是由于氧气极易溶于水
C.氧气具有可燃性,可以做燃料
D.物质在氧气中燃烧的反应,不一定是化合反应
查看答案和解析>>
科目: 来源: 题型:
【题目】在一定条件下的容积不变的容器中,当下列物理量不再变化时,表明反应A(g)+2B(g)![]() 3C(g)+D(s)已达到平衡的是( )
3C(g)+D(s)已达到平衡的是( )
① 混合气体的压强 ② 混合气体的密度
③ 混合气体的总质量 ④ 气体的总物质的量
A. ① ④B. ② ③C. ① ② ③D. ① ②
查看答案和解析>>
科目: 来源: 题型:
【题目】分类是学习化学的一种重要方法,以下分类不正确的是( )
A.常见的黑色固体:氧化铜、四氧化三铁
B.常见的由原子构成的物质:铜、金刚石
C.常见的含有氧分子的物质:空气、二氧化碳
D.常见的氧化物:氧化铜、氧化镁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com