
科目: 来源: 题型:
【题目】现有下列4种有机物:①CH4 ②CH2=CH2 ③CH3CH2CH2CH3 ④CH3CH2OH ⑤葡萄糖
(1)与①互为同系物的是______(填序号)。
(2)写出④的官能团名称为 _________________ 。
(3)写出③的同分异构体的结构简式_______。
(4)写出③的二氯代物有____________种.
(5)糖尿病通常是指病人尿液中_________的含量高。
查看答案和解析>>
科目: 来源: 题型:
【题目】关于容量瓶的使用,下列说法中错误的是
A. 不能在容量瓶中溶解固体或稀释浓溶液
B. 容量瓶不能加热
C. 容量瓶可以用来长期存放溶液
D. 容量瓶不能作为反应容器
查看答案和解析>>
科目: 来源: 题型:
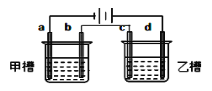
【题目】如图 a、b、c、d均为铂电极,供选择的电解质溶液如下表。要满足条件是:①工作一段时间后,甲槽电解液pH上升,而乙槽电解液pH下降;②b、c两极放电离子的物质的量相等。则应选用的电解液是
组 | A | B | C | D |
甲槽 | KCl | NaCl | NaOH | Cu(NO3)2 |
乙槽 | AgNO3 | NaNO3 | CuSO4 | NaCl |
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种前四周期元素。A的核外电子总数与其 周期数相同;B的价电子排布式为nsnnpn+2;C、D为同周期元素,C是同周期元素中离子半径最小的元素,D元素最外层有一个未成对电子;E位于元素周期表的第四周期第IVB族,常用加热ED4溶液的方法制备纳米材料。
回答下列问题:
(1)D原子的价电子排布图为___________,E原子核外有_____个未成对电子,五种元素中电负性最大的是___________(填元素符号)。
(2)化合物D2B的中心原子的杂化方式为______________,它的VSEPR模型名称____________,分子的立体构型为_____________。
(3)与分子晶体D2B3互为等电子体的一种分子为____________(填化学式)。
(4)由A、B、D三种元素所形成的一系列化合物中氧化性最强的是_______(填化学式,下同),酸性最强的是_________________。
(5)单质B有两种同素异形体,其中沸点高的是______(填分子式),原因是__________。
(6)C与D能形成化合物Q。在1.01×105Pa、T1℃时,气体摩尔体积为53.4L/mol,实验测得Q的气态密度为5.00g/L,则此时Q的化学式为____________________。
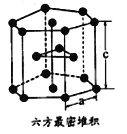
(7)E单质有两种同素异形体,高温下是体心立方堆积,但在常温下的晶体结构为如图所示的六方最密堆积。已知晶胞参数分别为acm和ccm,则该晶体的密度可表示为______g·cm-3。(用含a和c的式子表示,用NA表示阿伏伽德罗常数的值)。
 。
。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列反应过程中的能量变化与右图一致的是

A. 2Al+Fe2O3![]() 2Fe+Al2O3
2Fe+Al2O3
B. C+CO2![]() 2CO
2CO
C. CaCO3![]() CaO+CO2↑
CaO+CO2↑
D. C+H2O![]() CO+H2
CO+H2
查看答案和解析>>
科目: 来源: 题型:
【题目】I.现有一瓶无色澄清溶液,可能由Na+、K+、NH4+、Fe2+、SO42-、I-、CO32-、Cl-、SO32-、MnO4-中的几种组成,请根据以下实验步骤及现象回答下列问题:
步骤一:取适量待测液,加入NaOH溶液并加热,得到溶液A,并产生刺激性气味的气体;
步骤二:向溶液A中加入足量稀盐酸和BaCl2溶液,得到溶液B、白色沉淀及有刺激性气味的气体;
步骤三:向溶液B中通入适量Cl2,得到黄褐色溶液C。
(1)下列有关该溶液说法正确的是________________(填字母)。
A 一定存在SO42-、I-、NH4+、SO32- B 一定不存在Fe2+、CO32-、MnO4-
C 可能存在CO32-、Cl-、Na+、K+、 D 可用AgNO3溶液确认原溶液中是否存在Cl-
(2)步骤三得到黄褐色溶液的离子方程式是____________________。
(3)若向原溶液中先加入足量的盐酸,再加入足量的______________(填化学式)并加热,也能得出步骤一、步骤二相同的结论。
(4)对于溶液中还可能存在的阳离子,确认其存在的实验方法是__________________。
II.用一定质量的铜片和25.0 mL 18.0 mol·L-1的浓硫酸在加热条件充分反应,最终铜片与硫酸均有剩余。假定反应前后溶液的体积不变,设剩余硫酸的浓度为d mol·L-1,现向反应后溶液中缓慢加入硝酸钾固体,充分搅拌直到剩余铜片恰好完全反应,反应消耗硝酸钾____________mol(用含d的代数式表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列叙述中,正确的是 ( )
A. H2SO4的摩尔质量是98
B. 等质量的CO与CO2中所含碳原子数之比为7︰11
C. 等质量的O2和O3中所含的氧原子数相同
D. 98g H2SO4溶解于500mL 所得溶液中硫酸的物质的量浓度为2 molL-1
查看答案和解析>>
科目: 来源: 题型:
【题目】A、B、C、W均为中学常见的物质,它们之间有如图所示的转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
![]()
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如下转化关系:
![]()
(1)若A、B、C三种物质都含有一种金属元素,且B为两性物质,W俗称苛性钠。
①A、B、C三种物质中所含有的金属元素单质与W反应的化学方程式为_______________。
②A溶液一步转化为C溶液的反应离子方程式为________________。
(2)若X是一种黄绿色的气体,Y的饱和溶液滴入沸水中能生成红褐色胶体。
①检验溶液Z是否变质最灵敏的一种试剂是____________________(名称);
②一定条件下W与水反应的化学方程式_______________________________。
(3)X常温下为气体化合物,Z是一种红棕色气体,X气体的检验方法____________________,X转化为Y的化学方程式为______________________;
(4)X为一元强碱溶液,W是形成酸雨的主要气体。
①则Y到Z的离子方程式为________________________________________;
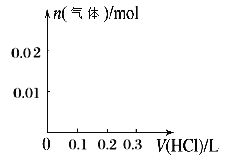
②请画出向含0.01molX和0.01molY的溶液中逐滴加入0.1mol/L稀盐酸的体积和生成气体的物质的量的关系的图像___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 标准状况下,2.24LHF所含分子数为0.1NA
B. 某温度下,2LpH=12的NaOH溶液中含OH-的数目为0.02NA
C. 化学反应中每生成1molO2,转移的电子数为4NA
D. 丙烯和环丙烷组成的42g混合气体分子中共用电子对总数为9NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com