
科目: 来源: 题型:
【题目】下列说法正确的是( )
A.SO2能使KMnO4水溶液褪色
B.可以用澄清石灰水鉴别SO2和CO2
C.硫粉在过量的纯氧中燃烧可以生成SO3
D.少量SO2通过浓的CaCl2溶液能生成白色沉淀
查看答案和解析>>
科目: 来源: 题型:
【题目】如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )
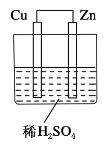
实验后的记录:
①Cu为负极,Zn为正极
②Cu极上有气泡产生,发生还原反应
③SO42-向Cu极移动
④若有0.5 mol电子流经导线,则可产生0.25 mol气体
⑤电子的流向是:Cu―→Zn
⑥正极反应式:Cu+2e-===Cu2+,发生氧化反应
A. ①②③B. ②④C. ②③④D. ③④⑤
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)某温度时,在2 L容器中A、B两种物质间的转化反应中,A、B物质的量随时间变化的曲线如下图所示,由图中数据分析得:
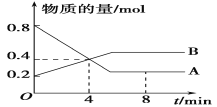
①该反应的化学方程式为____________________;
②反应开始至4 min时,B的平均反应速率为________ ,A的反应速率为_____ ,A的转化率为_____。
③4 min时,反应是否达到平衡状态?________(填“是”或“否”),8 min时,v(正)________v(逆)(填“>”、“<”或“=”)。
(2)下图表示在密闭容器中反应:2SO2(g) + O2(g)![]() 2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是______________;b时改变的条件可能是______________。
2SO3(g)△H<0达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,a时改变的条件可能是______________;b时改变的条件可能是______________。
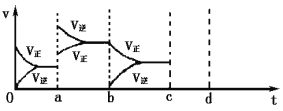
查看答案和解析>>
科目: 来源: 题型:
【题目】三氯化碘(ICl3)在药物合成中用途非常广泛,其熔点:33 ℃,沸点:73 ℃。实验室可用如图装置制取 ICl3。

(1)仪器 a 的名称是_____。
(2)制备氯气选用的药品为漂白精固体[ 主要成分为 Ca(ClO)2] 和浓盐酸, 相关反应的化学方程式为______。
(3)装置 B 可用于除杂,也是安全瓶,能监测实验进行时装置 C 中是否发生堵塞,请写出发生堵塞时 B 中的现象是 ____。
(4)试剂 X 为_____。
(5)氯气与单质碘反应温度稍低于 70 ℃,则装置 D 适宜的加热方式为__。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列说法不正确的是( )
A. 用水可以鉴别苯、四氯化碳、乙醇三种无色液体
B. 用Cu(OH)2悬浊液可以鉴别乙醇、乙酸溶液、葡萄糖溶液
C. 石油的分馏、煤的液化和气化都是物理变化,石油的裂化、裂解都是化学变化
D. 制取环氧乙烷:2CH2=CH2+O2Ag,250℃2![]() ,符合绿色化学的理念
,符合绿色化学的理念
查看答案和解析>>
科目: 来源: 题型:
【题目】下列对科学家的相关成果的说法正确的是( )
A. 屠呦呦发现抗疟新药青蒿素(C15H22O5),青蒿素属于烃类
B. 闵恩泽研发重油裂解的催化剂,催化裂解可以获得很多重要的化工原料
C. 凯库勒研究了苯环的结构,苯环是碳碳单键和碳碳双键交替的结构
D. 门捷列夫提出元素周期律,元素周期律指元素的性质随相对原子质量的递增而呈周期性的变化
查看答案和解析>>
科目: 来源: 题型:
【题目】依据事实,书写下列热化学方程式:
(1)在25℃、101kPa时,1molC与1mol水蒸气反应生成1molCO和1molH2,吸热131.5kJ:______________________________________。
(2)根据下图写出热化学方程式__________________________________________。
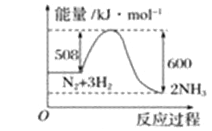
(3)已知稀溶液中,1 mol H2SO4与NaOH溶液恰好完全反应时,放出114.6 kJ热量,写出表示H2SO4与NaOH反应中和热的热化学方程式__________________。
(4)已知:2SO2(g)+O2(g)![]() 2SO3(g) ΔH=-196.6 kJ·mol–1
2SO3(g) ΔH=-196.6 kJ·mol–1
2NO(g)+O2(g)![]() 2NO2(g) ΔH=-113.0 kJ·mol–1
2NO2(g) ΔH=-113.0 kJ·mol–1
请写出NO2与SO2反应生成SO3和NO的热化学方程式____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】W、X、Y、Z 是原子序数依次增大的四种短周期元素。W 的气态氢化物能使紫色石蕊溶液变蓝,W、X和Y三种元素的最高价氧化物的水化物两两之间可以发生反应,W、X、Y、Z 的最外层电子数之和为 16。回答下列问题:
(1)Z 单质的电子式是 ________________。W 的气态氢化物能使紫色石蕊溶液变蓝的原因:__________________(用化学方程式表示)。
(2)X、Y、Z 三种元素的简单离子的离子半径由大到小的顺序是:_____。
(3)Z 最高价氧化物对应的水化物化学式为 ____。
(4)Z 和氧元素、硫元素组成的 SOZ2 是一种液态化合物,沸点为 77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出, 该气体可使滴有品红试液的滤纸褪色。请写出 SOZ2 和水反应的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用,回答下列问题:
(1)氮元素原子的 L 层电子数为 ___________;
(2)肼(N2H4)又称联氨。无色油状液体。有类似于氨的刺鼻气味。可作为火箭发动机的燃料。
①)肼中氮元素的化合价为 ____。
②NH3 与 NaClO 反应可得到肼,该反应的化学方程式为_____。
③16g 液态肼在空气中燃烧,生成氮气和水蒸气时放出的热量为 267.1kJ,写出该反应的热化学方程式: ____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某工业含铜废料含有 Cu、CuO、CuS、CuSO4 等成分,利用该含铜废料可生产硝酸铜晶体[Cu(NO3)2·3H2O],生产的工艺流程如图所示,请回答下列问题:

(1)“焙烧”过程中除生成 SO2 的反应外,另外一个反应的化学方程式是______。
(2)“酸化”过程为加快反应速率,可采用的措施有______(写出一条即可)。
(3)若试剂 a 为 Zn,则“置换”的离子方程式为_____。
(4)“淘洗”的作用是_________________。
(5)“反应”一步中使用 20% HNO3 和 10% H2O2,整个过程无红棕色气体产生,则发生反应的离子方程式为_______________________________________;若该步骤只使用 20% HNO3,随着反应的进行,温度升高,出现大量红棕色气体,则还原剂与氧化剂的物质的量之比为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com